
【题目】在AlCl3和MgCl2的混合溶液中,逐滴加入NaOH溶液直至过量,理论上,加入NaOH的体积和所得沉淀的物质的量的示意图如下,b处NaOH的体积为1L,则下列判断正确的是
( )
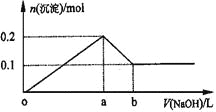
A.混合溶液中Al3+的物质的量为0.2mol
B.NaOH的浓度为0.5 mol/L
C.在b点处溶液中的溶质只有NaAlO2
D.图中线段oa:ab=5:1
【答案】D
【解析】
AlCl3和MgCl2的混合溶液中,逐滴加入NaOH溶液,发生反应生成氢氧化铝、氢氧化镁沉淀,加入aLNaOH溶液时,沉淀达最大值共0.2mol,此时溶液为NaCl溶液,继续滴加NaOH溶液直至过量,氢氧化铝与NaOH反应逐渐溶解,在bL时,即再继续滴加NaOH溶液(b-a)L时,氢氧化铝完全溶解,沉淀为氢氧化镁0.1mol,溶液为NaCl、NaAlO2溶液,据此解答。
A、根据图示信息和Al原子守恒有:n(NaAlO2)=n(AlCl3)=n[Al(OH)3]=0.1mol,故A错误;
B、在bL时,溶液为NaCl、NaAlO2溶液,由图象可知:n[Al(OH)3]=0.1mol,n(Mg(OH)2]=0.1mol,根据Mg原子守恒有n(MgCl2)=n(Mg(OH)2]=0.1mol,根据Al原子守恒有n(NaAlO2)=n(AlCl3)=n[Al(OH)3]=0.1mol,由Cl原子守恒有n(Cl)=n(NaCl)=2n(MgCl2)+3n(AlCl3)=2×0.1mol+3×0.1mol=0.5mol,由Na原子守恒有n(NaOH)=n(NaCl)+n(NaAlO2)=0.5mol+0.1mol=0.6mol,所以c(NaOH)=0.6mol÷1L=0.6mol/L,故B错误;
C、在bL时,即再继续滴加NaOH溶液(b-a)L时,氢氧化铝完全溶解,沉淀为氢氧化镁0.1mol,溶液为NaCl、NaAlO2溶液,故C错误;
D、加入aLNaOH溶液时,沉淀达最大值共0.2mol,由反应方程式可知,此时溶液为NaCl溶液,在bL时,即再继续滴加NaOH溶液(b-a)L时,氢氧化铝与NaOH恰好反应,氢氧化铝完全溶解,沉淀为氢氧化镁0.1mol,溶液为NaCl、NaAlO2溶液,所以两部分NaOH溶液的体积之比等于消耗的NaOH的物质的量之比,即为n(NaCl)与n(NaAlO2)之比,故oa:ab=a:(b-a)=0.5mol:0.1mol=5:1,故D正确。
故选D。


科目:高中化学 来源: 题型:
【题目】某待测溶液(阳离子为Na+)中只可能含有SO42-、SO32-、Cl-、Br-、NO3-、HCO3-中的一种或若干种,进行下列实验(每次实验所加试剂均足量):回答下列问题:
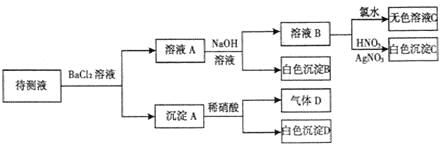
(1)待测液中是否含SO42-、SO32-离子__________________________________________
(2)气体D的化学式为____________,反应生成沉淀B的离子方程式为:____________
(3)根据以上实验,待测液中肯定没有的离子__________________________;肯定存在的离子是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应 A(g)+3B(g)![]() 2C(g)+2D(g)在四种不同情况下的反应速率分别如下,其中反应速率最大的是( )
2C(g)+2D(g)在四种不同情况下的反应速率分别如下,其中反应速率最大的是( )
A.v(A)=0.15mol/(L·min)B.v(B)=0.6 mol/(L·min)
C.v(C)=0.4 mol/(L·min)D.v(D)=0.01 mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M是聚合物胶黏剂、涂料等的单体,其一条合成路线如下(部分试剂及反应条件省略):

完成下列填空:
(1)反应①的反应类型是____________。反应④的反应条件是_____________。
(2)除催化氧化法外,由A得到![]() 所需试剂为___________。
所需试剂为___________。
(3)已知B能发生银镜反应。由反应②、反应③说明:在该条件下,_______________。
(4)写出结构简式。C________________ M________________
(5)D与1-丁醇反应的产物与氯乙烯共聚可提高聚合物性能,写出该共聚物的结构简式。_____________
(6)写出一种满足下列条件的丁醛的同分异构体的结构简式。____________
①不含羰基②含有3种不同化学环境的氢原子
已知:双键碳上连有羟基的结构不稳定。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在通风橱中进行下列实验:
步骤 |
|
| |
现象 | Fe表面产生大量无色气泡,液面上方变为红棕色 | Fe表面产生少量红棕色 气泡后,迅速停止 | Fe、Cu接触后,其表面 均产生红棕色气泡 |
下列说法中,不正确的是( )
A.Ⅰ中气体由无色变红棕色的化学方程式为:2NO+O2=2NO2
B.Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应
C.对比Ⅰ、Ⅱ中现象,说明稀HNO3的氧化性强于浓HNO3
D.针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否持续被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下是利用主要成分为Cu2S和Fe2O3的工业废弃固体(其他成分不参与反应)制备有关物质,实验流程如图所示:
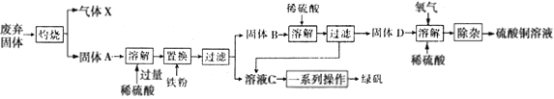
回答下列问题:
(1)气体X的化学式为____。
(2)加入铁粉时发生反应的离子方程式为:2H++Fe=Fe2++H2↑、____。
(3)常温下,固体D、O2和稀硫酸混合后几乎不反应,而加少量绿矾后随即发生反应。已知FeSO4对此反应起催化作用,则催化过程中反应的离子方程式为4Fe2++O2+4H+=4Fe3++2H2O、_____。
(4)除杂时需先加合适的氧化剂将Fe2+氧化为Fe3+,再加试剂Y调节溶液pH以除去Fe3+,则氧化剂及试剂Y可以是____(填编号)。
a.H2O2、CuO b.HNO3、Cu(OH)2 c.KMnO4、CuCl2 d.漂白粉、CuCO3
(5)无水硫酸铜受热分解生成氧化铜和气体,受热温度不同气体可能为SO3、SO2和O2中的一种、两种或三种。现设计如下实验测定产生的SO2、SO3和O2的物质的量,并计算各物质的化学计量数,从而确定CuSO4分解的化学方程式(已知实验结束时,硫酸铜完全分解)。
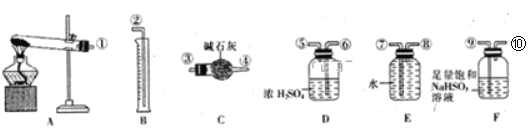
①仪器C的名称是_____,仪器F的作用是____。
②组装探究实验的装置,按从左至右的方向,各仪器接口连接顺序为:①→⑨→⑩→⑥→⑤→_____→ → → →②(填接口序号)。
③若某小组称取6.4g无水CuSO4,实验过程中装置C增加的质量为3.84g,量筒中水的体积折算成标准状况下气体体积224mL,请通过计算确定实验条件下CuSO4分解的化学方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】局部麻醉药普鲁卡因E(结构简式为![]() )的三条合成路线如下图所示(部分反应试剂和条件已省略):
)的三条合成路线如下图所示(部分反应试剂和条件已省略):
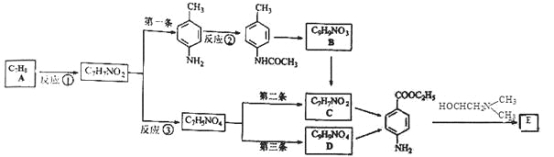
完成下列填空:
(1).比A多一个碳原子,且一溴代物只有3种的A的同系物的名称是___________。
(2).写出反应试剂和反应条件。反应①______;③______
(3).设计反应②的目的是____________。
(4).B的结构简式为_____;C的名称是____。
(5).写出一种满足下列条件的D的同分异构体的结构简式____。
①芳香族化合物 ②能发生水解反应 ③有3种不同环境的氢原子
1 mol该物质与NaOH溶液共热最多消耗_____mol NaOH。
(6).普鲁卡因的三条合成路线中,第一条合成路线与第二条、第三条相比不太理想,理由是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高锰酸钾溶液常用于物质的定性检验与定量分析。
(1)实验室里欲用KMnO4固体来配制240mL 0.1 molL-1的KMnO4酸性溶液。
①需用的仪器有天平、药匙、烧杯、玻璃棒、量筒、胶头滴管、_________
②配制过程中玻璃棒所起的作用是_________
③下列操作对实验结果的影响偏小的是______(填序号)
a.加水定容时俯视刻度线 b.容量瓶内壁附有水珠而未干燥处理
c.若未用蒸馏水洗涤烧杯内壁或未将洗涤液注入容量瓶
d. 颠倒摇匀后发现凹液面低于刻度线又加水补上
④下列为打乱了的操作示意图,请按先后顺序正确排序_______。

(2)用上述酸性KMnO4溶液来测定FeSO4溶液中Fe2+的物质的量浓度。
①配平该反应的化学方程式:
__FeSO4+ KMnO4+ H2SO4= K2SO4+ MnSO4+ Fe2(SO4)3+ H2O
②该反应中的氧化剂是__________,氧化产物是__________
③若消耗3.16gKMnO4,则该反应转移的电子数目为______
(3)已知反应:①Cl2+2KBr=2KCl+Br2,②2KMnO4+16HCl(浓) =2KCl + 2MnCl2+ 5Cl2↑+8H2O,③Br2+K2S=2KBr+S。
①下列说法正确的是___。
A.上述三个反应都有单质生成,所以都是置换反应
B.氧化性由强到弱顺序为KMnO4>Cl2>Br2>S
C.反应②中还原剂与氧化剂的物质的量之比为8:1
D.反应③中1mol还原剂被氧化则转移电子的物质的量为2mol
②用单线桥法标出反应②中电子转移的方向和数目_____。
2KMnO4+16HCl(浓) = 2KCl + 2MnCl2+ 5Cl2↑+8H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
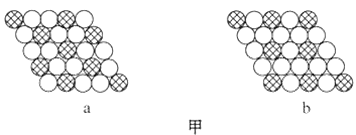
【题目】(1)如图甲所示为二维平面晶体示意图,所表示物质的化学式为AX3的是__________。
(2)图乙为一个金属铜的晶胞,请完成以下各题。
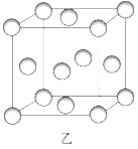
①该晶胞“实际”拥有的铜原子数是_________个。
②该晶胞称为_____________。(填序号)
A.六方晶胞
B.体心立方晶胞
C.面心立方晶胞
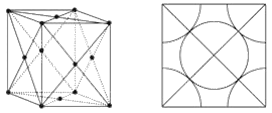
③我们在晶体结构中可以划出一块正立方体的结构单元,金属原子处于正立方体的八个顶点和六个侧面上,(图示如下图)这类金属晶体中原子的空间利用率是_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com