
����Ŀ��������������Ҫ�ɷ�ΪCu2S��Fe2O3�Ĺ�ҵ�������壨�����ɷֲ����뷴Ӧ���Ʊ��й����ʣ�ʵ��������ͼ��ʾ��
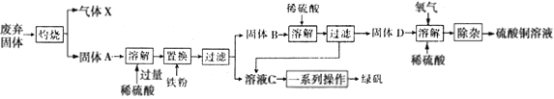
�ش��������⣺
��1������X�Ļ�ѧʽΪ____��
��2����������ʱ������Ӧ�����ӷ���ʽΪ��2H++Fe=Fe2++H2����____��
��3�������£�����D��O2��ϡ�����Ϻ�����Ӧ�����������̷����漴������Ӧ����֪FeSO4�Դ˷�Ӧ������ã���������з�Ӧ�����ӷ���ʽΪ4Fe2++O2+4H+=4Fe3++2H2O��_____��
��4������ʱ���ȼӺ��ʵ���������Fe2+����ΪFe3+���ټ��Լ�Y������ҺpH�Գ�ȥFe3+�������������Լ�Y������____�����ţ���
a��H2O2��CuO b��HNO3��Cu(OH)2 c��KMnO4��CuCl2 d��Ư�ۡ�CuCO3
��5����ˮ����ͭ���ȷֽ���������ͭ�����壬�����¶Ȳ�ͬ�������ΪSO3��SO2��O2�е�һ�֡����ֻ����֡����������ʵ��ⶨ������SO2��SO3��O2�����ʵ���������������ʵĻ�ѧ���������Ӷ�ȷ��CuSO4�ֽ�Ļ�ѧ����ʽ����֪ʵ�����ʱ������ͭ��ȫ�ֽ⣩��
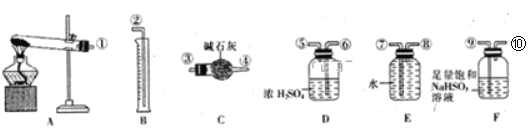
������C��������_____������F��������____��
����װ̽��ʵ���װ�ã����������ҵķ��������ӿ�����˳��Ϊ���١��������ޡ��ݡ�_____�� �� �� ���ڣ���ӿ���ţ���
����ijС���ȡ6.4g��ˮCuSO4,ʵ�������װ��C���ӵ�����Ϊ3.84g����Ͳ��ˮ���������ɱ�״�����������224mL����ͨ������ȷ��ʵ��������CuSO4�ֽ�Ļ�ѧ����ʽ��___��
���𰸡�SO2 Fe��Cu2+��Fe2����Cu��2Fe3����Fe��3Fe2�� 2Fe3����Cu��2Fe2����Cu2�� a ����� ����SO3ʹ֮ת��ΪH2SO4���ͷų�SO2 �ۢܢ�� 4CuSO4![]() 4CuO��2SO2����2SO3����O2��
4CuO��2SO2����2SO3����O2��
��������
��Ҫ�ɷ�ΪCu2S��Fe2O3�Ĺ�ҵ�����������յ�����ͭ���������������������壬����XΪSO2������AΪ����ͭ���������Ļ���A�м��������ܽ⣬�ټ�����������ۣ�������������Һ��ͭ�����˺�õ���ҺCΪFeSO4��Һ������BΪ����ͭ�Ļ�������B�м���ϡ���������������Һ��ͭ�����Թ���DΪCu������������Һ����Ũ�������½ᾧ�ɵ��̷����壬ͭ��������ϡ������Һ�з�Ӧ������ͭ��Һ���ݴ˷������
(1)��������������֪����XΪSO2���ʴ�Ϊ��SO2��
(2)��������ʱ�������ᡢ�����ӡ�ͭ���Ӷ�������Ӧ����Ӧ�����ӷ���ʽΪ2H++Fe=Fe2++H2����Fe+Cu2+=Cu+Fe2+��Fe+2Fe3+=3Fe2+���ʴ�Ϊ��Fe+Cu2+=Cu+Fe2+��Fe+2Fe3+=3Fe2+��
(3)�����£�FeSO4��ͭ��������ϡ����ķ�Ӧ����Ĺ��������������ȱ������������ӣ�4Fe2++O2+4H+=4Fe3++2H2O��������������ͭ����ͭ���ӣ���Ӧ�����ӷ���ʽΪCu+2Fe3+=2Fe2++Cu2+���ʴ�Ϊ��Cu+2Fe3+=2Fe2++Cu2+��
(4)����ʱ���ȼӺ��ʵ���������Fe2+����ΪFe3+���ټ��Լ�Y������ҺpH�Գ�ȥFe3+��Ϊ�˲������µ����ʣ����������������ΪH2O2������pHֵ���Լ�Y����ΪCuO��Cu(OH)2��CuCO3����ѡa��
(5)�ٸ���װ��ͼ��֪C�������Ǹ���ܣ�F��װ��������������Һ������������������ʹ֮ת��Ϊ���ᣬ�������������ʴ�Ϊ������ܣ�����SO3ʹ֮ת��ΪH2SO4���ͷų�SO2��
����ˮ����ͭ���ȷֽ���������ͭ�����壬�����¶Ȳ�ͬ�������ΪSO3��SO2��O2�е�һ�֡����ֻ����֡�Ҫ�ⶨ������SO2��SO3��O2�����ʵ�����ʵ��ʱ�����ݷ�Ӧװ�á�ϴ��װ�á�����װ�á��ռ�װ�ý�������A����ȡ����ķ���װ�á�B����ȡ���������������C�����ն�������D�Ǹ��������Ͷ�������E����ˮ���ռ�������F����������������Ҫ����ȡ���塢��ȥ�������������塢���ն��������ռ��������������������������������˳��Ϊ�١��������ޡ��ݡ��ۡ��ܡ�����ߡ��ڣ��ʴ�Ϊ���ۢܢ�ߣ�
��6.4g��ˮCuSO4�������ʵ���Ϊ![]() =0.04mol��װ��C���ӵ�����Ϊ3.84g�����������������Ϊ3.84g�����ʵ���Ϊ
=0.04mol��װ��C���ӵ�����Ϊ3.84g�����������������Ϊ3.84g�����ʵ���Ϊ![]() =0.06mol����Ͳ��ˮ���������ɱ�״�����������224mL�������������������ʵ���Ϊ
=0.06mol����Ͳ��ˮ���������ɱ�״�����������224mL�������������������ʵ���Ϊ![]() =0.01mol��ÿĦ����������ͨ��������������Һʱ����2mol���������跴Ӧ�в�����������Ϊxmol����Ӧ�в�����������Ϊymol������2x+y��0.06��x+y��0.04����ã�x=0.02��y=0.02������ͭԪ���غ����ɵ�����ͭ�����ʵ���ӦΪ0.04mol�����Է�Ӧ��CuSO4��CuO��SO3��SO2��O2�����ʵ���֮��Ϊ0.04��0.04��0.02��0.02��0.01=4��4��span>2��2��1�����Է�Ӧ�Ļ�ѧ����ʽΪ4CuSO4
=0.01mol��ÿĦ����������ͨ��������������Һʱ����2mol���������跴Ӧ�в�����������Ϊxmol����Ӧ�в�����������Ϊymol������2x+y��0.06��x+y��0.04����ã�x=0.02��y=0.02������ͭԪ���غ����ɵ�����ͭ�����ʵ���ӦΪ0.04mol�����Է�Ӧ��CuSO4��CuO��SO3��SO2��O2�����ʵ���֮��Ϊ0.04��0.04��0.02��0.02��0.01=4��4��span>2��2��1�����Է�Ӧ�Ļ�ѧ����ʽΪ4CuSO4![]() 4CuO+2SO3��+2SO2��+O2�����ʴ�Ϊ��4CuSO4
4CuO+2SO3��+2SO2��+O2�����ʴ�Ϊ��4CuSO4 ![]() 4CuO+2SO3��+2SO2��+O2����
4CuO+2SO3��+2SO2��+O2����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������A��K����ͼ��ת����ϵ������D��EΪ���嵥�ʣ�A��HΪ�����������Իش�(ͼ����Щ��Ӧ�IJ���ͷ�Ӧ������û��ȫ�����)��
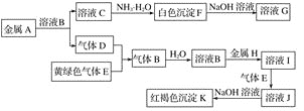
(1)д���������ʵĻ�ѧʽ��D��________�� I��______��
(2)д����C��F����Ӧ�����ӷ���ʽ��______________________________________��
(3)д����Ӧ��J��K�������ӷ���ʽ��____________________________________��
(4)����ҺI�е���NaOH��Һ���ɹ۲쵽��������______________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£���2L�ĺ����ܱ������У�X��Y��Z������������ʵ�����ʱ��仯��������ͼ��ʾ��
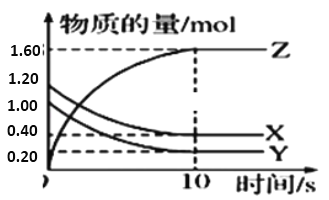
��1���÷�Ӧ�Ļ�ѧ����ʽΪ_____��
��2���ӷ�Ӧ��ʼ��10sʱ����Y��ʾ�ķ�Ӧ����Ϊ________��X��ת����Ϊ_____ ��
��3��10sʱ���÷�Ӧ ___ �ﵽ�˻�ѧƽ��״̬������ǡ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������̼����ȼ�ϵ����Li2CO3��K2CO3Ϊ����ʣ���C4H10Ϊȼ�ϣ��õ�ع���ԭ����ͼ������˵����ȷ���ǣ� ��
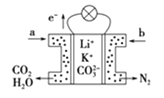
A.aΪC4H10��bΪCO2
B.�����ڵ�����У�CO32-�������ƶ�
C.�˵���ڳ���ʱҲ�ܹ���
D.ͨ�붡���һ���Ǹ������缫��ӦʽΪC4H10-26e-+13CO32-=17CO2��+5H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����AlCl3��MgCl2�Ļ����Һ�У���μ���NaOH��Һֱ�������������ϣ�����NaOH����������ó��������ʵ�����ʾ��ͼ���£�b��NaOH�����Ϊ1L���������ж���ȷ����
�� ��
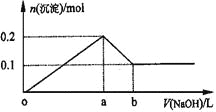
A.�����Һ��Al3�������ʵ���Ϊ0.2mol
B.NaOH��Ũ��Ϊ0.5 mol/L
C.��b�㴦��Һ�е�����ֻ��NaAlO2
D.ͼ���߶�oa:ab��5:1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ϩ��һ����Ҫ�Ļ���ԭ�ϣ����ɶ���������Ʊ����ش��������⣺
��1�������飨C4H10��������1-��ϩ��C4H8�����Ȼ�ѧ����ʽ���£�
��C4H10(g)= C4H8(g)+H2(g) ��H1
��֪����C4H10(g)+ ![]() O2(g)= C4H8(g)+H2O(g) ��H2=-119 kJ��mol-1
O2(g)= C4H8(g)+H2O(g) ��H2=-119 kJ��mol-1
��H2(g)+ ![]() O2(g)= H2O(g) ��H3=-242 kJ��mol-1
O2(g)= H2O(g) ��H3=-242 kJ��mol-1
��Ӧ�ٵĦ�H1Ϊ________ kJ��mol-1��ͼ��a���Ƿ�Ӧ��ƽ��ת�����뷴Ӧ�¶ȼ�ѹǿ�Ĺ�ϵͼ��x_____________0.1������ڡ���С�ڡ�������ʹ��ϩ��ƽ�������ߣ�Ӧ��ȡ�Ĵ�ʩ��__________�����ţ���
A�������¶� B�������¶� C������ѹǿ D������ѹǿ

��2������������Ļ��������һ������ͨ������д����ķ�Ӧ���������������ǻ���������������к��ж�ϩ�����顢�����ȡ�ͼ��b��Ϊ��ϩ�������������n��������/n�����飩�Ĺ�ϵ��ͼ�����߳��������ߺ͵ı仯���ƣ��併�͵�ԭ����___________��
��3��ͼ��c��Ϊ��Ӧ���ʺͷ�Ӧ�¶ȵĹ�ϵ���ߣ���������Ҫ�Ǹ����ѽ����ɵĶ�̼����������ϩ������590��֮ǰ���¶����߶������ԭ�������___________��____________��590��֮��ϩ���ʿ��ٽ��͵���Ҫԭ�������_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��NaOH��Ħ������Ϊ��__________ ��
��2��24.5��H2SO4�����ʵ���Ϊ��___________��
��3������£�8.96LCO2������Ϊ��___________��
��4����3.01��1023��Nԭ�ӵ�NH3�ڱ���µ����Ϊ:_____________ ��
��5��3g����п��������ϡ���ᷴӦ�����ɱ���µ��������Ϊ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������£����淴Ӧ��2NO(g)��O2(g)![]() 2NO2(g)������̶����ܱ������н��У��ﵽƽ��״̬�ı�־���ǣ� ��
2NO2(g)������̶����ܱ������н��У��ﵽƽ��״̬�ı�־���ǣ� ��
�ٵ�λʱ��������nmolO2��ͬʱ����2nmolNO2
�ڵ�λʱ��������nmolO2��ͬʱ����2nmolNO
����NO2��NO��O2��ʾ�ķ�Ӧ���ʵı�Ϊ2��2��1��״̬
�ܻ���������ɫ���ٸı��״̬
�ݻ��������ܶȲ��ٸı��״̬
��������ѹǿ���ٸı��״̬
��������ƽ����Է����������ٸı��״̬
A. �٢ܢޢ�B. �ڢۢݢ�C. �٢ۢܢ�D. ȫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I���� 5 g �����Ͻ�Ͷ�뵽 200 mL ��ˮ�У�������ȫ�ܽ⣬���� 4.48 L ��״���µ����壬��Һ��ֻ��һ�����ʡ����������ó������Ͻ������ֽ��������ʵ���֮��Ϊ_______��������Һ�����ʵ����ʵ���Ũ��Ϊ__________(������Һ����仯���Բ���)��
���� NaOH��AlCl3��MgCl2 ���ֹ�����ɵĻ������������ˮ�У��� 0.58 g ��ɫ���������������� ����Һ����μ��� 0.5 mol L-1 �����ᣬ�����������������ɳ�������������ͼ��ʾ��

����㣺
��1��������� MgCl2 ������__________g��
��2��P ���ʾ�����������_________ml��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com