
【题目】近代化学工业的基础是“三酸两碱”,早在我国古代就已经有人通过煅烧绿矾并将产生的气体溶于水中的方法制得硫酸,该法制备硫酸的过程中发生的主要反应如下:
反应Ⅰ:2FeSO4·7H2O=Fe2O3+SO2↑+SO3↑+14H2O↑;
反应Ⅱ:SO3+H2O=H2SO4。
下列说法正确的是
A.当生成标准状况下气体22.4L时,转移1mol电子
B.6.4gSO2中所含的质子数与6.4gSO3中所含的质子数相等
C.SO2、SO3的中心原子杂化类型不同
D.目前,工业上制硫酸的吸收阶段是采用浓硫酸吸收SO3
【答案】BD
【解析】
反应Ⅰ:2FeSO4·7H2O=Fe2O3+SO2↑+SO3↑+14H2O↑是氧化还原反应,Fe由+2价变为+3价,S由+6价变为+4价,生成的SO2和SO3的比例为1:1。
A.标准状况下的SO3为固态,当生成标准状况下气体22.4 L时,即SO2为1 mol,S由+6价变为+4价,转移2 mol电子,A错误;
B.6.4g SO2为0.1 mol,其中所含的质子数为(16+8×2)×0.1=3.2 mol;6.4g SO3为0.08 mol,其中所含的质子数为(16+8×3)×0.08=3.2 mol,前后两者相等,B正确;
C.SO2中S是sp2杂化,有一个电子对是孤对电子,所以分子构型是V型,SO3也是sp2杂化,但三个电子对全成键,其空间构型是平面三角形,SO2、SO3的中心原子杂化类型相同,空间构型不同,C错误;
D.吸收塔中SO3若用水吸收,发生反应:SO3+H2O![]() H2SO4,该反应为放热反应,放出的热量易导致酸雾形成,阻隔在三氧化硫和水之间,阻碍三氧化硫的被吸收;而浓硫酸的沸点高,难以气化,不会形成酸雾,同时三氧化硫易溶于浓硫酸,所以工业上从吸收塔顶部喷洒浓硫酸作吸收液,得到“发烟”硫酸,D正确;
H2SO4,该反应为放热反应,放出的热量易导致酸雾形成,阻隔在三氧化硫和水之间,阻碍三氧化硫的被吸收;而浓硫酸的沸点高,难以气化,不会形成酸雾,同时三氧化硫易溶于浓硫酸,所以工业上从吸收塔顶部喷洒浓硫酸作吸收液,得到“发烟”硫酸,D正确;
答案选BD。


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
【题目】甲醇既可用于基本有机原料,又可作为燃料用于替代矿物燃料。
(1)以下是工业上合成甲醇的反应:![]()
![]() 下表所列数据是该反应在不同温度下的化学平衡常数
下表所列数据是该反应在不同温度下的化学平衡常数![]() .
.
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
由表中数据判断反应I为 ______ 热反应(填“吸”或“放”) ![]() 某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应,达到平衡后,测得
某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应,达到平衡后,测得![]() ,则CO的转化率为 ______ ,此时的温度为 ______ 从表中选择.
,则CO的转化率为 ______ ,此时的温度为 ______ 从表中选择.
(2)已知在常温常压下:
①![]()
②![]()
③![]()
则反应![]() ______
______ ![]() 用
用![]() 、
、![]() 、
、![]() 表示
表示
(3)处理废水时,最后![]() 以
以![]() 形式除去,当
形式除去,当![]() 时,
时,![]() 沉淀完全,此时溶液的
沉淀完全,此时溶液的![]() ______ (已知,
______ (已知,![]() ,
,![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由两种常见金属组成的混合物A,在合适的条件下可按下图进行反应(部分产物和水省略),已知F为红褐色沉淀,请回答:

回答下列问题:
(1)混合物A的成分是_________(请填化学式)。
(2)反应①的离子方程式为:__________。
(3)反应②的化学方程式为:__________。
(4)写出E中加入过量NaOH的所有反应的离子方程式:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷烯(如图)是由磷原子六元环组成的蜂巢状褶皱二维晶体,它是白磷(![]() )的同素异形体。设NA为阿伏加德罗常数,下列说法正确的是
)的同素异形体。设NA为阿伏加德罗常数,下列说法正确的是

A.3.1g白磷中含P—P键的数目为0.3NA
B.6.2g磷烯中含六元环的数目为0.1NA
C.0.1molP4与0.6molH2在密闭容器中发生反应P4+6H2![]() 4PH3,生成PH3分子的数目为0.4NA
4PH3,生成PH3分子的数目为0.4NA
D.0.1molP4发生反应P4+5O2=2P2O5,转移的电子数为20NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示:
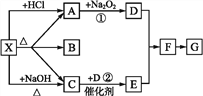
图中每一方格表示有关的一种反应物或生成物,其中A、C为无色气体,请填写下列空白:
(1)物质X可以是______,C是_________, F是______。
(2)反应①的化学方程式是_________,反应②的化学方程式是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于碱金属元素的说法正确的是( )
①原子结构的相同点是最外层电子数相同,都为1
②原子结构的不同点是随核电荷数的增加,电子层数增多,原子半径增大
③具有相似的化学性质,都是活泼金属
④都具有强还原性,在化合物中显![]() 价
价
⑤化学性质有差别,从Li到Cs,失电子能力逐渐增强
A.①③④B.①③⑤C.②④⑤D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】塑料、橡胶等材料的交联剂F的合成路线如图所示:

已知:
回答下列问题:
(1)芳香族化合物A中官能团的名称为________________。
(2)C→D的反应类型是_______________,E的结构简式为________________。
(3)F与NaOH反应的化学方程式为___________________________________。
(4)F的同分异构体中符合下列条件的有______________(不考虑立体异构)种。
a.属于![]() 的二取代物
的二取代物
b.取代基处于对位且完全相同
c.含酯基且能发生银镜反应
其中核磁共振氢谱有4组峰,峰面积之比为6:2:1:1的结构简式为__________________(写出一种)。
(5)参照题干中合成路线,设计以丙酮为主要原料制备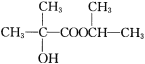 的合成路线(无机试剂任选)。________________________
的合成路线(无机试剂任选)。________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中①到⑩10种元素,填写下表空白:
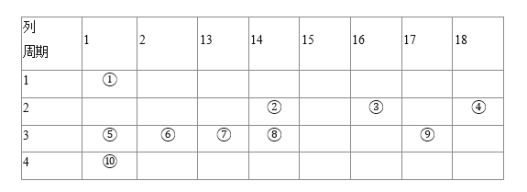
(1)在最高价氧化物对应的水化物中,酸性最强的化合物的化学式是______,碱性最强的化合物的化学式是______。![]() 均填化学式
均填化学式![]()
(2)最高价氧化物对应的水化物是两性的元素是______![]() 填元素符号
填元素符号![]() ,写出它的氢氧化物与⑤的氢氧化物反应的离子方程式______。
,写出它的氢氧化物与⑤的氢氧化物反应的离子方程式______。
(3)③⑤⑥三元素形成的简单离子具有相同的电子层结构,它们的离子半径由大到小顺序是![]() 用离子符号表示
用离子符号表示![]() ______。
______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下一些氧化物和单质之间可发生如下图所示的反应:其中,氧化物Ⅰ是红棕色固体,氧化物Ⅱ、Ⅲ、Ⅳ在反应条件下都是气体。
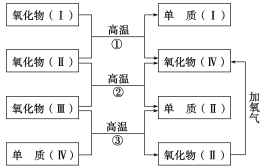
(1)氧化物Ⅰ的化学式是________,氧化物Ⅱ的化学式是________。
(2)反应①的化学方程式是_________;反应②的化学方程式_______;反应③的化学方程式是_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com