
| A、同温同压下,体积相同的氢气和氩气所含的原子数相等 |
| B、常温常压下,22.4 L 的C2H2气体和C2H4气体的混合物中含有的碳原子数目为0.2NA |
| C、2.4g金属镁与足量的盐酸反应,生成氢分子数目为2NA |
| D、1mol NH4+中含有电子数为10NA |


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
| A、K+、Mg2+、Cl-、NO3- |
| B、Ba2+、Ca2+、Cl-、CO32- |
| C、Na+、OH-、Mg2+、Cl- |
| D、Mg2+、Cu2+、CO32-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cl2是氧化剂,NaOH是还原剂 |
| B、被氧化的Cl原子和被还原的Cl原子的物质的量之比为1:5 |
| C、NaClO3既是氧化产物,又是还原产物 |
| D、每生成1mol的NaClO3,转移6mol的电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、6.02×1023 |
| B、1.806×1024 |
| C、1.204×1024 |
| D、2.408×1024 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、强电解质在溶液中完全电离,不存在电离平衡 |
| B、在溶液中,导电能力强的电解质是强电解质,导电能力弱的电解质是弱电解质 |
| C、强电解质都是离子化合物,弱电解质都是共价化合物 |
| D、纯净的强电解质在液态时,有的导电,有的不导电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、对“地沟油”进行分馏可得到汽油 |
| B、向煤中加入适量CaSO4,可大大减少燃烧产物中SO2的量 |
| C、误食可溶性重金属盐后,应采取的有效应急措施是喝大量的豆浆或牛奶 |
| D、PM2.5二氧化碳都属于空气质量日报的内容 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、元素非金属性Cl>S的实验依据是酸性HCl>H2S | ||
| B、二氧化碳分子中存在共价键和分子间作用力 | ||
C、SO
| ||
D、ClO
|
查看答案和解析>>
科目:高中化学 来源: 题型:
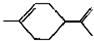 ,下列有关它的推测不正确的是( )
,下列有关它的推测不正确的是( )| A、分子式为C10H16 |
| B、常温下为液态,难溶于水 |
C、与过量的溴的CCl4溶液反应后产物为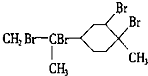 |
| D、它不能使酸性高锰酸钾溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com