
【题目】[2015·重庆]黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:
S(s)+2KNO3(s)+3C(s)![]() K2S(s)+N2(g)+3CO2(g) ΔH=x kJ·mol1
K2S(s)+N2(g)+3CO2(g) ΔH=x kJ·mol1
已知:碳的燃烧热ΔH1=a kJ·mol1
S(s)+2K(s)![]() K2S(s) ΔH2=b kJ·mol1
K2S(s) ΔH2=b kJ·mol1
2K(s)+N2(g)+3O2(g)![]() 2KNO3(s) ΔH3=c kJ·mol1
2KNO3(s) ΔH3=c kJ·mol1
则x为
A.3a+bc B.c3ab C.a+bc D.cab
【答案】A
【解析】本题考查盖斯定律的应用,意在考查考生的基本计算能力。
①C (s) +O2(g)![]() CO2(g) ΔH1=a kJ·mol1
CO2(g) ΔH1=a kJ·mol1
②S(s) +2K(s)![]() K2S(s) ΔH2=b kJ·mol1
K2S(s) ΔH2=b kJ·mol1
③2K(s)+ N2(g)+3O2(g)![]() 2KNO3(s) ΔH3=c kJ·mol1
2KNO3(s) ΔH3=c kJ·mol1
S(s) + 2KNO3(s)+ 3C(s)![]() K2S(s)+N2(g)+3CO2(g) ΔH=x kJ·mol1
K2S(s)+N2(g)+3CO2(g) ΔH=x kJ·mol1
根据盖斯定律:②③+ 3×①可得:S(s) + 2KNO3(s)+3C(s)![]() K2S(s)+N2(g)+3CO2(g) ΔH= (3a + b c) kJ·mol1,故x=3a+bc,选项A正确。
K2S(s)+N2(g)+3CO2(g) ΔH= (3a + b c) kJ·mol1,故x=3a+bc,选项A正确。
【名师点拨】当题目中出现多个热化学方程式,需求新的热化学方程式或ΔH时,一定要利用盖斯定律,其关键点是找出所求热化学方程式与已知热化学方程式的关系,如本题中需把已知热化学方程式中无关的O2、K消除即可。


 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源: 题型:
【题目】某原电池反应的离子方程式为Fe+2H+=Fe2++H2↑,则下列说法正确的是
A. 硝酸可能为电解质溶液
B. 锌可能为原电池正极
C. 铁的质量不变
D. 铜可能为原电池正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对化学反应速率和化学平衡的分析中,不正确的是
①在一密闭容器中充入1 mol H2和1 mol I2,达到平衡后,保持恒压,向其中再加入1 mol H2和1 mol I2,重新达到平衡时,反应速率增大
②已达平衡的反应N2(g)+3H2(g)![]() 2NH3(g) △H<0,升高温度,可以增大正反应速率,减小逆反应速率
2NH3(g) △H<0,升高温度,可以增大正反应速率,减小逆反应速率
③在2 L密闭容器中充入2 mol A气体和1 mol B气体,在一定条件下发生反应:2A(g)+B(g)![]() 2C(g),达到平衡时,C的浓度为0.6 mol/L,则A的转化率为30%
2C(g),达到平衡时,C的浓度为0.6 mol/L,则A的转化率为30%
④Mg、Al在相同条件下分别与0.1 mol/L盐酸反应,反应速率相同
A.①② B.①②③ C.②③④ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为实验室某浓硫酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:

(1)该浓硫酸的物质的量浓度为___________________。
(2)用此浓硫酸配制 240mL 1.0 mol·L-l 稀硫酸所需浓硫酸的体积是____________,量取浓硫酸所用的量筒的规格是_________(从下列量筒的规格中选用)
A.10mL B.20mL C.50mL D.100mL
(3)稀释浓硫酸的操作为_________________________________________________;
(4)容量瓶上标有以下五项中的______________;
A.温度 B.浓度 C.规格 D.压强 E.刻度线
(5)配制过程中,下列操作会引起结果偏高的是_______(填序号);
① 未洗涤烧杯、玻璃棒 ② 量取浓硫酸时仰视 ③ 定容时俯视刻度线
④ 容量瓶不干燥,含有少量蒸馏水 ⑤ 溶液未冷却至室温就转移到容量瓶
(6)100 mL 1.0 mol·L-l 稀硫酸与300 mL 1.0 mol·L-l BaCl2溶液混合,所得溶液中H+的物质的量浓度为_______________ (忽略混合时溶液体积的变化)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法中正确的是 ( )
A.有单质生成的反应一定是氧化还原反应
B.焰色反应是元素表现出来的化学性质
C.由两种元素组成,原子个数比为1:1的物质一定是纯净物
D.能与酸反应产物中有盐和水的氧化物不一定是碱性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列各组物质:(A) O2和O3; (B) ![]() ;
; 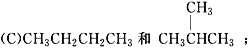
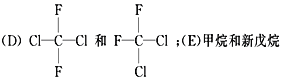
(1)__________组两物质互为同位素;(2)__________组两物质互为同素异形体;
(3)__________组两物质互为同系物;(4)__________组两物质互为同分异构体;
(5) _________组两物质互为同一物质。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g) ![]() 2C(g),各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下表和如图表示:
2C(g),各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下表和如图表示:
容器 | 甲 | 乙 | 丙 |
容积 | 0.5L | 0.5L | 1.0L |
温度/℃ | T1 | T2 | T2 |
反应物 起始量 | 1.5molA 0.5molB | 1.5molA 0.5molB | 6.0molA 2.0molB |
下列说法正确的是
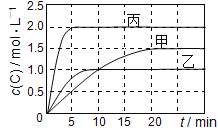
A.10 min内甲容器中反应的平均速率v(A)=0.025 mol/(Lmin)
B.由图可知:T1<T2,且该反应为吸热反应
C.x=1,若平衡时保持温度不变,改变容器体积平衡移动
D.T1℃,起始时甲容器中充入0.5molA、1.5molB,平衡时A的转化率为75%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NO2与N2O4 可相互转化: 2NO2( g)![]() N2O4(g) △H=24.2 kJ mol1,在恒温下, 将一定量和N2O4的混合气体充入体积为2 L的密闭容器中,其中物质的浓度随时间变化的关系如图所示。下列推理分析不合理的是
N2O4(g) △H=24.2 kJ mol1,在恒温下, 将一定量和N2O4的混合气体充入体积为2 L的密闭容器中,其中物质的浓度随时间变化的关系如图所示。下列推理分析不合理的是

A.前10 min内,用v(NO2)表示的反应速率为0. 02 molL1min1
B.反应进行到10 min时,体系吸收的热量为9.68 kJ
C.b、d两点中v(正)与v(逆)均相等
D.25 min时,正反应速率增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com