
【题目】某原电池反应的离子方程式为Fe+2H+=Fe2++H2↑,则下列说法正确的是
A. 硝酸可能为电解质溶液
B. 锌可能为原电池正极
C. 铁的质量不变
D. 铜可能为原电池正极
科目:高中化学 来源: 题型:
【题目】丙烯酸(CH2=CH—COOH)的性质可能有( )
①加成反应②取代反应③酯化反应④中和反应⑤氧化反应
A.①③B.①③④C.①③④⑤D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】230Th和232Th是钍的两种同位素,232Th可以转化成233U。下列有关Th的说法正确的是
A. Th 元素的质量数是232 B. Th 元素的相对原子质量是231
C. 232Th 转换成233U是化学变化 D. 230Th和232Th的化学性质相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】O2是人类赖以生存的物质,O2的摩尔质量为( )
A. 16 g·mol-1 B. 32 g·mol-1
C. 64 g·mol-1 D. 10 g·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是人类宝贵的自然资源。下图是某工厂对海水资源综合利用的部分流程示意图。


(1)请列举海水淡化的两种方法__________、__________。
(2)精制的食盐水通过离子交换膜电解槽电解。上图为离子交换膜法电解原理示意图。电解饱和食盐水的离子方程式为______________________,试根据电极反应分析透过交换膜的离子X是__________。
(3)已知[Ca(OH)2=5.5×l0-6,Mg(OH)2=1.8×l0-11]。将c(Mg2-)=3.6×l0-3mol/L 的 MgCl2溶液与 cmol/L的NaOH溶液等体积混合,要使混合液产生Mg(OH)2沉淀,c至少等于__________mol/L。经步骤③所得的Mg(OH)2沉淀中常混有Ca(OH)2,怎样除去?写出你的方案:_____________________________。
(4)工业制取镁首先用MgCO3进行热分解,笫二步加焦炭进行氯化得到MgCl2,最后通过电解MgCl2制取Mg,写出该法笫二步的化学方程式__________________________________________。电解熔融氯化镁所得的镁蒸气冷却后即为固体镁。下列气体中,镁蒸气可以在其氛围中冷却的是__________(选填编号字母)。
A.Cl2 B.N2 C.H2 D.空气
(5)甲同学认为:步骤③后可加热Mg(OH)2沉淀得到MgO,再电解熔融的MgO制金属镁,这样可简化实验步骤,体现实验的简约性原则。乙不同意甲的观点,他的理由是__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固定和利用CO2能有效地利用资源,并减少空气中的温室气体.CO2与化合物Ⅰ反应生成化合物Ⅱ,如反应所示(其他试剂、产物及反应条件均省略).
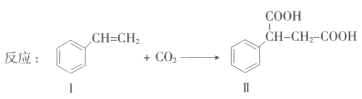
(1)化合物Ⅰ的官能团名称为___________,分子式为______,1 mol该物质完全燃烧需消耗_______mol O2 .
(2)写出化合物Ⅰ在一定条件下的加聚反应方程式___________。(不需要注明反应条件).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[2015·重庆]黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:
S(s)+2KNO3(s)+3C(s)![]() K2S(s)+N2(g)+3CO2(g) ΔH=x kJ·mol1
K2S(s)+N2(g)+3CO2(g) ΔH=x kJ·mol1
已知:碳的燃烧热ΔH1=a kJ·mol1
S(s)+2K(s)![]() K2S(s) ΔH2=b kJ·mol1
K2S(s) ΔH2=b kJ·mol1
2K(s)+N2(g)+3O2(g)![]() 2KNO3(s) ΔH3=c kJ·mol1
2KNO3(s) ΔH3=c kJ·mol1
则x为
A.3a+bc B.c3ab C.a+bc D.cab
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向容积为2 L的密闭容器中充入一定量的CO和NO2发生反应:4CO(g)+2NO2(g)![]() N2(g)+4CO2(g) ΔH<0。有关该反应的描述正确的是
N2(g)+4CO2(g) ΔH<0。有关该反应的描述正确的是

A.在一定温度、固定容积的密闭容器里,混合气体的密度不再改变可以说明上述可逆反应已达平衡
B.由图1可得加入适当的催化剂,E和ΔH 都减小
C.图2中0~10 min内该反应的平均速率v(CO)=0.03 mol·L1·min1,从11 min起其它条件不变,压缩容器的体积为1 L,则n(NO2)的变化曲线为d
D.图3中T1和T2表示温度,对应温度下的平衡常数为K1、K2,则:T1>T2,K1>K2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com