
【题目】对于温度、压强一定的气体,下列数值中与其物质的量无关的是
A. 质量 B. 体积 C. 分子数目 D. 气体摩尔体积
科目:高中化学 来源: 题型:
【题目】加热N2O5依次发生的分解反应为:
①N2O5(g)N2O3(g)+O2(g)
②N2O3(g)N2O(g)+O2(g)
在容积为2L的密闭容器中充入8mol N2O5 , 加热到t℃,达到平衡状态后O2为9mol,N2O3为3.4mol.则t℃时反应①的平衡常数为( )
A.10.7
B.8.5
C.9.6
D.10.2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某汽车安全气囊的产气药剂主要含有NaN3、Fe2O3、KClO4、NaHCO3等物质。当汽车发生碰撞时,产气药剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
(1)NaN3是气体发生剂,受热分解产生N2和Na,N2的电子式为____。
(2)Fe2O3是主氧化剂,与Na反应生成的还原产物为____(已知该反应为置换反应)。
(3)KClO4是助氧化剂,反应过程中与Na作用生成KCl和Na2O。KClO4含有化学键的类型为__________,K的原子结构示意图为________。
(4)NaHCO3是冷却剂,吸收产气过程中释放的热量而发生分解,其化学方程式为__________________。
(5)100 g上述产气药剂产生的气体通过碱石灰后得到N2 33.6 L(标准状况)。
①用碱石灰除去的物质为____;
②该产气药剂中NaN3的质量分数为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述不相符的是( )
A. 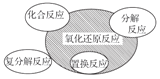 四种基本反应类型与氧化还原反应的关系
四种基本反应类型与氧化还原反应的关系
B.  AlCl3溶液中滴加NaOH溶液生成沉淀的情况
AlCl3溶液中滴加NaOH溶液生成沉淀的情况
C.  Ba(OH)2溶液中滴加硫酸溶液导电性的情况
Ba(OH)2溶液中滴加硫酸溶液导电性的情况
D.  等体积、等浓度稀硫酸分别与足量铁和镁反应的情况
等体积、等浓度稀硫酸分别与足量铁和镁反应的情况
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上从铝土矿(主要成分是Al2O3还含有SiO2、Fe203等杂质)中提取铝可采用如图工艺流程(反应条件已经省略):

请回答下列问题:
(1)图中I、Ⅱ、Ⅲ步骤中涉及分离溶液与沉淀的实验方法是___________(填操作名称)。
(2)Al2O3是两性氧化物,SiO2是酸性氧化物,Fe2O3是碱性氧化物,根据它们的性质,判断固体B的成分是__________(填化学式)。
(3)Fe2O3和盐酸反应的化学方程式为______________,沉淀C的化学式是__________。
(4)如果溶液D中通入“过量CO2”,改成通入“过量HCl”可以吗? 为什么? ____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关硅及其化合物的说法中不正确的是( )
A. 在粗硅的提取中发生反应2C+SiO2![]() 2CO+Si,硅元素被还原
2CO+Si,硅元素被还原
B. 太阳能电池可采用硅材料制作,其应用有利于环保、节能
C. 用SiO2制取硅酸,应先使二氧化硅与氢氧化钠溶液反应,然后再通入CO2
D. 由Na2CO3+SiO2![]() CO2+Na2SiO3可知硅酸的酸性强于碳酸
CO2+Na2SiO3可知硅酸的酸性强于碳酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一体积不变的密闭容器中充入2mol A、0.6mol C和一定量的B三种气体,一定条件下发生反应2A(g)+B(g)3c(g),各物质的浓度随时间变化的关系如图1所示,其中如t0~t1阶段c(B)未画出.图2为反应体系中反应速率随时间变化的情况,且t2、t3、t4各改变一种不同的条件. 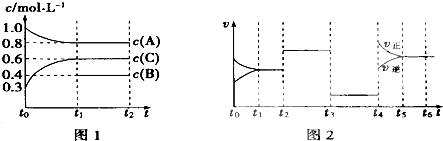
(1)若t1=15min,则t0~t1阶段以c的浓度变化表示的反应速率V(C)= .
(2)t3时改变的条件为 , B的起始物质的量为 .
(3)t4~t5阶段,若A的物质的量减少了O.01mol,而此阶段中反应体系吸收能量为a kJ,写出此条件下该反应的热化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨氮是造成水体富营养化的重要因素之一,用次氯酸钠水解生成的次氯酸将水中的氨氮(用NH3表示)转化为氮气除去,相关反应如下:
① NH3 +HClO===NH2Cl+H2O ② NH2Cl+HClO===NHCl2+H2O ③ 2NHCl2 +H2O===N2+HClO+3HCl
已知在水溶液中NH2Cl较稳定,NHCl2不稳定易转化为氮气。在其他条件一定的情况下,改变![]() (即NaClO溶液的投入量),溶液中次氯酸钠去除氨氮效果与余氯(溶液中+1价氯元素的含量)影响如右图所示。则下列说法正确的是
(即NaClO溶液的投入量),溶液中次氯酸钠去除氨氮效果与余氯(溶液中+1价氯元素的含量)影响如右图所示。则下列说法正确的是

A. 次氯酸与氨的总反应可表示为:2NH3+3HClO===N2+3H2O+3HCl
B. 反应中氨氮去除效果最佳的n(NaClO)/n(NH3)值约为1.5
C. a点之前溶液中发生的主要反应为:NH2Cl+HClO===NHCl2+H2O
D. 次氯酸钠溶液pH较小时有O2生成,促使氨氮去除率提高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,向10mL0.1mol LCaCl2溶液中滴加0.1mol L 的Na2CO3溶液,滴加过程中溶液中-lgc(Ca2+)与Na2CO3 溶液体积(V)的关系如图所示,下列有关说法正确的是

A. Z 点对应的分散系很稳定
B. w、x、y三点中,水的电离程度最大的为y点
C. 若用等浓度的Na2SO4 溶液代替Na2CO3 溶液,则图像在x点后的变化如虚线部分所示
D. Ksp(CaCO3])=5 x 10-10mol2/L2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com