
| A. | ①②③④⑤ | B. | ①④⑤ | C. | ③④⑤ | D. | ③⑤ |
分析 ①为检验RX是碘代烷,将RX与NaOH水溶液混合加热后,要先加入酸再加入AgNO3溶液,否则实验不成功;
②实验室里用无水乙醇和浓硫酸共热至170℃制乙烯;
③锌和稀硝酸反应生成NO而不是氢气;
④在制取新制氢氧化铜悬浊液时,应该NaOH过量,溶液呈碱性;
⑤为检验淀粉已水解,将淀粉与少量稀硫酸加热一段时间后,先加入碱溶液再加入银氨溶液,水浴加热,否则实验不成功.
解答 解:①为检验RX是碘代烷,将RX与NaOH水溶液混合加热后,要先加入HNO3,中和未反应的NaOH,然后再加入AgNO3溶液,否则实验不成功,故错误;
②实验室里用无水乙醇和浓硫酸共热至170℃制乙烯,140℃时乙醇发生取代反应生成乙醚,故错误;
③稀硝酸具有强氧化性,锌和稀硝酸反应生成NO而不是氢气,应该用稀硫酸或稀盐酸制取氢气,故错误;
④在制取新制氢氧化铜悬浊液时,应该NaOH过量,溶液呈碱性,应该是在试管中加入2mL10%的NaOH溶液,滴入2%的CuSO4溶液4~6滴,振荡后加入乙醛溶液0.5mL,加热至沸腾来检验醛基,故错误;
⑤为检验淀粉已水解,将淀粉与少量稀硫酸加热一段时间后,先加入NaOH溶液中和未反应的稀硫酸,再加入银氨溶液,水浴加热,银镜反应必须在碱性条件下,否则实验不成功,故错误;
故选A.
点评 本题考查化学实验方案评价,为高频考点,涉及物质制备温度的选取、物质性质、实验时溶液酸碱性控制等知识点,明确实验原理及物质性质是解本题关键,易错选项是①⑤,很多同学往往漏掉加入酸或碱而导致实验失败,题目难度中等.


 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:选择题
| A. | 保存氢氧化钠溶液,常用带橡胶塞的玻璃瓶 | |
| B. | 保存浓硝酸,常用带玻璃塞的棕色试剂瓶 | |
| C. | 保存金属铝时,常在试剂瓶中加入煤油进行封存 | |
| D. | 保存氢氟酸时,常用塑料瓶而不用玻璃瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀盐酸滴在铜片上:Cu+2H+═Cu2++H2↑ | |
| B. | 水玻璃中通入过量二氧化碳气体:SiO32-+CO2+H2O═H2SiO3+CO32- | |
| C. | 浓烧碱溶液中加入铝片:Al+OH-+H2O═AlO2-+H2↑ | |
| D. | NaHSO4与足量Ba(OH)2溶液混合:H++SO42-+Ba2++OH-═BaSO4↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 离子 | Mg2+ | Al3+ | Cl- | X |
| 物质的量浓度 | a | 2a | 2a | b |
| A. | Na+、6a | B. | SO42-、3a | C. | OH-、6a | D. | CO32-、4a |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
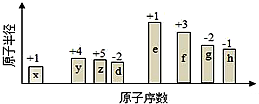 随原子序数的递增,八种短周期元素(用字母表示)原子半径的相对大小、最高正价或最低负价的变化如图所示.根据判断出的元素回答下列问题:
随原子序数的递增,八种短周期元素(用字母表示)原子半径的相对大小、最高正价或最低负价的变化如图所示.根据判断出的元素回答下列问题: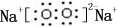 ;B是常见的液态化合物,其稀溶液易被催化分解,可使用的催化剂为AB.(填序号)
;B是常见的液态化合物,其稀溶液易被催化分解,可使用的催化剂为AB.(填序号)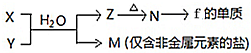
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com