
| A、2 | B、3 | C、0.001 | D、11 |
| 10-14 |
| 10-3 |


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
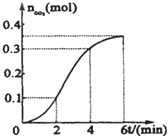
| A、反应开始2分钟内平均反应速率最大 |
| B、反应4分钟后平均反应速率最小 |
| C、反应开始4分钟内温度对反应速率的影响比浓度大 |
| D、反应在第2min到第4min间生成CO2的平均反应速率最大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4+、Al3+、Br-、SO42- |
| B、Na+、Mg2+、Cl-、NO3- |
| C、K+、Ba2+、ClO-、NO3- |
| D、K+、Na+、I-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、配合物中必定存在配位键 |
| B、配合物中只有配位键 |
| C、[Cu(H2O)6]2+中的Cu2+提供空轨道,H2O中的氧原子提供孤电子对形成配位键 |
| D、配合物在半导体等尖端技术、医学科学、催化反应和材料化学等领域都有着广泛的应用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、除③外 | B、①②⑤⑥ |
| C、除③⑧外 | D、除③④⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、⑤ | B、①②⑥ |
| C、②⑤⑥⑦ | D、①③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
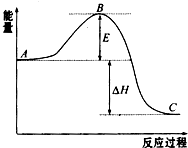 2SO2(g)+O2 (g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ?mol-1
2SO2(g)+O2 (g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ?mol-1查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2 mol?L-1NaOH溶液 |
| B、2 mol?L-1NaCl溶液 |
| C、2 mol?L-1NaHSO4溶液 |
| D、乙醇溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com