
【题目】I.(1)图I表示10mL量筒中液面的位置,A与B,B与C刻度间相差1mL,如果刻度A为4,则量筒中液体的体积是①,由于放置位置不当读数时俯视,读出的数值为②则①②的正确数值为___________

A①3.2mL、②小于3.2mL B.①4.8mL、②大于4.8mL
C.①3.2mL、②大于3.2mL D.①4.8mL、②小于4.8mL
(2)实验室需配制1mol·L-1的NaOH溶液200mL,在用托盘天平称取NaOH固体时,天平读数为________填代号,下同)。
A.大于8.0g B.小于8.0g C.8.0g
II.表示溶液浓度的方法通常有两种;溶液中溶质的质量分数(W)和物质的量浓度 (c),因此在配制溶液时,根据不同的需要,有不同的配制方法。请完成下列填空题。
(1)用10%(密度为1.01g/cm3)的氢氧化钠溶液配制成27.5g 2%的氢氧化钠溶液。
①计算:需_________g 10%(密度为1.01g/cm3)的氢氧化钠溶液
②量取:用_________mL量筒量取10%的氢氧化钠溶液
(2)把98%(密度为1.84g/cm3)的浓硫酸稀释成2mol/L的稀硫酸100mL,回答下列问题:
①需要量取浓硫酸_______ mL
②下列实验操作使配制的溶液浓度偏的是__________
A.容量瓶洗涤后未干燥
B.量取溶液时,仰视刻度线
C.装入试剂瓶时,有少量溶液溅出
D.没有洗涤烧杯和玻璃棒
E.定容时,加水不慎超出刻度线,又倒出一些
【答案】CA5.51010.9B
【解析】
I.(1)量筒的刻度线自上而下是递减的,所以如果刻度A为4,则B的读数就是3.2mL,因此量筒中液体的体积①是3.2mL;由于放置位置不当读数时俯视,则读数偏大,②大于3.2mL,答案选C;
(2)200mL 1molL-1 NaOH溶液中含有溶质氢氧化钠的物质的量为:1mol/L×0.2L=0.2mol,需要氢氧化钠的质量为:40g/mol×0.2mol=8.0g;但用托盘天平称量氢氧化钠时必须放在小烧杯中或玻璃片上称量,故质量应该大于8.0g,答案选A;
II. (1)①由ω1m1=ω2m2得m2=![]() =
=![]() =5.5g;
=5.5g;
②量取液体应一次量取,选用量程最小的量筒,故用10mL量筒量取5.5mL 10%的NaOH溶液;
(2)①硫酸的物质的量2mol/L×0.1L=0.2mol,硫酸的质量0.2mol×98g/mol=19.6g,需浓硫酸的质量![]() =20g 需要量取浓硫酸
=20g 需要量取浓硫酸![]() =10.9mL;
=10.9mL;
②A、容量瓶洗涤后未干燥,不影响溶液配制,对浓度无影响,选项A不选;B、量取溶液时,仰视刻度线,所取浓硫酸的量偏多,配得溶液浓度偏高,选项B选;C.装入试剂瓶时,有少量溶液溅出,溶质的量减少,所配得溶液浓度偏低,选项C不选;D.没有洗涤烧杯和玻璃棒,溶质的量减少,所配溶液的浓度偏低,选项D不选;E.定容时,加水不慎超出刻度线,又倒出一些,则水加多了,所配溶液浓度偏低,选项E不选;答案选B。


科目:高中化学 来源: 题型:
【题目】用质量分数为36.5%的浓盐酸(密度为1.16 g·cm-3)配制成1 mol·L-1的稀盐酸。现实验室仅需要这种盐酸220 mL,试回答下列问题:
(1)配制稀盐酸时,应选用容量为________mL的容量瓶。
(2)经计算需要________mL浓盐酸,在量取时宜选用下列量筒中的________。
A.5 mL B.10 mL C.25 mL D.50 mL
(3)在量取浓盐酸后,进行了下列操作:
①等稀释的盐酸的温度与室温一致后,沿玻璃棒注入250 mL容量瓶中。
②往容量瓶中小心加蒸馏水至液面离容量瓶刻度线1~2 cm时,改用胶头滴管加蒸馏水,使溶液的液面与瓶颈的刻度标线相切。
③在盛盐酸的烧杯中注入蒸馏水,并用玻璃棒搅动,使其混合均匀。
④用蒸馏水洗涤烧杯和玻璃棒2至3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是(填序号)____________。
(4)在上述配制过程中,用刚刚洗涤洁净的量筒来量取浓盐酸,其配制的稀盐酸浓度是________(填“偏高”、“偏低”或“无影响”)。若未用蒸馏水洗涤烧杯内壁或未将洗涤液注入容量瓶,则配制的稀盐酸浓度是________(填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中,所选装置或实验设计合理的是

A. 图⑤所示装置中盛有饱和NaOH溶液用以除去CO2中含有的少量HCl气体
B. 用乙醇提取碘水中的碘选择图③所示装置
C. 用图①和②所示装置进行粗盐提纯
D. 用图④所示装置可把由5种沸点相差较大的液体组成的混合物中的成分一一分离出来
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某药物中间体F的合成流程如下:
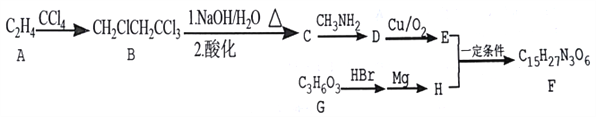
已知:(1) ![]() ;
;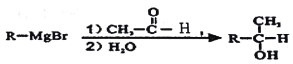
(2)碳碳双键与羟基相连不稳定
请回答:
(1)A→B的反应类型为_____________。
(2)有关物质D的叙述错误的是______(填序号)。
A.能使KMnO4溶液褪色 B.能缩聚成高分子
C.能与甲醇发生酯化反应 D.能发生水解反应
(3)B→C过程中反应1的化学方程式为____________。
(4)F的结构简式为_____________。
(5)写出满足下述条件的E的同分异构体____________。
①水解产物能消耗2molNaOH;②分子中有三种不同类型的氢;③只含一个甲基
(6)结合题给信息,以乙烯为原料制备2-丁醇,设计合成路线(其他试剂任选) ____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L容积不变的容器中,发生N2+3H22NH3的反应.现通入4molH2和4molN2,10s内用H2表示的反应速率为0.12mol/(Ls),则10s后容器中N2的物质的量是
A.3.6molB.3.2molC.2.8molD.1.6mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有镁铝铜合金5.2g,加入过量的盐酸中,在标准状况下放出氢气5.6L,反应后过滤得沉淀0.1g。若将此合金放入过量的烧碱溶液中,反应后,在标准状况下大约能产生多少升氢气?镁铝铜的质量各为多少克? (写计算过程)___________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的铁粉加入100mL稀硫酸中,为中和过量硫酸,且使Fe2+完全转化为Fe(OH)2,共消耗掉2mol·L-1NaOH溶液150mL。原硫酸溶液的浓度是
A. 0.5mol·L-1 B. 1mol·L-1 C. 1.5mol·L-1 D. 2mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示与对应叙述不相符的是( )

A. 图甲表示一定温度下FeS和CuS的沉淀溶解平衡曲线,则Ksp(FeS) >Ksp(CuS)
B. 图乙表示pH=2的甲酸与乙酸溶液稀释时的pH变化曲线,则酸性:甲酸>乙酸
C. 图丙用0.1000 mol·L-lNaOH溶液滴定25.00 mL盐酸的滴定曲线,则 c(HCl)=0.0800 mol ·L-1
D. 图丁表示反应N2(g)+3H2(g) ![]() 2NH3(g)平衡时NH3体积分数随起始n(N2)/n(H2)变化的曲线,则转化率:αA(H2)=αB(H2)
2NH3(g)平衡时NH3体积分数随起始n(N2)/n(H2)变化的曲线,则转化率:αA(H2)=αB(H2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 32.2g Na2SO4·10H2O 溶于67.8g水中,w(Na2SO4)=32.2%
B. 标准状况下,22.4LHCl溶于1L水中,盐酸的物质的量浓度为1 mol/L
C. 将1 mol/L的NaCl溶液与0.5mol/L的BaCl2溶液等体积混合后,不考虑体积变化,c(Cl-)=1 mol/L
D. 同浓度的三种溶液: Na2SO4、MgSO4、Al2(SO4)3,其体积比为3:2:1,则SO42-浓度之比为3:2:3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com