
(Ⅰ)溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物。
(1)写出溴乙烷在NaOH水溶液中的反应方程式:
反应类型 。某同学取少量溴乙烷与NaOH水溶液反应后的混合溶液,向其中滴加AgNO3溶液,加热,产生少量沉淀。该同学由此得出溴乙烷与NaOH水溶液反应,生成了溴化钠,你认为是否合理,原因: 。
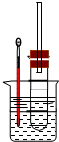
(2)写出溴乙烷在NaOH乙醇溶液中的反应方程式 反应类型 。反应中生成的气体可以用下图所示装置检验,现象是 ,水的作用是 。除高锰酸钾酸性溶液外,还可以用 检验生成的气体,此时还有必要将气体先通入水中吗? (填“有”或“没有”) 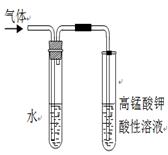
(Ⅱ)下面是实验室制乙烯并检验其性质的装置图,请回答: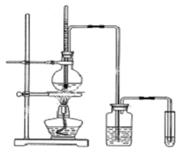
(1)写出圆底烧瓶中反应的方程式 ,
反应类型_______________;
(2)烧瓶中混合液逐渐变黑,并产生某些无机杂质气体,写出产生杂质气体的化学方程式:
;
(3)为了检验乙烯的生成,试管中应盛放 ,
现象为 ;
(4)洗瓶中盛放的试剂为 ,作用________________________________。
(Ⅲ)某学习小组同学为了确定盐酸 、苯酚、碳酸的酸性强弱,设计了如图所示的装置图进行实验: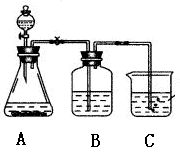
(1)锥形瓶内装某可溶性盐,写出A中反应的离子方程式:
;
(2)C中的现象为 ,写出C中反应的化学方程式:_____________;
(3)B中的试剂为 ,作用 。
(Ⅰ)
(1)CH3CH2Br+NaOH→CH3CH2OH+NaBr 取代(或水解) 不合理 没有用硝酸中和氢氧化钠溶液
(2)CH3CH2Br+NaOH—→CH2=CH2↑+NaBr+H2O 消去反应 溶液褪色 吸收乙醇 溴的四氯化碳溶液 没有
(Ⅱ)
(1)CH3CH2OH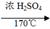 CH2=CH2↑ +H2O 消去反应
CH2=CH2↑ +H2O 消去反应
(2) C + 2H2SO4(浓)  CO2↑ + 2SO2↑+ 2H2O
CO2↑ + 2SO2↑+ 2H2O
(3)高锰酸钾溶液(或溴的四氯化碳溶液) 溶液褪色
(4)氢氧化钠溶液 吸收SO2 CO2
(Ⅲ) (1)CO32-+ 2H+=H2O+ CO2↑
(2) 白色浑浊 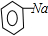 +CO2+H2O→
+CO2+H2O→ +NaHCO3
+NaHCO3
(3)饱和碳酸氢钠溶液 吸收CO2中的HCl
解析试题分析:(Ⅰ)(1)溴乙烷与NaOH水溶液发生水解反应(取代反应),反应方程式为CH3CH2Br+NaOH→CH3CH2OH+NaBr。由于AgNO3与NaOH溶液反应也生成沉淀,故不合理。
(2)溴乙烷与NaOH乙醇溶液发生消去反应,方程式为:CH3CH2Br+NaOH—→CH2=CH2↑+NaBr+H2O。高锰酸钾溶液能氧化乙烯气体而褪色。由于挥发出的乙醇也可被高锰酸钾溶液氧化,使高锰酸钾溶液褪色,应先除去,水的作用就是吸收乙醇。还可以用Br2与乙烯发生反应褪色来验证,其中不用先通入水中。
(Ⅲ)(2)二氧化碳、水和苯酚钠反应生成苯酚和碳酸氢钠,反应方程式为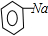 +CO2+H2O→
+CO2+H2O→ +NaHCO3。
+NaHCO3。
考点:有机实验
点评:本题是有关实验方案的设计和评价的考查,要求学生熟悉所实验的内容及原理,能够考查同学们进行分析问题、解决问题的能力。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
 溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究.
溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究.查看答案和解析>>
科目:高中化学 来源: 题型:
 溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究.
溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究.查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 醇 |
| 加热 |
| 醇 |
| 加热 |
| 浓H2SO4 |
| 170℃ |
| 浓H2SO4 |
| 170℃ |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
 溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究.
溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究.
| ||
| △ |
| ||
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究.
溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com