
目前电解法制烧碱通常采用离子交换膜法,阳(阴)离子交换膜不允许阴(阳)
离子通过。则以下叙述错误的是( )
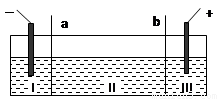
A、NaOH、H2均在Ⅰ区产生
B、 图中a为阴离子交换膜
C、Ⅲ区炭棒上的电极反应式为2Cl--2e →Cl2↑
D、电解时往Ⅲ区的溶液中滴加甲基橙,溶液先变红后褪色
科目:高中化学 来源: 题型:阅读理解

| ||
| ||
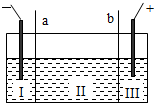 则以下叙述正确的是
则以下叙述正确的是查看答案和解析>>
科目:高中化学 来源:闵行区模拟 题型:问答题
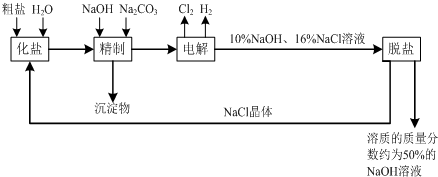
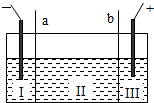
查看答案和解析>>
科目:高中化学 来源:2008年上海市闵行区高考化学模拟试卷(解析版) 题型:填空题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com