
����Ŀ��ij���dz��Ը���Ϊԭ�����ǣ�ͬʱ�õ������ĸ��������Ը�������ۺ����ã�����������߾���Ч�棬���һ��ܷ�ֹ������Ⱦ���ְ����·�ʽ���У�

��֪F��H���Ǿ�����ζ��Һ�壬FΪE�����ۺ�������������Ԫ��״�Գƽṹ������գ�
��1��A������________��D��ͬ���칹��Ľṹ��ʽΪ________________��
��2��E��G�Ļ�ѧ����ʽ_________________________��
��3��G��H�Ļ�ѧ����ʽ_________________________��
��4��F�Ľṹ��ʽ��_____________________��
���𰸡� ��ά�� CH3��O��CH3 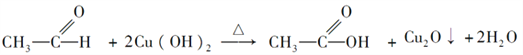 CH3CH2OH+CH3COOH
CH3CH2OH+CH3COOH![]() CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O 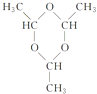
��������������A�ķ���ʽ��C6H10O5��n��֪A���ǵ��۾�����ά�أ���ϵ����ʵ��ȷ��AΪ��ά�أ�BΪ�����ǣ�DΪ�ƾ���EΪ��ȩ��FΪE��������Ҿ����������Ԫ��״�Գƽṹ���������ݳɼ�ԭ��ֻ����C=O��ʽ�ӳ����ɡ���ͼ��ʾ��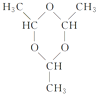 ����1��A��������ά�أ�DΪ�ƾ�����ͬ���칹��Ľṹ��ʽΪCH3��O��CH3����2��E��G����ȩ�����������ᣬ��Ӧ�Ļ�ѧ����ʽΪ��
����1��A��������ά�أ�DΪ�ƾ�����ͬ���칹��Ľṹ��ʽΪCH3��O��CH3����2��E��G����ȩ�����������ᣬ��Ӧ�Ļ�ѧ����ʽΪ��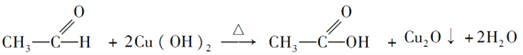 ��
��
��3��G��H������Ҵ���Ũ����Ĵ��·�Ӧ��������������ˮ����Ӧ�Ļ�ѧ����ʽΪ��CH3CH2OH+CH3COOH![]() CH3COOCH2CH3+H2O����4��F�Ľṹ��ʽΪ��
CH3COOCH2CH3+H2O����4��F�Ľṹ��ʽΪ�� ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й����ʱȽ���ȷ���ǣ� ��
A. Al3+��Na+��O2-���뾶��������
B. N��O��F���������������
C. F2��Cl2��Br2��I2���ʵ��۵�����
D. ﮡ��ơ��ء�卑�����ˮ��Ӧ�û�������Խ��Խ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Σ�ջ�ѧҩƷҪ�ڰ�װ��ǩ��ӡ�Ͼ�ʾ�Ա�־�����л�ѧҩƷ�����뾯ʾ��־���ƶ�Ӧ��ȷ����(����)
A. �ƾ������綾Ʒ B. Ũ���ᡪ����ʴƷ
C. ���͡�����ըƷ D. �ռ���綾Ʒ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Һ�����÷�Һ©���ܷ�������ֵ��ǣ� ��
A.�Ҵ�������
B.��ȩ��ˮ
C.�ױ���ˮ
D.�����屽
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����ζ��A����������ǵ�200������������ֵ�͡��ڸкá�������С������90������ҹ㷺ʹ�á�A�Ľṹ��ʽΪ��

��֪������һ�������£��������������뺬��NH2�Ļ����ﷴӦ���������������磺
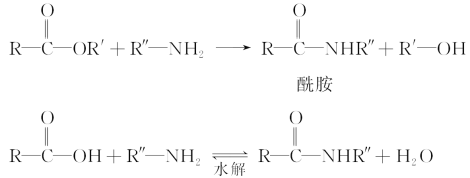
��������������ˮ�⡣����д���пհף�
(1)��ϡ�������¼��ȣ�������A�������ɵ�ˮ�������________��________��
(2)�ڽ�Ũ��ͳ�ʱ����������£�������A����ˮ������________��________��________��
(3)������A�����ڵĹ�����֮��Ҳ���Է�����Ӧ��������һ���������������Ǽ״���________________��(��д�ṹ��ʽ���÷����г��������⣬������һ����ԭ����ɵĻ�)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ڼ�չ��տɴ����ȷ��������������ø�����Al��Al2O3��Cr2O3�ȣ��н�����������ʵ�ָ��������������á��乤���������£�

��1�����ȷ�ұ�����������������˽�������____��������������������ԭ��������
��2����Һ1�е���������CrO42-��_______��
��3�����̢���Cr2O3����ķ�Ӧ�У�������0.4 mol CrO42-��������������O2�������ʵ�����____��
��4��ͨ��CO2������ҺpHʵ�����ʵķ��롣
������A���յõ�Al2O3�����õ�ⷨұ��Al��ұ��Al�Ļ�ѧ����ʽ��_______��
������B���ȷֽ��������ʿ���ѭ�����ã�B��_______��
����֪��2 CrO42-�� 2H+ ![]() Cr2O72-�� H2O K �� 4.0��1014
Cr2O72-�� H2O K �� 4.0��1014
��Һ3��Cr2O72-��Ũ����0.04 mol/L����CrO42-��Ũ����_______ mol/L��
��5�����̢��Ŀ���ǵõ�K2Cr2O7��Ʒ����Ʒ���ؽᾧ���Ƶô�����K2Cr2O7��
��ͬ�¶��»�������ܽ��(g/100gH2O)
���������� | 0��C | 20��C | 40��C | 60��C | 80��C |
NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
KCl | 28.0 | 34.2 | 40.1 | 45.8 | 51.3 |
K2SO4 | 7.4 | 11.1 | 14.8 | 18.2 | 21.4 |
K2Cr2O7 | 12.3 | 26.3 | 45.6 | 73.0 | |
Na2Cr2O7 | 163 | 183 | 215 | 269 | 376 |
��ϱ������ݷ��������̢�õ�K2Cr2O7��Ʒ�IJ����ǣ�����Һ���м���ϡ�����KCl���壬Ȼ��_______________�����˵õ�K2Cr2O7��Ʒ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ˮԡ���ȵ�ʵ���ǣ� ��
A.����������ӦB.��ȩ��������Ӧ
C.ʵ��������������D.ʵ���������ᶡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���1 mol��CuSO4��5H2O(s)����ˮ��ʹ��Һ�¶Ƚ��ͣ���ЧӦΪ��H1����1 mol��CuSO4(s)����ˮ��ʹ��Һ�¶����ߣ���ЧӦΪ��H2��CuSO4(s)��5H2O(s)���ȷֽ�Ļ�ѧ����ʽΪCuSO4��5H2O(s)![]() CuSO4(s)��5H2O(l)����ЧӦΪ��H3���������ж���ȷ����(����)
CuSO4(s)��5H2O(l)����ЧӦΪ��H3���������ж���ȷ����(����)
A. ��H2����H3 B. ��H1����H3 C. ��H1����H3����H2 D. ��H1����H2����H3
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com