
【题目】在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g) ![]() 2NO2(g),随温度升高,混合气体的颜色变深。
2NO2(g),随温度升高,混合气体的颜色变深。
(1)反应的ΔH________0(填“大于”或“小于”);100 ℃时,体系中各物质浓度随时间变化如图所示。在0~60 s时段,反应速率v(N2O4)为________mol·L-1·s-1;反应的平衡常数K1为_____________。

(2)100 ℃时达到平衡后,改变反应温度为T,c(N2O4)以0.0020 mol·L-1·s-1的平均速率降低,经10 s又达到平衡。T______100 ℃(填“大于”或“小于”),判断理由是____________________________________________。
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向________(填“正反应”或“逆反应”)方向移动,判断理由是____________________________________。
【答案】 大于 0.0010 0.36 mol·L-1 大于 反应正方向吸热,反应向吸热方向进行,故温度升高 逆反应 对气体分子数增大的反应,增大压强平衡向逆反应方向移动
【解析】(1)温度升高,混合气体的颜色变深,说明平衡向正反应方向进行,因此正反应是吸热反应,则反应的ΔH大于0;在0~60 s时段内消耗四氧化二氮的物质的量浓度为0.1mol/L-0.040mol/L=0.06mol/L,因此反应速率v(N2O4)=0.06mol/L÷60s=0.0010mol·L-1·s-1;平衡时N2O4、NO2的浓度分别是0.04mol/L、0.12mol/L,则反应的平衡常数K1为![]() 。(2)c(N2O4)以0.0020 mol·L-1·s-1的平均速率降低,说明平衡向正反应方向进行,由于正反应吸热,所以改变的条件是升高温度,即T大于100 ℃;(3)由于正反应体积增大,所以对气体分子数增大的反应,增大压强平衡向逆反应方向移动。
。(2)c(N2O4)以0.0020 mol·L-1·s-1的平均速率降低,说明平衡向正反应方向进行,由于正反应吸热,所以改变的条件是升高温度,即T大于100 ℃;(3)由于正反应体积增大,所以对气体分子数增大的反应,增大压强平衡向逆反应方向移动。


科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列叙述正确的是
A. 标准状况下,33.6L氦气所含的原子数目是3NA
B. 2.2gKHCO3与Mg3N2的混合物中含有的质子数目为1.1NA
C. 0.3molNaHSO4固体在熔融状态下所含的SO42-数目为0.3NA
D. 25℃时,1LpH=12的Na2CO3溶液中含有Na+的数目为0.02NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示3套实验装置,分别回答下列问题。
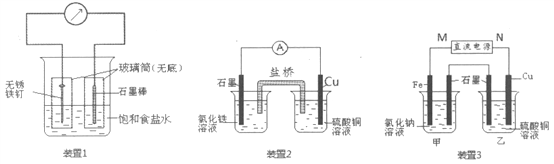
(1)装置1为铁的吸氧腐蚀实验,一段时间后,玻璃筒内的石墨电极上的电极反应式为_________。
(2)装置2中的石墨是_______极,该电极反应式为___________。
(3)装置3中甲烧杯盛放100mL0.2mol/L的NaCl溶液,乙烧杯盛放100mL0.5mol/L的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞,观察到石墨电极附近首先变红。
①电源的M端为________极;甲烧杯中铁电极的电极反应为_________________。
②乙烧杯中电解的总方程式为_______________。
③停止电解,取出Cu电极,洗涤、干燥、称量、电极增重0.64 g,甲烧杯中产生的气体标准状况下体积为________mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cu在稀硝酸中可以发生如下反应:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O 下列叙述正确的是()
A. HNO3在反应中失去电子
B. 氧化产物与还原产物的物质的量比为3:2
C. 发生氧化反应的硝酸占参加反应硝酸的1/4
D. 每1 mol HNO3参加反应,有3 mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等温等压下,关于等质量D2、T2两种气体的下列叙述中不正确的是()
A. 密度之比2:3 B. 质子数之比3:2 C. 中子数之比3:4 D. 体积之比2:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示物质变化的化学用语正确的是
A. NH3·H2O的电离方程式:NH3·H2O==NH4++OH-
B. 铁发生吸氧腐蚀的正极反应方程式:O2+2H2O+4e-==4OH-
C. 碳酸钠水解的离子方程式:CO32-+2H2O![]() 2OH-+H2CO3
2OH-+H2CO3
D. CO燃烧热的热化学方程式:2CO(g)+O2(g)=2CO2(g) △H =-566.0kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组元素性质或原子结构递变情况错误的是()
A.Li、Be、B原子最外层电子数依次增多
B.P、S、Cl元素最高正化合价依次升高
C.N、O、F原子半径依次增大
D.Li、Na、K的电子层数依次增多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是实验室制备氯气并进行一系列相关实验的装置。

(1)装置B作用之一是为了除去氯气中的杂质HCl,盛装的液体试剂为__________;
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ处依次放入的物质正确的是__________ (填字母编号) ;
编号 | Ⅰ | Ⅱ | Ⅲ |
a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
b | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(3)D中发生反应的化学方程式是_________________________________。将装置D中的溶液加入装置E中,溶液分为两层,上层呈紫红色,要分离出紫红色溶液,需使用的玻璃仪器是玻璃棒、烧杯和_____________;
(4)装置F中反应的化学方程式为_____________;
(5)如果本实验使用的浓盐酸质量分数为36.5%、密度为1.15 g/cm3,此盐酸的物质的量浓度为_____mol·L-1,若用250 mL水配制,则应溶解标况下HCl气体约为_____________L(结果保留3位有效数字)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com