
【题目】在AlCl3和FeCl3混合溶液中,先加入过量的KI溶液,再加入足量的Na2S溶液,所得到的沉淀物是( )
A.Fe(OH)3、Al(OH)3
B.Al(OH)3、I2
C.Fe2S3、I2
D.FeS、S、Al(OH)3
【答案】D
【解析】
试题分析:在FeCl3和AlCl3溶液中加过量KI,先是FeCl3与KI两盐发生氧化还原反应:2Fe3++2I-=2Fe2++I2,反应完后溶液中含大量Fe2+、Al3+、I2,再加入Na2S后,由于S2-+H2O![]() HS-+OH-.在Na2S溶液中,有大量S2-、OH-,依题意知,Fe2+结合S2-能力强,两盐发生复分解反应,形成FeS沉淀,Fe2++S2-=FeS↓;Al3+结合OH-能力强,形成Al(OH)3沉淀,Al3++3OH-=Al(OH)3↓,或理解为Al3+与S2-发生双水解反应:3Na2S+AlCl3+6H2O=2Al(OH)3↓+3H2S↑+6NaCl;但由于I2的存在发生:I2+S2-=S↓+2I-或I2+H2S=S↓+2HI,所以最终得到的沉淀是FeS、Al(OH)3和S的混合物,故选D。
HS-+OH-.在Na2S溶液中,有大量S2-、OH-,依题意知,Fe2+结合S2-能力强,两盐发生复分解反应,形成FeS沉淀,Fe2++S2-=FeS↓;Al3+结合OH-能力强,形成Al(OH)3沉淀,Al3++3OH-=Al(OH)3↓,或理解为Al3+与S2-发生双水解反应:3Na2S+AlCl3+6H2O=2Al(OH)3↓+3H2S↑+6NaCl;但由于I2的存在发生:I2+S2-=S↓+2I-或I2+H2S=S↓+2HI,所以最终得到的沉淀是FeS、Al(OH)3和S的混合物,故选D。


科目:高中化学 来源: 题型:
【题目】已知在稀溶液中,酸跟碱发生中和反应生成1mol水时的反应热叫做中和热.现利用如图装置进行中和热的测定,请回答下列问题:
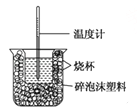
(1)图示装置有两处重要组成部分未画出,它们是 、 。
(2)烧杯间填满碎泡沫塑料的作用是 。
(3)若操作时分几次注入反应液,求得的反应热数值 (填“偏大”“偏小”或“无影响”)。
(4)做一次完整的中和热测定实验,温度计需使用 次。
(5)量取0.5mol/L的盐酸和0.55mol/L的NaOH溶液各50 mL进行实验,测得盐酸和NaOH溶液起始平均温度为t1℃,混合反应后最高温度为t2℃,设溶液密度均为1 g/mL,生成溶液的比热容c = 4.18 J/g℃。请列式计算中和热:△H= kJ/mol(不用化简)。
(6)已知:HCl(aq)+NaOH(aq)===NaCl(aq)+H2O(l) △H1= a kJ/mol
HCl(aq)+NH3H2O(aq)===NH4Cl(aq)+H2O(l) △H2= b kJ/mol
则NH3H2O(aq)![]() NH4+(aq)+ OH-(aq) △H3= ________ kJ/mol(用a、b表示)
NH4+(aq)+ OH-(aq) △H3= ________ kJ/mol(用a、b表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将纯锌片和纯铜片按图方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是
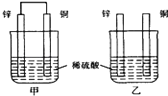
A. 两烧杯中铜片表面均无气泡产生
B. 甲中铜片是正极,乙中铜片是负极
C. 两烧杯中溶液的pH均增大
D. 甲、乙溶液均变蓝色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将羧酸的碱金属盐电解可生成烃类化合物,例如
2CH3COOK+2H2O=CH3—CH3↑+2CO2↑+H2↑+2KOH
现充分电解CH2ClCOOK水溶液,并加热电解后的水溶液,则下列说法中合理的是( )
A.CO2气体在阴极放出
B.加热后有不溶于水的油状物生成
C.混合液蒸干后得到的固体物质是KOH
D.混合液蒸干后得到的固体物质是KCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是中学化学常见单质, X、Y、Z、M、N、W、H、K是常见化合物,X是B和C的化合产物,它们之间有如下转化关系(反应物和产物中的H2O已略去):


(1)Y的电子式为 ,构成C单质的元素在周期表中位于
(2)反应①的离子方程式为 反应②的离子方程式为
(3)某工厂用B制漂白粉。
①写出制漂白粉的化学方程式
②为测定该工厂制得的漂白粉中有效成分的含量,某小组进行了如下实验:称取漂白粉2.0g,研磨后溶解,配制成250mL溶液,取出25.00mL加入到锥形瓶中,再加入过量的KI溶液和过量的硫酸,此时发生的离子方程式为: 静置。待完全反应后,用0.1mol·L-1的Na2S2O3溶液做标准溶液滴定反应生成的碘,已知反应式为:2Na2S2O3+I2=Na2S4O6+2NaI,共用去Na2S2O3溶液20.00mL。则该漂白粉中有效成分的质量分数为 (保留到小数点后两位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列条件下,可以大量共存的离子组是( )
A.某无色溶液中:Na+、Cu2+、Cl-、MnO4-
B.含有大量Fe3+的溶液中:Na+、SO42-、K+、SCN- -
C.含有大量NH4+的溶液中:Ba2+、 K+、Cl-、OH-
D.在pH=1的溶液中:K+、Fe3+、Cl-、NO3-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com