
下表各组物质之间通过一步反应不可以实现如图所示转化关系的是 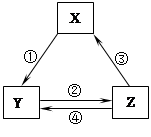
| 选项 | X | Y | Z | 箭头上所标 数字的反应条件 |
| A | SiO2 | Na2SiO3 | H2SiO3 | ①与Na2CO3熔融 |
| B | NaCl | NaHCO3 | Na2CO3 | ②加热 |
| C | N2 | NO2 | HNO3 | ③加热 |
| D | C | CO | CO2 | ④灼热炭粉 |
 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:单选题
物质发生化学变化时常伴有颜色变化,两者对应正确的有
| A.金属钠在空气中燃烧:银白色变白色 |
| B.纯铁丝在氧气中燃烧:黑色变红色 |
| C.苯、浓硫酸、浓硝酸混合溶液受热:无色变浅黄色 |
| D.用H2SO4(aq)滴定NaHCO3(aq)(甲基橙为指示剂):溶液橙色变黄色 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列根据实验操作和现象所得出的结论不正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向硅酸钠溶液中滴加1滴酚酞,然后逐滴加入稀盐酸至红色褪去 | 2 min后,试管里出现凝胶 | 酸性:盐酸>硅酸 |
| B | 在酒精灯上加热铝箔 | 铝箔熔化但不滴落 | 熔点:氧化铝>铝 |
| C | 常温下,向浓硫酸中投入铁片 | 铁片不溶解 | 常温下,铁不与浓硫酸反应 |
| D | 向某溶液中先滴加KSCN溶液,再滴加少量氯水 | 先无明显现象,后溶液变成血红色 | 溶液中含有Fe2+,没有Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
中学化学常见物质甲、乙、丙、丁之间存在转化关系:甲+乙→丙+丁。下列说法正确的是
| A.若甲为铜,丁为氯化亚铁,则乙一定是氯化铁 |
| B.若甲为碳,丁为硅,则丙一定是二氧化碳 |
| C.若甲为铝,丁为铁,则乙一定是氧化铁 |
| D.若甲为镁,丁为氢气,则乙一定是酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
甲、乙、丙、丁、戊的相互转化关系如图所示(反应条件略去,箭头表示一步转化)。下列各组物质中,不满足图示转化关系的是
| | 甲 | 乙 | 丙 | 戊 |
| ① | NH3 | O2 | NO | H2O |
| ② | Fe | H2O | H2 | Fe2O3 |
| ③ | Al2O3 | NaOH溶液 | Na AlO2溶液 | 过量CO2 |
| ④ | Na2O2 | CO2 | O2 | Na |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关物质的性质与应用均正确的是
| A.常温下Cl2能与强碱溶液反应,工业生产和实验室可用澄清石灰水吸收氯气尾气 |
| B.苯酚遇FeCl3溶液显紫色,可用FeCl3溶液检验工业生产的废水中是否存在苯酚 |
| C.铜的金属活动性比铁的弱,可在海轮外壳上装若干铜块以减缓船体的腐蚀速率 |
| D.碳酸钠溶液与硫酸钙能发生复分解反应,可用硫酸钠溶液清除锅炉水垢中的碳酸钙 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
根据下列有关实验得出的结论一定正确的是
| 选项 | 方法 | 结论 |
| A | 同温时,等质量的锌粒分别与足量稀硫酸反应 | 产生氢气量:加过胆矾=没加胆矾 |
| B | 向Fe(NO3)2溶液中滴入用硫酸酸化的H2O2溶液,则溶液变黄 | 氧化性:H2O2>Fe3+ |
| C | 相同温度下,等质量的大理石与等体积、等浓度的盐酸反应 | 反应速率:粉状大理石>块状大理石 |
| D | 向2mL 0.1mol·L-1Na2S溶液中滴入几滴0.1mol·L-1ZnSO4溶液,有白色沉淀生成;再加入几滴0.1mol·L-1 CuSO4溶液,则又有黑色沉淀生成 | 溶度积(Ksp):ZnS>CuS |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列陈述I、II正确且有因果关系的是
| 选项 | 陈述I | 陈述II |
| A | SO2有漂白性 | SO2可使酸性高锰酸钾溶液褪色 |
| B | 硫酸铜是强酸弱碱盐 | 蒸干CuSO4溶液可以得到Cu(OH)2固体 |
| C | SO2是酸性氧化物 | 将SO2通入BaCl2溶液可生成BaSO3沉淀 |
| D | 氢氧化铝显两性 | 向AlCl3溶液中滴加氨水,产生白色沉淀;再加入过量NaOH溶液,沉淀消失 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为40,B、W同周期,D、E同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等。
(1)E元素的盐酸盐或硫酸盐可以用来净水,原理是_______________________(文字表述)。
(2)A2W2的分子中所含的化学键为________、________,经测定A2W2为二元弱酸,其酸性比碳酸的还要弱,请写出其第一步电离的电离方程式___________。
(3)废印刷电路板上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现改用A2W2和稀硫酸浸泡废印刷电路板既达到上述目的,又保护了环境,试写出反应的离子方程式____________________。
(4)元素D的单质在一定条件下,能与A单质化合生成一种氢化物DA,熔点为800℃,DA能与水反应放氢气,若将1 mol DA和1 mol E单质混合加入足量的水,充分反应后生成气体的体积是__________________(标准状况下)。
(5)D的某化合物呈淡黄色,可与氯化亚铁溶液反应。若淡黄色固体与氯化亚铁反应的物质的量之比为1∶2,且无气体生成,则该反应的离子方程式为____________________。
(6)在常温下用气体密度测定BW2的相对分子质量,实验值比理论值偏________(填 “高”或“低”),其原因是___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com