
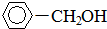

18 8 |
| A、②③⑥ | B、③⑥ |
| C、①③⑤⑥ | D、①②③④⑤⑥ |
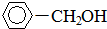 ,故③正确;
,故③正确;  ,故④错误;
,故④错误;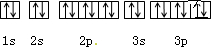 ,故⑤错误;
,故⑤错误;

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、饱和氯水中:Cl-、NO3-、Na+、SO32- |
| B、c(H+)=1.0×10-13mol/L溶液中:CH3COO-、K+、SO42-、Br- |
| C、与铝反应产生大量氢气的溶液:Na+、K+、CO32-、NO3- |
| D、pH=12的溶液中:NO3-、I-、Na+、Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向污水中投放明矾,生成能凝聚悬浮物的胶体:Al3++3H2O?Al(OH)3(胶体)+3H+ |
| B、钠与硫酸铜溶液反应:Cu2++2Na=2Na++Cu |
| C、铁屑溶于过量稀硝酸:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O |
| D、大理石溶于醋酸中:CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,48gO2和48g O3 含有的氧原子数均为3NA |
| B、1mol?L-1 NaCl溶液中含有Na+的个数为NA |
| C、22.4L N2所含分子数为NA |
| D、标准状况下,22.4 L的水中含有NA个H2O分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 甲 | 乙 | 丙 | 丁 | |
| 化合物中各元素 原子个数比 | A:C=1:1 | B:A=1:2 | D:E=1:3 | B:E=1:4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com