
| A、常温常压下,48gO2和48g O3 含有的氧原子数均为3NA |
| B、1mol?L-1 NaCl溶液中含有Na+的个数为NA |
| C、22.4L N2所含分子数为NA |
| D、标准状况下,22.4 L的水中含有NA个H2O分子 |


 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案科目:高中化学 来源: 题型:
| A、小于5Q | B、5Q |
| C、5Q~10Q | D、10Q |
查看答案和解析>>
科目:高中化学 来源: 题型:
 生物质能是一种洁净、可再生的能源.生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一.
生物质能是一种洁净、可再生的能源.生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径A<B |
| B、电负性A<B |
| C、元素A、B不同周期 |
| D、A原子序数小于B原子序数 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、36gH2O和22.4LCO2中Si和O,C和O之间的共价键均是4×6.02×1023 |
| B、0.1 L 3 mol?L-1的NH4NO3溶液中含有的NH4+数目为0.3×6.02×1023 |
| C、常温常压下,4.6 g NO2气体含有0.1×6.02×1023个NO2分子 |
| D、0.1 mol的甲基(-CH3)和羟基(-OH)所含电子数均为0.9×6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:
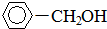

18 8 |
| A、②③⑥ | B、③⑥ |
| C、①③⑤⑥ | D、①②③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
144 62 |
150 62 |
A、
| ||||
B、
| ||||
C、
| ||||
D、据
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.15mol/L |
| B、0.2mol/L |
| C、0.3mol/L |
| D、0.4mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com