

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��4 | B��6 | C��7 | D��8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
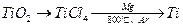
 2Cl2(g) = TiCl4(s)+O2(g)����H=+141kJ/mol
2Cl2(g) = TiCl4(s)+O2(g)����H=+141kJ/mol�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��NaOH | B��Na2O2 | C��MgCl2 | D��H2O2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��HCl NaCl | B��SiO2 CO2 |
| C��Na2CO3 KClO3 | D��H2O2 Na2O2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ֻ���й��ۼ������ʲ�һ���ǹ��ۻ����� |
| B���ɵ��Ӷ����ƶ�������������ǽ������� |
C���м��ܺ� ��Ĺ��ۼ����ڵ������۷е�һ���ܸ� ��Ĺ��ۼ����ڵ������۷е�һ���ܸ� |
| D�������ӻ������в����ܴ��ڷǼ��Թ��ۼ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��m + n ��p | B��m+n�� p | C��m�� p | D��m = p |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��C60��һ�����ͻ����� | B��C60�к����ۼ� |
| C��C60�к����Ӽ� | D��C60�ͽ��ʯ����̼��ͬλ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����������ӵľ����бغ��������� |
| B���ɼ��Լ����ɵ�AB2�ͷ��ӱ��Ǽ��Է��� |
| C���ǽ���Ԫ����ɵĻ�������ֻ���й��ۼ� |
| D�����Ӿ����бغ������ӽ������Ӿ����бغ��й��ۼ� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com