
【题目】完成下列各题:
(1)烃A的结构简式为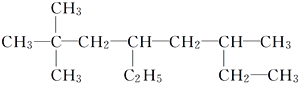 。用系统命名法命名烃A:__________________________________________________。
。用系统命名法命名烃A:__________________________________________________。
(2)某烃的分子式为C5H12,核磁共振氢谱图中显示三个峰,则该烃的一氯代物有________种,该烃的结构简式为________________。
(3)麻黄素又称黄碱,是我国特定的中药材麻黄中所含有的一种生物碱。经科学家研究发现其结构如下: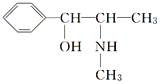 。下列各物质:
。下列各物质:
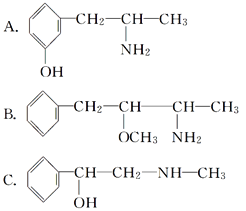
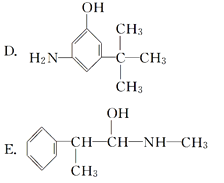
与麻黄素互为同分异构体的是________(填字母,下同),互为同系物的是________。
【答案】2,2,6-三甲基-4-乙基辛烷3CH3CH2CH2CH2CH3DEC
【解析】
(1)有机物A是烷烃,主链含有8个碳原子,3个甲基和1个乙基作支链,名称为2,2,6-三甲基-4-乙基辛烷;
(2)某烃的分子式为C5H12,核磁共振氢谱图中显示三个峰,是正戊烷,则该烃的一氯代物有3种,该烃的结构简式为CH3CH2CH2CH2CH3。
(3)分子式相同结构不同的化合物互为同分异构体,麻黄素的分子式为C10H15NO,A~E的分子式分别是C9H13NO、C11H17NO、C9H13NO、C10H15NO、C10H15NO,则与麻黄素互为同分异构体的是DE;结构相似分子组成相差若干个CH2原子团的化合物互为同系物,则与麻黄素互为同系物的是C。


 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案科目:高中化学 来源: 题型:
【题目】环境中常见的重金属污染物有汞、铅、锰、铬、镉。处理工业废水中含有的![]() 和
和![]() 常用的方法是还原沉淀法,该法的工艺流程为
常用的方法是还原沉淀法,该法的工艺流程为![]()
![]()
![]()
![]() Cr3+
Cr3+![]() Cr(OH)3。
Cr(OH)3。
其中第①步存在平衡:2![]() (黄色)+2H+
(黄色)+2H+![]()
![]() (橙色)+H2O。
(橙色)+H2O。
(1)写出第①步反应的平衡常数表达式:_________________________________。
(2)关于第①步反应,下列说法正确的是________(填序号)。
A.通过测定溶液的pH可以判断反应是否已达到平衡状态
B.该反应为氧化还原反应
C.在强酸性环境下,溶液的颜色为橙色
(3)第②步反应中,还原0.1 mol![]() ,需要________mol FeSO4·7H2O。
,需要________mol FeSO4·7H2O。
(4)第③步反应除生成Cr(OH)3沉淀外,还可能生成的沉淀为________。
(5)在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)![]() Cr3+(aq)+3OH-(aq)。常温下,Cr(OH)3的溶度积常数Ksp=10-32,当溶液中Cr3+的浓度降至10-5mol·L-1,认为Cr3+已经完全沉淀。现将第③步反应后溶液的pH调至4,请通过计算说明Cr3+是否沉淀完全(请写出计算过程)。____________
Cr3+(aq)+3OH-(aq)。常温下,Cr(OH)3的溶度积常数Ksp=10-32,当溶液中Cr3+的浓度降至10-5mol·L-1,认为Cr3+已经完全沉淀。现将第③步反应后溶液的pH调至4,请通过计算说明Cr3+是否沉淀完全(请写出计算过程)。____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法符合事实的是 ( )
A.CO2通入水玻璃中得到白色沉淀
B.SiO2溶于水成为硅酸
C.CO2通入饱和CaCl2溶液能生成白色沉淀
D.硅酸酸性比碳酸弱,所以SiO2不能跟Na2CO3反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锰锂电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质LiClO4溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2。回答下列问题:
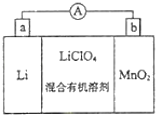
(1)外电路的电流方向是______(填“a→b”或“b→a”)。
(2)电池正极反应式_______。
(3)不能用水代替电池中的混合有机溶剂,原因是________。
(4)MnO2可与KOH和KClO3在高温下反应,生成K2MnO4,反应的化学方程式为_____,K2MnO4在酸性溶液中歧化,生成KMnO4和MnO2的物质的量之比为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁烯(C4H8)是制备线性低密度聚乙烯(LLDPE)的原料之一,可由丁烷(C4H10)催化脱氢制备,C4H10(g)![]() C4H8(g)+H2(g)
C4H8(g)+H2(g) ![]() H=+123kJ·mol-1。该工艺过程中生成的副产物有炭(C)、C2H6、C2H4、C4H6等。进料比[
H=+123kJ·mol-1。该工艺过程中生成的副产物有炭(C)、C2H6、C2H4、C4H6等。进料比[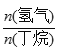 ]和温度对丁烯产率的影响如图1、图2所示。已知原料气中氢气的作用是活化固体催化剂。
]和温度对丁烯产率的影响如图1、图2所示。已知原料气中氢气的作用是活化固体催化剂。
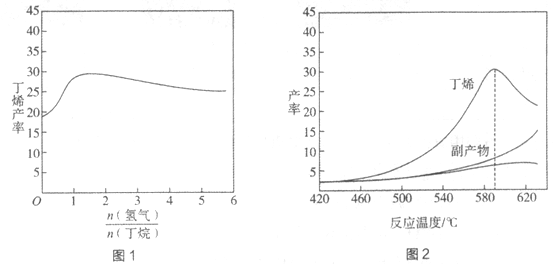
下列分析正确的是
A. 氢气的作用是活化固体催化剂,改变氢气量不会影响丁烯的产率
B. 丁烷催化脱氢是吸热反应,丁烯的产率随温度升高而不断增大
C. 随温度升高丁烯裂解生成的副产物增多,会影响丁烯的产率
D. 一定温度下,控制进料比[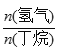 ]越小,越有利于提高丁烯的产率
]越小,越有利于提高丁烯的产率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子一定能大量存在的是
A. 加入铝粉可以产生H2的溶液中:Al3+、K+、SO42-、Cl﹣
B. 滴入酚酞显红色的溶液:Na+、Mg2+、NO3﹣、HSO3﹣
C. 在酸性溶液中:Cu2+、I-、![]() 、Na+
、Na+
D. 在中性溶液中:Mg2+、NO3-、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.有机物X是一种重要的有机合成中间体,用于制造塑料、涂料和黏合剂等高聚物。为研究X的组成与结构,进行了如下实验:
(1)有机物X的质谱图为: | |
| 有机物X的相对分子质量是________。 |
(2)将10.0 g X在足量O2中充分燃烧,并使其产物依次通过足量的无水CaCl2和KOH浓溶液,发现无水CaCl2增重7.2 g,KOH浓溶液增重22.0 g。 | 有机物X的分子式是______。 |
(3)经红外光谱测定,有机物X中含有醛基;有机物X的核磁共振氢谱图上有2个吸收峰,峰面积之比是3∶1。 | 有机物X的结构简式是__________。 |
II.写出与![]() 互为同分异构体,且一溴代物只有两种的芳香烃的结构简式和名称:________________、___________。
互为同分异构体,且一溴代物只有两种的芳香烃的结构简式和名称:________________、___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向100mL Fe2(SO4)3和CuSO4的混合溶液中逐渐加入铁粉,充分反应后溶液中固体剩余物的质量与加入铁粉的质量如图所示。忽略溶液体积的变化,下列说法不正确的是
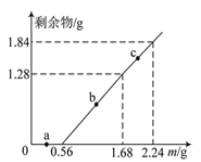
A. a点时溶液中阳离子为Cu2+、Fe2+和Fe3+
B. b点时溶液中发生的反应为:Fe+Cu2+=Cu+Fe2+
C. c点时溶液中溶质的物质的量浓度为0.5 mol·L-1
D. 原溶液中Fe2(SO4)3和CuSO4的物质的量浓度之比为1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述不相符合的是

A.图甲表示燃料燃烧反应的能量变化
B.图乙表示酶催化反应的反应速率随反应温度的变化
C.图丙表示弱电解质在水中建立电离平衡的过程
D.图丁表示强碱滴定强酸的滴定曲线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com