
一定温度下,向一容积为5 L的恒容密闭容器中充入0.4 mol SO2和0.2 mol O2,发生反应:2SO2(g)+O2(g) 2SO3(g) ΔH=-196 kJ·mol-1。当反应达到平衡时,容器内压强变为起始时的0.7倍。请回答下列问题:
2SO3(g) ΔH=-196 kJ·mol-1。当反应达到平衡时,容器内压强变为起始时的0.7倍。请回答下列问题:
(1)判断该反应达到平衡状态的标志是 (填字母)。
a.SO2、O2、SO3三者的浓度之比为2∶1∶2
b.容器内气体的压强不变
c.容器内混合气体的密度保持不变
d.SO3的物质的量不再变化
e.SO2的生成速率和SO3的生成速率相等
(2)①SO2的转化率为 ;②达到平衡时反应放出的热量为 ;③此温度下该反应的平衡常数K= 。
(3)如图表示平衡时SO2的体积分数随压强和温度变化的曲线,则:
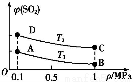
①温度关系:T1 T2(填“>”、“<”或“=”,下同);
②平衡常数关系:KA KB,KA KD。
(1)b、d、e (2)①90% ②35.28 kJ ③20 250
(3)①< ②= >
【解析】(1)SO2、O2、SO3三者浓度比为2∶1∶2,与平衡状态无必然联系,不能作为建立平衡的标志,容器内气体压强随反应进行而变化,气体压强不变,则建立平衡;气体总质量不变,容器体积不变,混合气体密度也不变,不能作为平衡状态标志;SO3的物质的量是随反应进行而发生变化的,当其不变时,表示反应已建立平衡;SO2的生成速率是v(SO2)逆,SO3生成速率是v(SO3)正,而v(SO2)正=v(SO3)正,则有v(SO2)逆=v(SO2)正,这是平衡建立的根本标志。所以可作为平衡状态标志的是b、d、e。
(2) 2SO2(g)+O2(g)  2SO3(g)
2SO3(g)
起始(mol) 0.4 0.2 0
变化(mol) x x/2 x
平衡(mol) 0.4-x 0.2-x/2 x
T、V恒定,气体的压强之比等于物质的量之比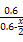 =
=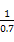 ,解得x=0.36,故SO2转化率为:
,解得x=0.36,故SO2转化率为: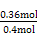 ×100%=90%。放出热量为:
×100%=90%。放出热量为: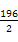 kJ·mol-1×0.4 mol×90%=35.28 kJ,K=
kJ·mol-1×0.4 mol×90%=35.28 kJ,K=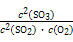 =
=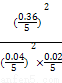 =20 250。
=20 250。
(3)该反应是放热反应,温度升高平衡左移,SO2体积分数增大,所以T2>T1,平衡常数只与温度有关,温度不变,K值不变,则KA=KB,升温,平衡左移,K值减小,KA>KD。


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源:2014高考化学二轮专题突破 专题三溶液组成的计量及其应用练习卷(解析版) 题型:选择题
在标准状况下,将a L NH3完全溶于水得到V mL氨水,溶液的密度为ρ g·cm-3,溶质的质量分数为w,溶质的物质的量浓度为c mol·L-1。下列叙述中正确的是( )
①w=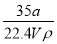 ×100%
×100%
②c=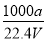
③若上述溶液中再加入V mL水后,所得溶液的质量分数大于0.5w
④若上述溶液中再加入0.5V mL同浓度稀盐酸,充分反应后溶液中离子浓度大小关系为c(NH4+)>c(Cl-)>c(OH-)>c(H+)
A.①④ B.②③ C.①③ D.②④
查看答案和解析>>
科目:高中化学 来源:2014高考化学专题突破训练 专题9金属及其化合物练习卷(解析版) 题型:选择题
A+B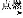 C
C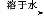 C溶液
C溶液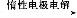 A+B,已知A、B为单质,C为化合物。能实现上述转化关系的是( )
A+B,已知A、B为单质,C为化合物。能实现上述转化关系的是( )
①若C溶于水后得到强碱溶液,则A可能是Na
②若C溶液遇Na2CO3放出CO2气体,则A可能是H2
③若C溶液中滴加KSCN溶液显血红色,则B可能为Fe
④若C溶液中滴加NaOH溶液有蓝色沉淀生成,则B可能为Cu
A.①② B.③④ C.①③ D.②④
查看答案和解析>>
科目:高中化学 来源:2014高考化学专题突破训练 专题8电化学原理练习卷(解析版) 题型:选择题
下列叙述正确的是( )
A.电镀时,通常把待镀的金属制品作阳极
B.氯碱工业是电解熔融的NaCl,在阳极能得到Cl2
C.如图中电子由Zn极流向Cu,盐桥中的Cl-移向CuSO4溶液
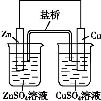
D.氢氧燃料电池(酸性电解质)中O2通入正极,电极反应为:O2+4H++4e-=2H2O
查看答案和解析>>
科目:高中化学 来源:2014高考化学专题突破训练 专题7电解质溶液练习卷(解析版) 题型:选择题
现有0.1 mol·L-1氨水10 mL,加蒸馏水稀释到1 L后,下列变化中正确的是( )
①电离程度增大;②c(NH3·H2O)增大;③N 数目增多;④c(OH-)增大;⑤导电性增强;⑥
数目增多;④c(OH-)增大;⑤导电性增强;⑥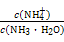 增大
增大
A.①②③ B.①③⑤ C.①③⑥ D.②④⑥
查看答案和解析>>
科目:高中化学 来源:2014高考化学专题突破训练 专题6化学反应速率和化学平衡练习卷(解析版) 题型:选择题
已知合成氨反应N2(g)+3H2(g) 2NH3(g) ΔH=-92.20 kJ·mol-1,在某温度下2 L的密闭容器中进行,测得如下数据:
2NH3(g) ΔH=-92.20 kJ·mol-1,在某温度下2 L的密闭容器中进行,测得如下数据:
时间(h) 物质的量(mol) | 0 | 1 | 2 | 3 | 4 |
N2 | 1.50 | n1 | 1.20 | n3 | n5 |
H2 | 4.50 | 4.20 | 3.60 | n4 | n6 |
NH3 | 0 | 0.20 | n2 | 1.00 | 1.00 |
下列说法正确的是( )
A.反应3 h内,反应速率v(N2)为0.17 mol·L-1·h-1
B.此温度下,该反应的平衡常数为0.037
C.反应进行到1 h时放出的热量为9.22 kJ
D.4 h时,若再加入1 mol N2,达到新的化学平衡时,N2的转化率是原来的两倍
查看答案和解析>>
科目:高中化学 来源:2014高考化学专题突破训练 专题5物质结构 元素周期律练习卷(解析版) 题型:填空题
A、B、C、D、E为原子序数依次增大的五种短周期元素,其中仅含有一种金属元素,A和D最外层电子数相同;B、C和E在周期表中相邻,且C、E同主族。B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成两种常见的液态化合物。 请回答下列问题:
(1)B的原子结构示意图 。
(2)C、D、E三种原子对应的离子半径由大到小的顺序是 (填具体离子);由A、B、C三种元素按4∶2∶3组成的化合物所含的化学键类型为 。
(3)用某种废弃的金属易拉罐与A、C、D组成的化合物溶液反应,该反应的离子方程式为: 。
(4)在100 mL 18 mol/L的浓的A、C、E组成的酸溶液中加入过量的铜片,加热使之充分反应, 产生的气体在标准状况下的体积可能是 (填序号);
a.7.32 L b.6.72 L c.20.16 L d.30.24 L
若使上述反应中剩余的铜片继续溶解,可向其中加入硝酸钠,反应的离子方程式为: 。
(5)A、C两元素的单质与熔融K2CO3组成的燃料电池,其负极反应式为 ,用该电池电解1 L 1 mol/L NaCl溶液当消耗标准状况下1.12 L H2时,NaCl溶液的pH= (假设电解过程中溶液的体积不变)。
查看答案和解析>>
科目:高中化学 来源:2014高考化学专题突破训练 专题4化学反应中的能量变化练习卷(解析版) 题型:选择题
已知:①2H2(g)+O2(g) 2H2O(g)ΔH=-483.6 kJ/mol
2H2O(g)ΔH=-483.6 kJ/mol
②H2(g)+S(g)=H2S(g) ΔH=-20.1 kJ/mol。下列判断正确的是( )
A.1 mol氢气完全燃烧吸热241.8 kJ
B.1 mol H2O(g)和1 mol H2S(g)的能量相差221.7 kJ
C.由①②知,水的热稳定性小于硫化氢
D.若反应②中改用固态硫,1 mol S(s)完全反应,放出的热量小于20.1 kJ
查看答案和解析>>
科目:高中化学 来源:2014高考化学专题突破训练 专题14有机化学基础选修5练习卷(解析版) 题型:填空题
生活中常用的某种香料X的结构简式为: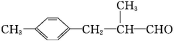
(1)香料X中含氧官能团的名称是 。
(2)香料X可发生的反应类型是 (填代号)。
a.酯化反应 b.还原反应
c.加成反应 d.消去反应
(3)已知:
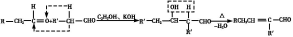
香料X的合成路线如下:
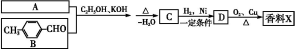
①A的结构简式是 。
②检验有机物C中含有碳碳双键所需用的试剂 。
a.银氨溶液 b.酸性高锰酸钾溶液
c.溴水 d.氢氧化钠溶液
③D→X的化学方程式为 。
④有机物B的某种同分异构体E,具有如下性质:
a.与浓溴水反应生成白色沉淀,且1 mol E最多能与4 mol Br2反应
b.红外光谱显示该有机物中存在碳碳双键
则E的结构简式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com