
AЁЂBЁЂCЁЂDЁЂEЮЊдзгађЪ§вРДЮдіДѓЕФЮхжжЖЬжмЦкдЊЫи,ЦфжаНіКЌгавЛжжН№ЪєдЊЫи,AКЭDзюЭтВуЕчзгЪ§ЯрЭЌ;BЁЂCКЭEдкжмЦкБэжаЯрСк,ЧвCЁЂEЭЌжїзхЁЃBЁЂCЕФзюЭтВуЕчзгЪ§жЎКЭЕШгкDЕФдзгКЫЭтЕчзгЪ§,AКЭCПЩаЮГЩСНжжГЃМћЕФвКЬЌЛЏКЯЮяЁЃ ЧыЛиД№ЯТСаЮЪЬт:
(1)BЕФдзгНсЙЙЪОвтЭМ ЁЃ
(2)CЁЂDЁЂEШ§жждзгЖдгІЕФРызгАыОЖгЩДѓЕНаЁЕФЫГађЪЧ (ЬюОпЬхРызг);гЩAЁЂBЁЂCШ§жждЊЫиАД4ЁУ2ЁУ3зщГЩЕФЛЏКЯЮяЫљКЌЕФЛЏбЇМќРраЭЮЊ ЁЃ
(3)гУФГжжЗЯЦњЕФН№ЪєвзРЙогыAЁЂCЁЂDзщГЩЕФЛЏКЯЮяШмвКЗДгІ,ИУЗДгІЕФРызгЗНГЬЪНЮЊ: ЁЃ
(4)дк100 mL 18 mol/LЕФХЈЕФAЁЂCЁЂEзщГЩЕФЫсШмвКжаМгШыЙ§СПЕФЭЦЌ,МгШШЪЙжЎГфЗжЗДгІ, ВњЩњЕФЦјЬхдкБъзМзДПіЯТЕФЬхЛ§ПЩФмЪЧ (ЬюађКХ);
a.7.32 L b.6.72 L c.20.16 L d.30.24 L
ШєЪЙЩЯЪіЗДгІжаЪЃгрЕФЭЦЌМЬајШмНт,ПЩЯђЦфжаМгШыЯѕЫсФЦ,ЗДгІЕФРызгЗНГЬЪНЮЊ: ЁЃ
(5)AЁЂCСНдЊЫиЕФЕЅжЪгыШлШкK2CO3зщГЩЕФШМСЯЕчГи,ЦфИКМЋЗДгІЪНЮЊ ,гУИУЕчГиЕчНт1 L 1 mol/L NaClШмвКЕБЯћКФБъзМзДПіЯТ1.12 L H2ЪБ,NaClШмвКЕФpH= (МйЩшЕчНтЙ§ГЬжаШмвКЕФЬхЛ§ВЛБф)ЁЃ
(1) (2)S2-ЃОO2-ЃОNa+ ЙВМлМќКЭРызгМќ
(2)S2-ЃОO2-ЃОNa+ ЙВМлМќКЭРызгМќ
(3)2Al+2OH-+2H2O=2Al +3H2Ёќ
+3H2Ёќ
(4)ab 3Cu+8H++2N =3Cu2++2NOЁќ+4H2O
=3Cu2++2NOЁќ+4H2O
(5)H2+C -2e-=CO2Ёќ+H2O 13
-2e-=CO2Ёќ+H2O 13
ЁОНтЮіЁПгЩгкAКЭCПЩаЮГЩСНжжГЃМћЕФвКЬЌЛЏКЯЮя,ЧвCЕФдзгађЪ§Дѓ,ЙЪAЮЊH,CЮЊO,НсКЯCЁЂEЮЊЭЌжїзхЕФЖЬжмЦкдЊЫи,дђEЮЊS;гжОнAЁЂDзюЭтВуЕчзгЪ§ЯрЭЌ,ЙЪDЮЊNa;дйОнBЁЂCЕФзюЭтВуЕчзгЪ§жЎКЭЕШгкDЕФдзгКЫЭтЕчзгЪ§,дђBЮЊNЁЃЙЪ(1)NЕФдзгНсЙЙЪОвтЭМЮЊ ЁЃ(2)ЕчзгВуЪ§дНЖр,РызгЕФАыОЖдНДѓ,ЖјЕчзгВуНсЙЙЯрЭЌЕФРызг,ЁАКЫДѓОЖаЁЁБ,ЙЪРызгАыОЖДѓаЁЫГађЮЊS2-ЃОO2-ЃОNa+,гЩAЁЂBЁЂCШ§жждЊЫиАД4ЁУ2ЁУ3зщГЩЕФЛЏКЯЮяЪЧNH4NO3,NH4NO3жаКЌгаРызгМќКЭЙВМлМќЁЃ(3)AlКЭNaOHШмвКЗДгІЩњГЩNaAlO2КЭH2,РызгЗНГЬЪНЮЊ2Al+2OH-+2H2O=2Al
ЁЃ(2)ЕчзгВуЪ§дНЖр,РызгЕФАыОЖдНДѓ,ЖјЕчзгВуНсЙЙЯрЭЌЕФРызг,ЁАКЫДѓОЖаЁЁБ,ЙЪРызгАыОЖДѓаЁЫГађЮЊS2-ЃОO2-ЃОNa+,гЩAЁЂBЁЂCШ§жждЊЫиАД4ЁУ2ЁУ3зщГЩЕФЛЏКЯЮяЪЧNH4NO3,NH4NO3жаКЌгаРызгМќКЭЙВМлМќЁЃ(3)AlКЭNaOHШмвКЗДгІЩњГЩNaAlO2КЭH2,РызгЗНГЬЪНЮЊ2Al+2OH-+2H2O=2Al +3H2ЁќЁЃ(4)AЁЂCЁЂEзщГЩЕФЫсЮЊH2SO4,ХЈH2SO4КЭCuЗДгІЕЋЯЁH2SO4КЭCuВЛЗДгІ,ЙЪЩњГЩSO2ЕФЮяжЪЕФСПаЁгкСђЫсЕФвЛАы,ИљОнСђдзгЪиКужЊ,ЦјЬхЕФЬхЛ§аЁгк20.16 L,ЙЪбЁaЁЂbЁЃШєМгШыNaNO3,ЬсЙЉЕФN
+3H2ЁќЁЃ(4)AЁЂCЁЂEзщГЩЕФЫсЮЊH2SO4,ХЈH2SO4КЭCuЗДгІЕЋЯЁH2SO4КЭCuВЛЗДгІ,ЙЪЩњГЩSO2ЕФЮяжЪЕФСПаЁгкСђЫсЕФвЛАы,ИљОнСђдзгЪиКужЊ,ЦјЬхЕФЬхЛ§аЁгк20.16 L,ЙЪбЁaЁЂbЁЃШєМгШыNaNO3,ЬсЙЉЕФN гыH+гжгыCuЗДгІ:3Cu+8H++2N
гыH+гжгыCuЗДгІ:3Cu+8H++2N =3Cu2++2NOЁќ+4H2OЁЃ(5)зщГЩЕФЕчГиЪЧЧтбѕШМСЯЕчГи,ИКМЋЩЯH2ЪЇШЅЕчзгКЭC
=3Cu2++2NOЁќ+4H2OЁЃ(5)зщГЩЕФЕчГиЪЧЧтбѕШМСЯЕчГи,ИКМЋЩЯH2ЪЇШЅЕчзгКЭC ЗДгІЩњГЩCO2КЭЫЎ,ЕчМЋЗДгІЪНЮЊH2+C
ЗДгІЩњГЩCO2КЭЫЎ,ЕчМЋЗДгІЪНЮЊH2+C -2e-=CO2Ёќ+H2OЁЃЕБЯћКФБъзМзДПіЯТ1.12 L H2МДn(H2)=0.05 mol,дђЕчНтNaClШмвКЪБЯћКФH2OЕчРыГіЕФH+ЕФЮяжЪЕФСПЮЊ0.1 mol,дђВњЩњЕФn(OH-)=0.1 mol,МД c(OH-)=
-2e-=CO2Ёќ+H2OЁЃЕБЯћКФБъзМзДПіЯТ1.12 L H2МДn(H2)=0.05 mol,дђЕчНтNaClШмвКЪБЯћКФH2OЕчРыГіЕФH+ЕФЮяжЪЕФСПЮЊ0.1 mol,дђВњЩњЕФn(OH-)=0.1 mol,МД c(OH-)= =0.1 mol/L,ЫљвдpH=13ЁЃ
=0.1 mol/L,ЫљвдpH=13ЁЃ


 гІгУЬтзївЕБОЯЕСаД№АИ
гІгУЬтзївЕБОЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2014ИпПМЛЏбЇЖўТжзЈЬтЭЛЦЦ зЈЬтЦпЛЏбЇЗДгІгыФмСПСЗЯАОэЃЈНтЮіАцЃЉ ЬтаЭЃКбЁдёЬт
вбжЊввШВгыБНеєЦјЭъШЋШМЩеЕФШШЛЏбЇЗНГЬЪНШчЯТЫљЪОЃК
Ђй2C2H2(g)ЃЋ5O2(g)=4CO2(g)ЃЋ2H2O(l)
ІЄHЃНЃ2 600 kJЁЄmolЃ1
Ђк2C6H6(g)ЃЋ15O2(g)=12CO2(g)ЃЋ6H2O(l)
ІЄHЃНЃ6 590 kJЁЄmolЃ1
ЯТСаЫЕЗЈе§ШЗЕФЪЧЃЈ ЃЉ
AЃЎ2 mol C2H2(g)ЭъШЋШМЩеЩњГЩЦјЬЌЫЎЪБЗХШШДѓгк2 600 kJ
BЃЎ2 mol C6H6(l)ЭъШЋШМЩеЩњГЩвКЬЌЫЎЪБЗХШШДѓгк6 590 kJ
CЃЎЯрЭЌЬѕМўЯТЃЌЕШжЪСПЕФC2H2(g)гыC6H6(g)ЭъШЋШМЩеЃЌC6H6(g)ЗХШШИќЖр
DЃЎC2H2(g)Ш§ОлЩњГЩC6H6(g)ЕФЙ§ГЬЪєгкЗХШШЗДгІ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2014ИпПМЛЏбЇзЈЬтЭЛЦЦбЕСЗ зЈЬт8ЕчЛЏбЇдРэСЗЯАОэЃЈНтЮіАцЃЉ ЬтаЭЃКбЁдёЬт
гУЫсадЧтбѕШМСЯЕчГиЮЊЕчдДНјааЕчНтЕФЪЕбщзАжУЭМШчЭМЫљЪО,ЯТСаЫЕЗЈжае§ШЗЕФЪЧЃЈ ЃЉ
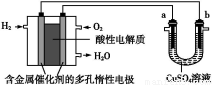
A.ШМСЯЕчГиЙЄзїЪБ,е§МЋЗДгІЮЊ:O2+2H2O+4e-=4OH-
B.aМЋЪЧЬњ,bМЋЪЧЭЪБ,bМЋж№НЅШмНт,aМЋЩЯгаЭЮіГі
C.aМЋЪЧДжЭ,bМЋЪЧДПЭЪБ,aМЋж№НЅШмНт,bМЋЩЯгаЭЮіГі
D.aЁЂbСНМЋОљЪЧЪЏФЋЪБ,дкЯрЭЌЬѕМўЯТaМЋВњЩњЕФЦјЬхгыЕчГижаЯћКФЕФH2ЬхЛ§ЯрЕШ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2014ИпПМЛЏбЇзЈЬтЭЛЦЦбЕСЗ зЈЬт6ЛЏбЇЗДгІЫйТЪКЭЛЏбЇЦНКтСЗЯАОэЃЈНтЮіАцЃЉ ЬтаЭЃКЬюПеЬт
вЛЖЈЮТЖШЯТ,ЯђвЛШнЛ§ЮЊ5 LЕФКуШнУмБеШнЦїжаГфШы0.4 mol SO2КЭ0.2 mol O2,ЗЂЩњЗДгІ:2SO2(g)+O2(g) 2SO3(g) ІЄH=-196 kJЁЄmol-1ЁЃЕБЗДгІДяЕНЦНКтЪБ,ШнЦїФкбЙЧПБфЮЊЦ№ЪМЪБЕФ0.7БЖЁЃЧыЛиД№ЯТСаЮЪЬт:
2SO3(g) ІЄH=-196 kJЁЄmol-1ЁЃЕБЗДгІДяЕНЦНКтЪБ,ШнЦїФкбЙЧПБфЮЊЦ№ЪМЪБЕФ0.7БЖЁЃЧыЛиД№ЯТСаЮЪЬт:
(1)ХаЖЯИУЗДгІДяЕНЦНКтзДЬЌЕФБъжОЪЧ (ЬюзжФИ)ЁЃ
a.SO2ЁЂO2ЁЂSO3Ш§епЕФХЈЖШжЎБШЮЊ2ЁУ1ЁУ2
b.ШнЦїФкЦјЬхЕФбЙЧПВЛБф
c.ШнЦїФкЛьКЯЦјЬхЕФУмЖШБЃГжВЛБф
d.SO3ЕФЮяжЪЕФСПВЛдйБфЛЏ
e.SO2ЕФЩњГЩЫйТЪКЭSO3ЕФЩњГЩЫйТЪЯрЕШ
(2)ЂйSO2ЕФзЊЛЏТЪЮЊ ;ЂкДяЕНЦНКтЪБЗДгІЗХГіЕФШШСПЮЊ ;ЂлДЫЮТЖШЯТИУЗДгІЕФЦНКтГЃЪ§K= ЁЃ
(3)ШчЭМБэЪОЦНКтЪБSO2ЕФЬхЛ§ЗжЪ§ЫцбЙЧПКЭЮТЖШБфЛЏЕФЧњЯп,дђ:
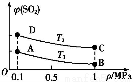
ЂйЮТЖШЙиЯЕ:T1 T2(ЬюЁАЃОЁБЁЂЁАЃМЁБЛђЁА=ЁБ,ЯТЭЌ);
ЂкЦНКтГЃЪ§ЙиЯЕ:KA KB,KA KDЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2014ИпПМЛЏбЇзЈЬтЭЛЦЦбЕСЗ зЈЬт6ЛЏбЇЗДгІЫйТЪКЭЛЏбЇЦНКтСЗЯАОэЃЈНтЮіАцЃЉ ЬтаЭЃКбЁдёЬт
ЮЊМѕаЁCO2ЖдЛЗОГЕФгАЯь,дкГЋЕМЁАЕЭЬМЁБЕФЭЌЪБ,ЛЙашМгЧПЖдCO2ДДаТРћгУЕФбаОПЁЃT1 ЁцЪБ,НЋ9 mol CO2 КЭ12 mol H2ГфШы3 LУмБеШнЦїжа,ЗЂЩњЗДгІCO2(g)+3H2(g) CH3OH(g)+H2O(g) ІЄHЃМ0,ШнЦїжаCH3OHЕФЮяжЪЕФСПЫцЪБМфБфЛЏШчЧњЯпЂёЫљЪО,ЦНКтЪБШнЦїФкбЙЧПЮЊp1ЁЃИФБфФГвЛЬѕМўжиаТНјааЩЯЪіЗДгІ,CH3OHЕФЮяжЪЕФСПЫцЪБМфБфЛЏШчЧњЯпЂђЫљЪОЁЃЯТСаЫЕЗЈДэЮѓЕФЪЧЃЈ ЃЉ
CH3OH(g)+H2O(g) ІЄHЃМ0,ШнЦїжаCH3OHЕФЮяжЪЕФСПЫцЪБМфБфЛЏШчЧњЯпЂёЫљЪО,ЦНКтЪБШнЦїФкбЙЧПЮЊp1ЁЃИФБфФГвЛЬѕМўжиаТНјааЩЯЪіЗДгІ,CH3OHЕФЮяжЪЕФСПЫцЪБМфБфЛЏШчЧњЯпЂђЫљЪОЁЃЯТСаЫЕЗЈДэЮѓЕФЪЧЃЈ ЃЉ

A.ЧњЯпЂђЖдгІЕФЬѕМўИФБфЪЧдіДѓбЙЧП
B.T2ЁцЪБ,ЩЯЪіЗДгІЦНКтГЃЪ§ЮЊ0.42,дђT2ЃОT1
C.дкT1Ёц,ШєЦ№ЪМЪБЯђШнЦїжаГфШы5 mol CO2ЁЂ5 mol H2ЁЂ5 mol CH3OH(g)КЭ5 mol H2O(g),дђДяЦНКтЧАv(е§)ЃОv(Фц)
D.дкT1Ёц,ШєЦ№ЪМЪБЯђШнЦїГфШы4.5 mol CO2ЁЂ6 mol H2,ЦНКтЪБШнЦїФкбЙЧПp=
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2014ИпПМЛЏбЇзЈЬтЭЛЦЦбЕСЗ зЈЬт5ЮяжЪНсЙЙ дЊЫижмЦкТЩСЗЯАОэЃЈНтЮіАцЃЉ ЬтаЭЃКбЁдёЬт
МзЁЂввЁЂБћЁЂЖЁЮЊЫФжжжїзхдЊЫи,вбжЊМзгыввЁЂБћЁЂЖЁШ§жждЊЫиЯрСк,МзЁЂввЕФдзгађЪ§жЎКЭЕШгкБћЕФдзгађЪ§,ЫФжждЊЫидзгЕФзюЭтВуЕчзгЪ§жЎКЭЮЊ20ЁЃЯТСаХаЖЯжае§ШЗЕФ
ЪЧЃЈ ЃЉ
A.дзгАыОЖ:БћЃОввЃОМз
B.зюЭтВуЕчзгЪ§:Бћ=ЖЁ
C.ЦјЬЌЧтЛЏЮяЕФЮШЖЈад:МзЃОБћ
D.зюИпМлбѕЛЏЮяЖдгІЕФЫЎЛЏЮяЕФЫсад:ЖЁЃОМз
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2014ИпПМЛЏбЇзЈЬтЭЛЦЦбЕСЗ зЈЬт4ЛЏбЇЗДгІжаЕФФмСПБфЛЏСЗЯАОэЃЈНтЮіАцЃЉ ЬтаЭЃКЬюПеЬт
(1)аТЕФЁЖЛЗОГПеЦјжЪСПБъзМЁЗ(GB 3095 2012)НЋгк2016Фъ1дТ1ШедкЮвЙњШЋУцЪЕЪЉЁЃОнДЫ,ЛЗОГПеЦјжЪСПжИЪ§(AQI)ШеБЈКЭЪЕЪББЈИцАќРЈСЫSO2ЁЂNO2ЁЂCOЁЂO3ЁЂPM10ЁЂPM2.5ЕШжИБъ,ЮЊЙЋжкЬсЙЉНЁПЕжИв§,в§ЕМЕБЕиОгУёКЯРэАВХХГіааКЭЩњЛюЁЃ
2012)НЋгк2016Фъ1дТ1ШедкЮвЙњШЋУцЪЕЪЉЁЃОнДЫ,ЛЗОГПеЦјжЪСПжИЪ§(AQI)ШеБЈКЭЪЕЪББЈИцАќРЈСЫSO2ЁЂNO2ЁЂCOЁЂO3ЁЂPM10ЁЂPM2.5ЕШжИБъ,ЮЊЙЋжкЬсЙЉНЁПЕжИв§,в§ЕМЕБЕиОгУёКЯРэАВХХГіааКЭЩњЛюЁЃ
ЂйЦћГЕХХГіЕФЮВЦјжаКЌгаCOКЭNOЕШЦјЬх,гУЛЏбЇЗНГЬЪННтЪЭВњЩњNOЕФдвђ ЁЃ
ЂкЦћГЕХХЦјЙмФкАВзАЕФДпЛЏзЊЛЏЦї,ПЩЪЙЦћГЕЮВЦјжаЕФжївЊЮлШОЮязЊЛЏЮЊЮоЖОЕФДѓЦјбЛЗЮяжЪЁЃвбжЊ:
N2(g)+O2(g)=2NO(g) ІЄH=+180.5 kJ/mol
2C(s)+O2(g)=2CO(g) ІЄH=-221.0 kJ/mol
C(s)+O2(g)=CO2(g) ІЄH=-393.5 kJ/mol
дђЗДгІ2NO(g)+2CO(g)=N2(g)+2CO2(g)ЕФІЄH= kJ/molЁЃ
(2)жБНгХХЗХЕЊбѕЛЏЮяЛсаЮГЩЫсгъЁЂЮэіВ,ДпЛЏЛЙдЗЈКЭбѕЛЏЮќЪеЗЈЪЧГЃгУЕФДІРэЗНЗЈЁЃРћгУNH3КЭCH4ЕШЦјЬхГ§ШЅбЬЦјжаЕФЕЊбѕЛЏЮяЁЃвбжЊ:CH4(g)+2O2(g)=CO2(g)+2H2O(l) ІЄH1=a kJ/mol;гћМЦЫуЗДгІCH4(g)+4NO(g)=CO2(g)+2H2O(l)+2N2(g)ЕФьЪБфІЄH2дђЛЙашвЊВщбЏФГЗДгІЕФьЪБфІЄH3,ЕБЗДгІжаИїЮяжЪЕФЛЏбЇМЦСПЪ§жЎБШЮЊзюМђећЪ§БШЪБ,ІЄH3=b kJ/mol,ИУЗДгІЕФШШЛЏбЇЗНГЬЪНЪЧ ,ОнДЫМЦЫуГіІЄH2= kJ/mol(гУКЌaЁЂbЕФЪНзгБэЪО)ЁЃ
(3)ЯТБэСаГіСЫЙЄвЕЩЯЮќЪеSO2ЕФШ§жжЗНЗЈЁЃ
ЗНЗЈЂё | гУАБЫЎНЋSO2зЊЛЏ(NH4)2SO3,дйбѕЛЏГЩ(NH4)2SO4 |
ЗНЗЈЂђ | гУЩњЮяжЪШШНтЦј(жївЊГЩЗжCOЁЂCH4ЁЂH2)НЋSO2дкИпЮТЯТЛЙдГЩЕЅжЪСђ |
ЗНЗЈЂѓ | гУNa2SO3ШмвКЮќЪеSO2,дйОЕчНтзЊЛЏЮЊH2SO4 |
ЗНЗЈЂђжївЊЗЂЩњСЫЯТСаЗДгІ:
2CO(g)+SO2(g)=S(g)+2CO2(g) ІЄH=+8.0 kJ/mol
2H2(g)+SO2(g)=S(g)+2H2O(g)ІЄH=+90.4 kJ/mol
2CO(g)+O2(g)=2CO2(g) ІЄH=-566.0 kJ/mol
2H2(g)+O2(g)=2H2O(g) ІЄH=-483.6 kJ/mol
дђS(g)гыO2(g)ЗДгІЩњГЩSO2(g)ЕФШШЛЏбЇЗНГЬЪНПЩБэЪОЮЊ ЁЃ
(4)КЯГЩАБгУЕФЧтЦјПЩвдМзЭщЮЊдСЯжЦЕУЁЃгаЙиЛЏбЇЗДгІЕФФмСПБфЛЏШчЭМЫљЪО,дђCH4(g)гыH2O(g)ЗДгІЩњГЩCO(g)КЭH2(g)ЕФШШЛЏбЇЗНГЬЪНЮЊ ЁЃ

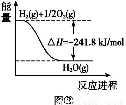
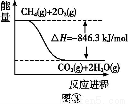
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2014ИпПМЛЏбЇзЈЬтЭЛЦЦбЕСЗ зЈЬт3бѕЛЏЛЙдЗДгІ РызгЗДгІСЗЯАОэЃЈНтЮіАцЃЉ ЬтаЭЃКбЁдёЬт
дкШлШкKOHжа,ДѓЦјжаЕФбѕПЩНЋИѕЬњПѓЃЈFeCr2O4ЃЉжаFeКЭCrЕФЛЏКЯМлЖМзЊЛЏЮЊ+6Мл,бѕЛЏ1 mol FeCr2O4дкРэТлЩЯашвЊбѕЦјЃЈ ЃЉ
A.2 mol B.2.5 mol C.3 mol D.4 mol
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2014ИпПМЛЏбЇзЈЬтЭЛЦЦбЕСЗ зЈЬт13ЮяжЪНсЙЙгыаджЪбЁао3СЗЯАОэЃЈНтЮіАцЃЉ ЬтаЭЃКЬюПеЬт
вЛЫЎСђЫсЫФАБКЯЭ(Ђђ)([Cu(NH3)4]SO4ЁЄH2O)ЪЧвЛжжживЊЕФШОСЯМАХЉвЉжаМфЬхЁЃЧыЛиД№ЯТСаЯрЙиЮЪЬт:
(1)CuЕФКЫЭтЕчзгХХВМЪНЮЊ ЁЃ
(2)NЕФLВужага ЖдГЩЖдЕчзг;N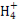 СЂЬхЙЙаЭЪЧ ,ЦфжааФдзгЕФдгЛЏЗНЪНЮЊ ЁЃ
СЂЬхЙЙаЭЪЧ ,ЦфжааФдзгЕФдгЛЏЗНЪНЮЊ ЁЃ
(3)АБЫЎШмвКжаДцдкЖржжЧтМќ,ШЮБэЪОГіЦфжаСНжж ;
(4)[Cu(NH3)4]SO4ЁЄH2OжаГЪЩюРЖЩЋЕФРызгЪЧ ,ИУЮЂСЃжаЕФЁАЕчзгЖдИјгшвЛНгЪмМќЁБЪєгк Мќ;
(5)CuЕФвЛжжТШЛЏЮяОЇАћНсЙЙШчЭМЫљЪО,ИУТШЛЏЮяЕФЛЏбЇЪН ЁЃ
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com