
| A | B | C | D | |
| �о�Ŀ�� | ѹǿ�Է�Ӧ��Ӱ�죨P2��P1�� | �¶ȶԷ�Ӧ��Ӱ�� | ƽ����ϵ����N2�Է�Ӧ��Ӱ�� | �����Է�Ӧ��Ӱ�� |
| ͼʾ | 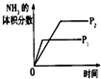 | 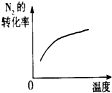 | 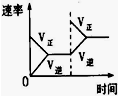 | 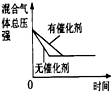 |
���� ��1���÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ�������¶�ƽ�������ƶ������û�з�Ӧ��ƽ��Ħ������=$\frac{0.2mol��28g/mol+0.6mol��2g/mol}{0.6mol+0.2mol}$�������ȫ��Ӧ��Ħ������Ϊ����Ħ��������
��2�����淴Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ���Ӧ��ϵ�и����ʵ����ʵ��������ʵ���Ũ�ȡ��ٷֺ����Լ��ɴ������һϵ�����������䣻
����0.2mol��������0.1mol������ƽ����Ӧ����v��N2��=$\frac{\frac{��n}{V}}{��t}$��
��3��A������ѹǿ����ѧ��Ӧ��������Ӧ����ƽ���ʱ�����̣�ƽ�������ƶ��������������������
B�������¶ȣ�ƽ�������ƶ���������ת���ʽ��ͣ�
C������Ӧ��Ũ��˲������Ӧ���������淴Ӧ���ʲ��䣬ƽ�������ƶ���
D�������ı仯ѧ��Ӧ���ʣ�����Ӱ��ƽ���ƶ���
��4����������¶�ƽ�������ƶ�����������¶�ƽ�������ƶ���
����ѹǿƽ�������������С�ķ����ƶ���
��� �⣺��1���÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ�������¶�ƽ�������ƶ�����ѧƽ�ⳣ����С�����Ը÷�Ӧ450���ƽ�ⳣ����500��ʱ��ƽ�ⳣ�������û�з�Ӧ��ƽ��Ħ������=$\frac{0.2mol��28g/mol+0.6mol��2g/mol}{0.6mol+0.2mol}$=8.5g/mol�������ȫ��Ӧ��Ħ������Ϊ����Ħ��������17g/mol��ʵ���ϻ������Ħ�������ڶ���֮�䣬������8.5g/mol��С��17g/mol��Ħ����������ֵ�ϵ�������Է���������������ƽ��ʽ����ΧΪ8.5��ƽ��ʽ����17��
�ʴ�Ϊ������8.5��ƽ��ʽ����17��
��2��A��2V����H2��=3V����NH3��ʱ��Ӧ�ﵽƽ��״̬�����Ե�3V����H2��=2V����NH3��ʱû�дﵽƽ��״̬���ʴ���
B����Ӧǰ�����������������䡢���ʵ�����С����Ӧǰ��������ƽ�ַ��������������������ƽ������������ʱ����仯ʱ���淴Ӧ������ȣ���Ӧ�ﵽƽ��״̬������ȷ��
C�����۷�Ӧ�Ƿ�ﵽƽ��״̬��������������ܶȲ���ʱ��仯�����Բ��ܾݴ��ж�ƽ��״̬���ʴ���
D����Ӧǰ���������ʵ�����С����������С��������������ķ�����������ʱ����仯ʱ�����淴Ӧ������ȣ���Ӧ�ﵽƽ��״̬������ȷ��
��ѡBD��
����0.2mol��������0.1mol������ƽ����Ӧ����v��N2��=$\frac{\frac{��n}{V}}{��t}$=$\frac{\frac{0.2mol}{2L}}{5min}$=0.02mol/��L��min����
�ʴ�Ϊ��BD��0.02��
��3��A������ѹǿ����ѧ��Ӧ��������Ӧ����ƽ���ʱ�����̣�ƽ�������ƶ������������������������ͼ���ϣ���A����
B�������¶ȣ�ƽ�������ƶ���������ת���ʽ��ͣ�����ͼ���ϣ���B����
C������Ӧ��Ũ��˲������Ӧ���������淴Ӧ���ʲ��䣬ƽ�������ƶ���ͼ����ϣ���C��ȷ��
D�������ı仯ѧ��Ӧ���ʣ�����Ӱ��ƽ���ƶ���ͼ���ϣ���D����
��ѡC��
��4����������¶�ƽ�������ƶ�������Ũ�ȴ���0��С��0.10mol/L��
��������¶�ƽ�������ƶ�������Ũ�ȴ���0.10mol/L��С��0.20mol/L��
������Ũ�Ȳ�������AC��
�ڵ�5����ĩ�����������������䣬������ͨ��0.2mol��N2��0.6mol��H2���൱������ѹǿ������ѹǿƽ�������������С�ķ����ƶ�����������Ӧ�����ƶ���
�ʴ�Ϊ��AC��������Ӧ����
���� ���⿼�黯ѧƽ����㡢��ѧƽ���ƶ�Ӱ�����ء���ѧƽ��״̬�жϵ�֪ʶ�㣬���ؿ���ѧ�������жϡ����㼰֪ʶ�������������ע�⣨4��ƽ���������뵪�����������Ե�ЧΪ����ѹǿ����Ŀ�ѶȲ���


 ������ϰ�ο����뵥Ԫ���ϵ�д�
������ϰ�ο����뵥Ԫ���ϵ�д� �����Ծ���ĩ���100��ϵ�д�
�����Ծ���ĩ���100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���� | B�� | �ױ� | C�� | CH2=CH-CN | D�� | �����ϩ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��ѧ�� | ���� | ��ѧ�� | ���� | ��ѧ�� | ���� |
| H-H | 436 | C-F | 427 | H-S | 339 |
| S=S | 255 | C-C1 | 330 | H-F | 565 |
| C1-C1 | 243 | C-I | 218 | H-C1 | 431 |
| O=O | �� | H-O | 464 | H-Br | 366 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
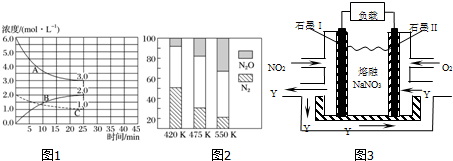
 һ�������£���Ӧ2NH3��g��?N2��g��+3H2��g���ﵽƽ��ʱN2������������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ�������
һ�������£���Ӧ2NH3��g��?N2��g��+3H2��g���ﵽƽ��ʱN2������������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ�������| A�� | ѹǿ��p1��p2 | B�� | b��c�����Ӧ��ƽ�ⳣ����Kc��Kb | ||
| C�� | a�㣺2v��NH3�����T3v��H2���� | D�� | a�㣺NH3��ת����Ϊ$\frac{1}{3}$ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| t/K | 300 | 400 | 500 | �� |
| K/��mol•L-1��2 | 4��106 | 8��107 | K1 | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
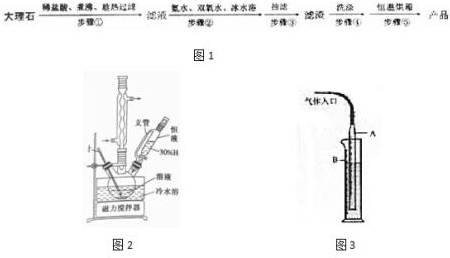
| �ⶨ���� | �ռ�ǰ����/mL | �ռ������/mL |
| ��1�� | 21.06 | 4.24 |
| ��2�� | 23.52 | 6.72 |
| ��3�� | 22.41 | 5.63 |
| ��4�� | 20.80 | 7.20 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ֻ��һ��Ԫ�ص�����һ���ǵ��� | B�� | ֻ��һ�ַ��ӵ�����һ�������� | ||
| C�� | �ǽ���������һ�������������� | D�� | �е������ɵķ�Ӧһ�����û���Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaOH��HCl ��Ӧ | B�� | CO��O2��ȼ | ||
| C�� | Ba��OH��2•8H2O��NH4NO3��Ӧ | D�� | SO3��H2O��Ӧ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com