
【题目】化学平衡常数![]() 、电离常数
、电离常数![]() 、
、![]() 、溶度积常数
、溶度积常数![]() 等常数是表示判断物质性质的重要常数,下列关于这些常数的说法中,正确的是
等常数是表示判断物质性质的重要常数,下列关于这些常数的说法中,正确的是![]()
![]()
A.当温度升高时,弱酸、弱碱的电离常数![]() 、
、![]() 均变小
均变小
B.![]() 说明等物质的量浓度的氢氰酸酸性比醋酸强
说明等物质的量浓度的氢氰酸酸性比醋酸强
C.向氯化钡溶液中加入等体积等浓度的碳酸钠和硫酸钠溶液,先产生![]() 沉淀,则
沉淀,则![]()
D.化学平衡常数的大小与温度、浓度、压强有关,与催化剂无关
【答案】C
【解析】
A.弱电解质电离是吸热的,升高温度促进弱电解质电离,所以当温度升高时,促进弱酸、弱碱电离,则弱酸、弱碱的电离常数(Ka、Kb)均变大,故A错误;
B.弱酸的电离平衡常数越大,说明该酸的电离程度越大,则该酸的酸性越强,Ka(HCN)<Ka(CH3COOH)说明相同物质的量浓度时,说明HCN电离程度小于醋酸,所以氢氰酸的酸性比醋酸的弱,故B错误;
C.溶度积常数小的物质先生成沉淀,向氯化钡溶液中加入等体积同浓度的碳酸钠和硫酸钠溶液,先产生BaSO4沉淀,则Ksp(BaSO4)<Ksp(BaCO3),故C正确;
D.化学平衡常数只与温度有关,与温度、压强、催化剂都无关,故D错误;
故选C。


科目:高中化学 来源: 题型:
【题目】常温下pH均为2的两种酸溶液X和Y各10 mL分别加水稀释到10000 mL,其pH与所加水的体积变化如图所示,下列结论中正确的是

A.加水后,Y酸的电离度增大
B.X酸在水溶液中存在电离平衡
C.加水后,X酸的电离平衡常数减小
D.X酸的物质的量浓度与Y酸的物质的量浓度相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在t℃时AgBr在水中的沉淀溶解平衡曲线如图所示。t℃时AgCl的Ksp=4×10-10,下列说法不正确的是
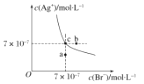
A.在t℃时,AgBr 的 Ksp为4.9×10-13
B.在 t ℃时,AgCl(s)+Br-(aq)![]() AgBr(s)+Cl-(aq)的平衡常数 K≈816
AgBr(s)+Cl-(aq)的平衡常数 K≈816
C.图中a点对应的是AgBr的不饱和溶液
D.在 AgBr 饱和溶液中加入NaBr固体,可使溶液由c点变到b点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,![]() 和
和![]() 两种酸溶液,起始时溶液体积均为
两种酸溶液,起始时溶液体积均为![]() 。分别向两溶液中加水进行稀释,稀释后溶液的体积为V,溶液pH随
。分别向两溶液中加水进行稀释,稀释后溶液的体积为V,溶液pH随![]() 的变化如图所示。下列说法正确的是
的变化如图所示。下列说法正确的是

A.等物质的量浓度的![]() 和
和![]() 溶液中,后者水的电离程度大
溶液中,后者水的电离程度大
B.当稀释至![]() 时,等体积的两种酸中和
时,等体积的两种酸中和![]()
C.当两溶液均稀释至![]() 时,溶液中:
时,溶液中:![]()
D.![]() 的电离方程式:
的电离方程式:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于电解质溶液下列说法中不正确的是
A.向浓度均为![]() 混合溶液中逐滴加入氨水,先生成蓝色
混合溶液中逐滴加入氨水,先生成蓝色![]() 沉淀,则
沉淀,则![]()
B.用等浓度的NaOH溶液中和等体积pH=2与pH=3的醋酸,所消耗的NaOH溶液的体积前者是后者的10倍
C.由![]() 溶液等体积混合,其离子浓度的顺序为:
溶液等体积混合,其离子浓度的顺序为:![]()
D.某温度下纯水中![]() ,则该温度下0.1mol/L的盐酸的pH=1
,则该温度下0.1mol/L的盐酸的pH=1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】t℃时,卤化银(AgX,X=Cl,Br)的2条溶解平衡曲线如图所示,已知AgCl,AgBr的Ksp依次减小,且p(Ag+)=-lgc(Ag+),p(X-)=-lgc(X-),利用pX-pAg的坐标系可表示出AgX的溶度积与溶液中的c(Ag+)和c(X-)的相互关系.下列说法错误的是
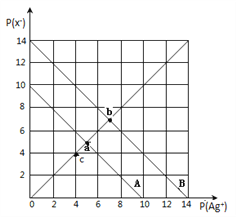
A. t℃时,c点可表示AgCl的不饱和溶液
B. B线表示的是AgBr
C. 取a、b两点处溶液等体积混合,维持t℃不变,混合溶液中一定无白色沉淀生成
D. 在t℃时,AgCl(s)+Br-(aq)![]() AgBr(s)+Cl-(aq)平衡常数K≈104
AgBr(s)+Cl-(aq)平衡常数K≈104
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.锅炉水垢中的![]() 经饱和碳酸钠溶液浸泡可转化为
经饱和碳酸钠溶液浸泡可转化为![]()
B.常温下,在含有![]() 和
和![]() 的溶液中,
的溶液中,![]() 和
和![]() 浓度之积是个常数
浓度之积是个常数
C.当醋酸达到电离平衡后,改变某条件电离平衡向正反应方向移动,则溶液的导电能力一定变强
D.将浓度为![]()
![]() 的HF溶液加水不断稀释,溶液
的HF溶液加水不断稀释,溶液![]() 始终保持增大
始终保持增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钾的冶炼可采用如下方法:2KF+CaC2![]() CaF2+2K↑+2C,下列有关说法合理的是( )
CaF2+2K↑+2C,下列有关说法合理的是( )
A.该反应的氧化剂是KF,氧化产物是K
B.该反应能说明C的还原性大于K
C.电解KF溶液不可能制备金属钾
D.CaC2、CaF2均为离子化合物,且阴、阳离子个数比均为2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应2SO2(g)+O2(g)![]() 2SO3(g)△H<0,在一定条件下达到平衡状态,时间为t1时改变条件.化学反应速率与反应时间的关系如图所示.下列说法正确的是( )
2SO3(g)△H<0,在一定条件下达到平衡状态,时间为t1时改变条件.化学反应速率与反应时间的关系如图所示.下列说法正确的是( )

A. 维持温度、容积不变,t1时充入SO3(g)
B. 维持压强不变,t1时升高反应体系温度
C. 维持温度、容积不变,t1时充入一定量Ar
D. 维持温度、压强不变,t1时充入SO3(g)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com