
| A、氧化性:Ag+>Cu2+>Zn2+ |
| B、溶液中Cu2+与Fe2+的物质的量之比为1:1 |
| C、Ag+的最先与Fe反应 |
| D、1molFe可还原1molCu2+ |
| 0.1mol×1 |
| 2 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、Cu2+、K+、Cl-、NO3- |
| B、Ag+、Na+、Cl-、NO3- |
| C、Mg2+、Al3+、SO42-、Cl- |
| D、Ba2+、NH4+、Cl-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
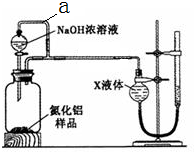 氮化铝(AlN)是一种新型无机材料.
氮化铝(AlN)是一种新型无机材料.样品 m1g |
| 过量NaOH溶液 |
| ① |
| 过量CO2 |
| ② |
| 过滤、洗涤 |
| ③ |
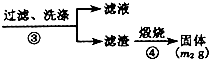
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
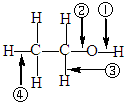
| A、与醋酸、浓硫酸共热时,②键断裂 |
| B、与金属钠反应时,①键断裂 |
| C、与浓硫酸共热至170℃时,②、④键断裂 |
| D、在Ag催化下与O2反应时,①、③键断裂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、PH3、sp2平面三角形 |
| B、SO32-、sp2 平面三角形 |
| C、NO3-、sp3 三角锥形 |
| D、SO2、sp2V形 |
查看答案和解析>>
科目:高中化学 来源: 题型:
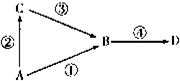 A、B、C、D均为中学常见物质,其中A为单质,B、C、D为化台物,并且存在如下转化关系:试回答下列问题:
A、B、C、D均为中学常见物质,其中A为单质,B、C、D为化台物,并且存在如下转化关系:试回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com