
| 1 |
| 2 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、K=
| ||
B、K=
| ||
C、K=
| ||
D、K=
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧化性:Ag+>Cu2+>Zn2+ |
| B、溶液中Cu2+与Fe2+的物质的量之比为1:1 |
| C、Ag+的最先与Fe反应 |
| D、1molFe可还原1molCu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、60mL | B、90mL |
| C、120mL | D、150mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入AgNO3溶液,观察有无浅黄色沉淀 |
| B、加入NaOH溶液共热,滴入AgNO3溶液,观察有无淡黄色沉淀生成 |
| C、加入NaOH溶液共热,然后加稀硝酸呈酸性,再滴入AgNO3溶液,观察有无淡黄色沉淀生成 |
| D、加入NaOH、乙醇溶液共热,然后加稀硝酸呈酸性,再滴入AgNO3溶液,观察有无淡黄色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
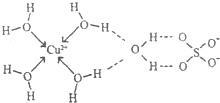 第四周期元素的单质及化合物在工农业生产中应用广泛.
第四周期元素的单质及化合物在工农业生产中应用广泛.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、聚二氧化碳塑料是合成高分子材料 |
| B、聚二氧化碳塑料与干冰互为同素异形体 |
| C、聚二氧化碳塑料的使用也会产生白色污染 |
| D、聚二氧化碳塑料与干冰是同一种物质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com