
【题目】恒容条件下,1 mol SiHCl3发生如下反应:2SiHCl3(g)![]() SiH2Cl2(g)+SiCl4(g)。已知:v正=v消耗(SiHCl3)=k正x2(SiHCl3),v逆=2v消耗(SiH2Cl2)=k逆x(SiH2Cl2)x(SiCl4),k正、k逆分别为正、逆向反应速率常数(仅与温度有关),x为物质的量分数。如图是不同温度下x(SiHCl3)随时间的变化。下列说法正确的是
SiH2Cl2(g)+SiCl4(g)。已知:v正=v消耗(SiHCl3)=k正x2(SiHCl3),v逆=2v消耗(SiH2Cl2)=k逆x(SiH2Cl2)x(SiCl4),k正、k逆分别为正、逆向反应速率常数(仅与温度有关),x为物质的量分数。如图是不同温度下x(SiHCl3)随时间的变化。下列说法正确的是

A. 该反应为放热反应,v正,a<v逆,b
B. T1 K时平衡体系中可通过移走SiCl4提高SiHCl3的转化率
C. 当反应进行到a处时,v正/v逆=16/9
D. T2 K时平衡体系中再充入1 mol SiHCl3,平衡正向移动,x(SiH2Cl2)增大
【答案】BC
【解析】
A.因两曲线对应的状态只是温度不同,由图像知达到平衡所需时间T2K大于T1K,温度越高反应速率越快,所以温度T2>T1。又T2K下达到平衡时SiHCl3的物质的量分数比T1K平衡时小,说明升温平衡向正反应方向移动,由此推知该反应为吸热反应,A项错误;
B.从平衡体系中移走SiCl4,即减小生成物浓度,根据勒夏特列原理知,平衡将向正反应方向移动,反应物的转化率提高,B项正确;
C. 2SiHCl3(g)![]() SiH2Cl2(g)+SiCl4(g)反应前后分子数不变,即反应开始至达平衡的过程中混合气体总物质的量始终为1mol,由图像知T2K下达到平衡时SiHCl3的物质的量分数为0.75,则此时SiH2Cl2和SiCl4的物质的量分数均为0.125,因为平衡时V正=V逆,V正=k正x2(SiHCl3)=0.752k正,V逆=k逆x(SiH2Cl2)x(SiCl4)=0.1252k逆,则0.752k正=0.1252k逆,
SiH2Cl2(g)+SiCl4(g)反应前后分子数不变,即反应开始至达平衡的过程中混合气体总物质的量始终为1mol,由图像知T2K下达到平衡时SiHCl3的物质的量分数为0.75,则此时SiH2Cl2和SiCl4的物质的量分数均为0.125,因为平衡时V正=V逆,V正=k正x2(SiHCl3)=0.752k正,V逆=k逆x(SiH2Cl2)x(SiCl4)=0.1252k逆,则0.752k正=0.1252k逆,![]() =
=![]() =
=![]() ,因k正和k逆只与温度有关,反应进行到a点处时V正= k正x2(SiHCl3)=0.82k正,V逆= k逆x(SiH2Cl2)x(SiCl4)=0.12k逆。
,因k正和k逆只与温度有关,反应进行到a点处时V正= k正x2(SiHCl3)=0.82k正,V逆= k逆x(SiH2Cl2)x(SiCl4)=0.12k逆。![]() =
=![]() ×
×![]() =
=![]() ×
×![]() =
=![]() 。C项正确;
。C项正确;
D.恒容条件下再充入1molSiHCl3,相当于增大压强,而2SiHCl3(g)![]() SiH2Cl2(g)+SiCl4(g)反应前后气体体积不变,所以平衡不移动,x(SiH2Cl2)不变,D项错误;答案选BC。
SiH2Cl2(g)+SiCl4(g)反应前后气体体积不变,所以平衡不移动,x(SiH2Cl2)不变,D项错误;答案选BC。


 快捷英语周周练系列答案
快捷英语周周练系列答案科目:高中化学 来源: 题型:
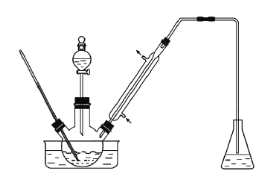
【题目】下图是一个实验室制取氯气并以氯气为原料进行一系列反应的装置,回答下列问题。(已知:①MnO2+4HCl(浓) ![]() MnCl2+2H2O+Cl2↑,②Cl2+SO2+2H2O=2HCl+H2SO4,③ Ba(OH)2+CO2=BaCO3↓+H2O)
MnCl2+2H2O+Cl2↑,②Cl2+SO2+2H2O=2HCl+H2SO4,③ Ba(OH)2+CO2=BaCO3↓+H2O)

(1)写出a仪器的名称___;
(2)装置D产生白色沉淀现象的原因___________;
(3)E装置的硬质玻璃管内盛有碳粉,发生氧化还原反应,其产物为CO2和HCl。试写出E中反应的化学方程式_______;
(4)F处的烧杯溶液中最终___(填“有”或“没有”)白色沉淀;
(5)F装置无法确认E处反应中有CO2产生,为了证明CO2的存在,要对F装置进行改造,下列装置符合要求的是___。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H是治疗关节炎等疼痛药物的主要成分,其合成路线如图所示:

请回答下列问题:
(1)F中的官能团名称为_____。
(2)D的结构简式为_____。
(3)①~⑦的7个反应中,反应类型属于取代反应的有_____(填反应序号)。
(4)写出B→C反应的化学方程式_____。
(5)芳香化合物X是E的同分异构体,能发生水解反应,且酸性水解产物遇FeCl3溶液显紫色,X可能的结构共有_____种,写出其中一种有机物的结构简式,其核磁共振氢谐显示有4种不同化学环境氢_____。
(6)参考上述合成路线,写出用![]() 为原料制备
为原料制备 的合成路线(无机试剂任选)。___________________
的合成路线(无机试剂任选)。___________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“除氢气外,烃、肼、甲醇、氨、煤气等液体或气体,均可作燃料电池的燃料”。已知肼燃烧时发生下列反应,N2H4+O2![]() N2+2H2O。以Pt为电极,以硫酸为电解质溶液组成肼燃料电池,下列关于肼燃料电池的说法中不正确是 )
N2+2H2O。以Pt为电极,以硫酸为电解质溶液组成肼燃料电池,下列关于肼燃料电池的说法中不正确是 )
A. 肼是燃料电池的负极反应物,O2是正极反应物
B. 肼燃料电池的正极反应为 O2 + 2H2O + 4e-= 4OH-
C. 肼燃料电池的负极反应为:N2H4 —4e—=N2↑+4H+
D. 电池工作过程中H+向正极移动,但H+物质的量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室以苯甲醛为原料制备间溴苯甲醛(实验装置见下图,相关物质的沸点见附表)。
物质 | 沸点/℃ | 物质 | 沸点/℃ |
溴 | 58.8 | 1,2-二氯乙烷 | 83.5 |
苯甲醛 | 179 | 间溴苯甲醛 | 229 |
其实验步骤为:
步骤1:将三颈瓶中的一定配比的无水AlCl3、1,2-二氯乙烷和苯甲醛充分混合后,升温至60℃,缓慢滴加经浓硫酸干燥过的液溴,保温反应一段时间,冷却。
步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液。有机相用10%NaHCO3溶液洗涤。
步骤3:经洗涤的有机相加入适量无水MgSO4固体,放置一段时间后过滤。
步骤4:减压蒸馏有机相,收集相应馏分。
(1) 实验装置中冷凝管的主要作用是___________________。
(2) 步骤1所加入的物质中,有一种物质是催化剂,其化学式为__________________
(3) 写出由苯甲醛制取间溴苯甲醛的化学方程式_____________________________________________________
(4) 为防止污染环境,锥形瓶中盛装的溶液应该是______________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含MgCl2、KCl、Na2SO4三种溶质的混合液中,已知其中含Cl-1.5mol,K+和Na+共1.5mol,Mg2+为0.5mol,则SO42-的物质的量为
A. 0.2molB. 0.5molC. 0.25molD. 0.15mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列与有机物的结构、性质的有关叙述中正确的是
A. 苯既能发生取代反应,又能发生加成反应
B. 乙烯、甲烷、聚乙烯均可使酸性高锰酸钾溶液褪色
C. 分馏、干馏都是物理变化,裂化、裂解都是化学变化
D. 纤维素、聚乙烯、油脂都属于高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向盛有50 mL pH=3的HA溶液的绝热容器中加入pH=14的NaOH溶液,加入NaOH溶液的体积(V)与所得混合溶液的温度(T)的关系如图所示。下列叙述正确的是( )

A. HA溶液的物质的量浓度为0.0l mol/L
B. a→b的过程中,混合溶液不可能存在:c(A-)=c(Na+)
C. b→c的过程中,温度降低的主要原因是溶液中A-发生了水解反应
D. 25℃时,HA的电离平衡常数K约为1.25×10—6
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com