
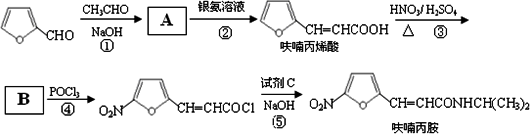
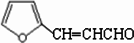 ;
;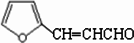 与银氨溶液反应生成呋喃丙烯酸,呋喃丙烯酸与硝酸在浓硫酸作用下反应生成B:
与银氨溶液反应生成呋喃丙烯酸,呋喃丙烯酸与硝酸在浓硫酸作用下反应生成B: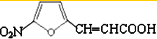 ,反应③方程式为:
,反应③方程式为: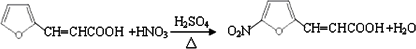 ;
; 与POCl3反应生成
与POCl3反应生成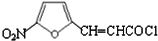 ,
, 与H2NCH(CH3)2反应生成呋喃丙胺:
与H2NCH(CH3)2反应生成呋喃丙胺: ,据此进行解答.
,据此进行解答.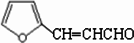 ;
;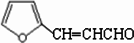 与银氨溶液反应生成呋喃丙烯酸:
与银氨溶液反应生成呋喃丙烯酸: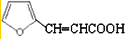 ,呋喃丙烯酸与硝酸在浓硫酸作用下反应生成B:
,呋喃丙烯酸与硝酸在浓硫酸作用下反应生成B: ,反应③方程式为:
,反应③方程式为: ;
; 与POCl3反应生成
与POCl3反应生成 ,
, 与H2NCH(CH3)2反应生成呋喃丙胺,
与H2NCH(CH3)2反应生成呋喃丙胺,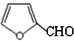 转化成
转化成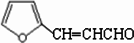 的反应①为加成反应和消去反应;
的反应①为加成反应和消去反应;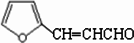 与银氨溶液的反应为氧化反应;
与银氨溶液的反应为氧化反应; 为取代反应;
为取代反应; 与POCl3反应生成
与POCl3反应生成 ,该反应为取代反应;
,该反应为取代反应; 为取代反应,
为取代反应, ,其分子中含有4种位置不同的H原子,则其核磁共振氢谱中含有4个吸收峰,每种H原子的数目都为1,则各吸收峰的面积比为1:1:1:1,
,其分子中含有4种位置不同的H原子,则其核磁共振氢谱中含有4个吸收峰,每种H原子的数目都为1,则各吸收峰的面积比为1:1:1:1,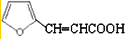 )具有多种同分异构体,呋喃丙烯酸中含有1个环、3个碳碳双键、1个碳氧双键,其不饱和度为:1+3+1=5,含有7个C原子,形成的有机物中属于醛类且含有酚羟基的同分异构体中,苯环的不饱和度为4,醛基的不饱和度为1,即:满足条件的有机物分子中含有1个苯环、1个醛基、2个酚羟基,①两个羟基在苯环的邻位碳上时,如图:
)具有多种同分异构体,呋喃丙烯酸中含有1个环、3个碳碳双键、1个碳氧双键,其不饱和度为:1+3+1=5,含有7个C原子,形成的有机物中属于醛类且含有酚羟基的同分异构体中,苯环的不饱和度为4,醛基的不饱和度为1,即:满足条件的有机物分子中含有1个苯环、1个醛基、2个酚羟基,①两个羟基在苯环的邻位碳上时,如图: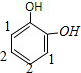 ,醛基可以在1、2号C,存在两种同分异构体;②两个羟基在间位C原子上时,如图:
,醛基可以在1、2号C,存在两种同分异构体;②两个羟基在间位C原子上时,如图: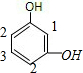 ,醛基可以在1、2、3号C上,存在3种同分异构体;③两个羟基中苯环的对位C上时,如图:
,醛基可以在1、2、3号C上,存在3种同分异构体;③两个羟基中苯环的对位C上时,如图: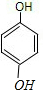 ,苯环上的4个H原子位置等效,只存在1种同分异构体,所以总共含有6种满足条件的结构,
,苯环上的4个H原子位置等效,只存在1种同分异构体,所以总共含有6种满足条件的结构, ,反应的化学方程式为:
,反应的化学方程式为: ,
, ;
;

 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 随着氮氧化物污染的日趋严重,国家将于“十二五”期间加大对氮氧化的排放的控制力度.消除氮氧化物污染有多种方法,其中一种是用活性炭还原法处理氮氧化物,有关反应为:C(s)+2NO(g)?N2(g)+CO2(g)△H>0.
随着氮氧化物污染的日趋严重,国家将于“十二五”期间加大对氮氧化的排放的控制力度.消除氮氧化物污染有多种方法,其中一种是用活性炭还原法处理氮氧化物,有关反应为:C(s)+2NO(g)?N2(g)+CO2(g)△H>0.| 时间/min | 0 | 20 | 40 | 50 |
| c(NO)/mol?L-1 | 0.100 | 0.040 | 0.032 | 0.032 |
| c(N2)/mol?L-1 | 0 | 0.030 | 0.034 | 0.034 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

| 实验操作 | 实验现象及结论 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、可用酸性高锰酸钾溶液检验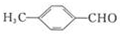 中的醛基 中的醛基 |
| B、可用新制的银氨溶液鉴别乙酸甲酯和乙醛 |
| C、能用一种试剂区分葡萄糖溶液、甘油、醋酸福尔马林等4种溶液 |
| D、1-戊炔和裂化汽油都能是溴水褪色,且褪色原理相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com