
【题目】同温同压下相等质量的SO2气体和CO2气体,下列有关比较的叙述中,正确的是( )
①分子数之比为11:16 ②体积比为16:11
③密度比为16:11 ④体积比为1:1.
A. ①③B. ②④C. ②③D. ①④
科目:高中化学 来源: 题型:
【题目】下列关于物质的量浓度表述正确的是( )
A.0.3 mol?L﹣1的Na2SO4溶液中含有的Na+和SO ![]() 的总物质的量为0.9 mol
的总物质的量为0.9 mol
B.当1 L水吸收22.4 L氨气时所得氨水的浓度不是1 mol?L﹣1 , 只有当22.4 L氨气溶于水制得1 L氨水时,其浓度才是1 mol?L﹣1
C.在K2SO4和NaCl的中性混合水溶液中,如果Na+和SO42﹣的物质的量相等,则K+和Cl﹣的物质的量浓度一定相同
D.10℃时,0.35 mol?L﹣1的KCl饱和溶液100 mL蒸发掉5 g水,冷却到10℃时,其体积小于100 mL,它的物质的量浓度仍为0.35 mol?L﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.所有卤代烃都难溶于水,且都是密度比水大的液体
B.所有卤代烃都是通过取代反应制得
C.卤代烃不属于烃类
D.卤代烃都可发生消去反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6 molL﹣1的H2SO4溶液中,乙同学将电极放入6 molL﹣1的NaOH溶液中,如图所示.
(1)写出甲中正极的电极反应式: .
(2)乙中负极为 , 总反应的离子方程式为 .
(3)如果甲同学与乙同学均认为“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出(填元素符号)的活动性更强,而乙会判断出(填写元素符号)的活动性更强.
(4)由此实验得出的下列结论中,正确的有(填字母).
A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质
B.镁的金属性不一定比铝的金属性强
C.该实验说明金属活动性顺序已过时,没有实用价值了
D.该实验说明化学研究对象复杂、反应受条件影响较大,因此应具体问题具体分析.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列各组化合物:
A.CH3CH2CH2CHO与 ![]()
B. ![]() 与
与 ![]()
C. ![]() 与
与 ![]()
D.CH3CH2C≡CH与CH2=CH﹣CH=CH2
E. ![]() 与
与 ![]()
F.戊烯和环戊烷
①属于同系物的有 , 属于同分异构体的有 .
②根据官能团的特点可将C中两化合物分别划分为类和类.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中能证明次氯酸是一种弱酸的是
A.次氯酸不稳定,易分解
B.次氯酸是一种强氧化剂
C.次氯酸钙能与碳酸作用生成碳酸钙和次氯酸
D.次氯酸能使染料和有机色质褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列框图中的物质均为中学化学中常见物质,其中甲、乙为单质,其余均为化合物.B为常见液态化合物,A为淡黄色固体,F、G所含元素相同且均为氯化物,G遇KSCN溶液显红色.
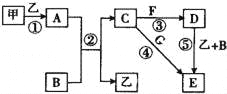
请回答下列问题:
(1)A是 .
(2)反应①~⑤中,属于氧化还原反应的是 填序号).
(3)反应⑤的化学方程式为 ;甲与B反应的离子方程式为 .
(4)在空气中将C溶液滴入F溶液中,观察到的现象是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平;②2CH3CHO+O2 ![]() 2CH3COOH.现以A为主要原料合成乙酸乙酯,其合成路线如图1所示.
2CH3COOH.现以A为主要原料合成乙酸乙酯,其合成路线如图1所示. 
乙酸乙酯的实验室和工业制法常采用如图2装置:回答下列问题:
(1)写出A的电子式 .
(2)B、D分子中的官能团名称分别、 .
(3)写出下列反应的反应类型:①② , ④ .
(4)写出下列反应的化学方程式:①②④
(5)制取乙酸乙酯浓H2SO4的作用是:① , ② . 欲提高乙酸的转化率,可采取的措施有、等.
(6)碳酸钠溶液的作用是 , 导气管不能插入液面以下,原因是 . 加热前,大试管中加入几粒碎瓷片的作用是 .
(7)实验室可用乙醇来制取乙烯,将生成的乙烯通入溴的四氯化碳溶液,反应后生成物的结构简式是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com