
【题目】“一酸两浸,两碱联合”法是实现粉煤灰(含SiO2、Al2O3、Fe2O3、CaO、MgO等)综合利用的新工艺。工业流程如下:

回答下列问题:
(1)聚合氯化铝铁(PAFC)化学式为[Al2(OH)nCl6-n]m·[Fe2(OH)xCl6-x]y,是一种新型高效的净水剂,PAFC中铁元素的化合价为___________。
(2)“一酸两浸”中的酸是________________(填结构式)。
(3)实际工业中“酸浸”、“碱浸”均不能充分反应,滤渣A中主要含有SiO2、Al2O3。“纯碱混合焙烧”中,它们分别发生反应的化学方程式为_____________、 ________________。
(4)“滤液B”的主要溶质有_____________(填化学式)。滤液混合后“蒸发”的作用是____________________________________。
(5)“电解”时的化学方程式________________________________。
【答案】 +3 H-Cl Na2CO3+SiO2![]() Na2SiO3+CO2↑ Na2CO3+Al2O3
Na2SiO3+CO2↑ Na2CO3+Al2O3![]() 2NaAlO2+CO2↑ AlCl3、NaCl 促进Al3+、Fe3+水解生成了聚合氯化铝铁(PAFC) 2NaCl+2H2O
2NaAlO2+CO2↑ AlCl3、NaCl 促进Al3+、Fe3+水解生成了聚合氯化铝铁(PAFC) 2NaCl+2H2O ![]() 2NaOH+Cl2↑+H2↑
2NaOH+Cl2↑+H2↑
【解析】(1)该物质是碱式氯化铝和碱式氯化铁形成的复杂物质,根据化合价规则,设铁元素的化合价为a,则有(6-x)+x=2a,所以铁元素的化合价为+3价;
(2)因最终产物为氯化物,所以该酸为盐酸,其结构式为H—Cl;
(3)SiO2和Al2O3在高温下都能与纯碱反应,类似于生产玻璃的主要反应原理:Na2CO3+ SiO2 ![]() Na2SiO3+CO2↑ 和Na2CO3 +Al2O3
Na2SiO3+CO2↑ 和Na2CO3 +Al2O3 ![]() 2NaAlO2+CO2↑;
2NaAlO2+CO2↑;
(4)根据滤渣A中主要含有SiO2和Al2O3,与纯碱焙烧后生成Na2SiO3和NaAlO2,再用盐酸酸浸后得到滤渣为H2SiO3,所以滤液B的主要溶质为AlCl3和NaCl;滤液混合后其中的溶质为AlCl3、FeCl3和NaCl,由于Al3+和Fe3+都能够水解,且加热能够促进水解,所以滤液混合后加热蒸发的作用就是促进Al3+、Fe3+水解生成聚合氯化铝铁(PAFC);
(5)分离出聚合氯化铝铁(PAFC)后的滤液中主要是NaCl,即粗盐,经过精制处理后,再进行电解,即氯碱工业,反应的化学方程式为2NaCl+2H2O ![]() 2NaOH+Cl2↑+H2↑。
2NaOH+Cl2↑+H2↑。


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
①标准状况下,0.2 mol任何物质的体积均为4.48 L ②若1 mol气体的体积为22.4 L,则它一定处于标准状况下 ③标准状况下,1 L HCl和1 L H2O的物质的量相同 ④标准状况下,1 g H2和14 g N2的体积相同 ⑤28 g CO的体积为22.4 L ⑥两种物质的物质的量相同,则它们在标准状况下的体积也相同 ⑦在同温同体积时,气体物质的物质的量越大,则压强越大 ⑧同温同压下,气体的密度与气体的相对分子质量成正比
A. ①②③④ B. ②③⑥⑦⑧ C. ⑤⑥⑦⑧ D. ④⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)请用双线桥法表示反应2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O化合价的升降和电子的转移情况,并回答下列问题:
标双线桥:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O_______。
该反应的氧化产物是________。若有1mol KMnO4参加反应,转移的电子的物质的量是_____,被氧化的HCl的物质的量是________。
(2)氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中制得:SiO2+C+N2![]() Si3N4+CO。
Si3N4+CO。
①配平上述反应的化学方程式(将化学计量数填在答题卡相应的横线上)____;
②该反应的氧化剂是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为不同化学元素组成的化合物示意图,以下说法正确的是( )
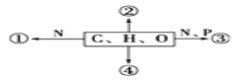
A. 若图中①为某种化合物的基本单位,则①最可能是核苷酸
B. 若②大量积累于皮下和内脏器官周围,则②是磷脂
C. 若④主要在人体肝脏和肌肉内合成,则④最可能是糖原
D. 若③为生物大分子,则一定被甲基绿染成绿色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机化合物A的结构简式如下:
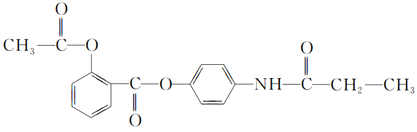
(1)A的分子式是________。
(2)A在NaOH水溶液中充分加热后,再加入过量的盐酸酸化后,可得到B、C、D和![]() 四种有机物,且相对分子质量大小关系为B>C>D,则B、C、D的结构简式分别是B________;C________;D________。
四种有机物,且相对分子质量大小关系为B>C>D,则B、C、D的结构简式分别是B________;C________;D________。
(3)下列物质中,不能与B发生化学反应的是________(填空序号)。
①浓H2SO4和浓HNO3的混合液 ②CH3CH2OH(酸催化) ③CH3CH2CH2CH3 ④Na ⑤浓溴水
(4)在B的同分异构体中,属于1,3,5三取代苯的化合物的结构简式为_________________。
(5)写出B与碳酸氢钠反应的化学方程式:___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示的是细胞中含有的四种有机物的结构与功能。请据图回答下列问题。

(1)图中E含有的元素有_____,A是_____,A形成E的方式为_____。
(2)图中的F为_____。
(3)图中G在植物体内主要是_____,在动物体内主要是_____。
(4)图中H是_____,每克该物质完全氧化分解放出的能量约为39 kJ。
(5)仅由E、F两种物质构成的生物是_____。
(6)E在细胞内的合成受F、G、H中的_____控制。
(7)由C构成的植物细胞特有的结构物质是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物X是一种香豆素衍生物,可以用作香料,其合成路线如下:
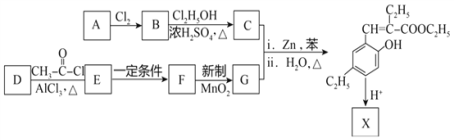
已知: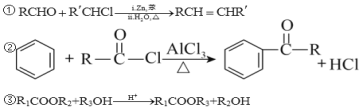
(1)A所含官能团的名称是___________。
(2)B生成C反应的化学方程式是___________________________________________。
(3)G的结构简式是____________________。
(4)F的结构简式是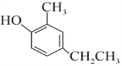 。D的分子式是C7H8O,与F互为同系物。D的结构简式是________。
。D的分子式是C7H8O,与F互为同系物。D的结构简式是________。
(5)X的分子式是C13H14O2,X与足量NaOH溶液共热的化学方程式是________________。
(6)E可以经多步反应合成F,请写出一条可能的合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.车用燃料技术的研究受到广泛关注,目前利用氢能的氢氧燃料电池技术较成熟。某兴趣小组想探究氢氧燃料电池反应的工作原理,设计如图(a)所示的实验装置。实验前,U 型管中装满溶液,电极均为铂电极。
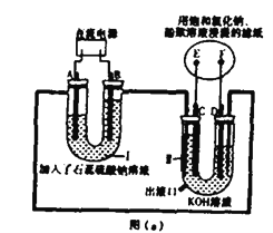
(1)I池为______(填“原电池”、“电解池”),判断A、B的电极名称的依据是:__________ B极的电极反应式:__________
(2)通电一段时间后,滤纸上发生明显颜色变化,则发生反应的化学方程式为___________
(3)Ⅱ池中电极具有导电和_______的作用,写出D的电极反应式:___________
Ⅱ.该兴趣小组查阅资料发现,现有的技术在原料氢气的储存和运输方面都存在安全隐患.2017年3月大连理工大学研究以“铂一碳化钼催化甲醇和水液化重组制备氢气”的新方法获得重大突破,并在美国《自然》杂志发表,具体原理如上图(b)所示:
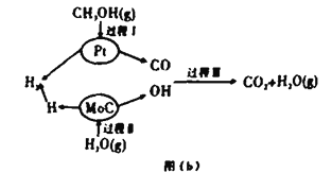
(4)过程Ⅱ属于_________(填“吸热”或“放热)过程。
(5)依据下表完成总反应的热化学方程式:____________
化学键 | C=O | H-H | C-O | H-O | C-H |
E/(kJ/mol) | 803 | 436 | 326 | 464 | 414 |
(6)天然气是一种清洁的化石燃料.也可以在一定的条件下与水反应产生CO2和H2,若生产等量氢气,则消耗甲醇和甲烷的质量比为:_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com