
【题目】NaOH、FeCl3、AlCl3三种固体组成的混合物溶于足量水后,产生1.07g沉淀,再向所得悬浊液中逐滴加入1mol/L HCl溶液,加入HCl溶液的体积与生成沉淀的关系如图所示.

试回答:
(1)A点沉淀为______,(填化学式)B点沉淀为________.(填化学式)
(2)原固体混合物中各物质的物质的量分别是多少?___________
(3)C点处的盐酸的体积是多少毫升? ____________
【答案】 Fe(OH)3 Al(OH)3,Fe(OH)3 原混合物中n(AlCl3)=0.03mol、n(FeCl3)=0.01mol、n(NaOH)=0.17mol 170mL.
【解析】向所得浊液中,逐滴加入1mol/L盐酸,由加入盐酸的体积和生成沉淀的质量关系图分析:①0-20mL,随盐酸的体积增加,生成沉淀的质量不变,说明A点沉淀是Fe(OH)3;m[Fe(OH)3]=1.07g,NaOH、AlCl3、FeCl3组成的混合物,溶于足量水发生反应是:FeCl3+3NaOH=Fe(OH)3↓+3NaCl;AlCl3+4NaOH=NaAlO2+3NaCl+2H2O,NaOH有剩余,溶液是NaCl、NaAlO2和NaOH的混合液,该阶段发生反应是:NaOH+HCl=NaCl+H2O;②20mL处,加入20mL盐酸刚好中和未反应的NaOH,溶液为NaCl、NaAlO2;③20mL-50mL,即A点→B点,随盐酸的体积增加,生成沉淀的质量增加,该阶段发生反应是:NaAlO2+HCl+H2O=Al(OH)3↓+NaCl,离子方程式是:H2O+AlO2-+H+=Al(OH)3↓④50mL处,NaAlO2与盐酸恰好反应,需盐酸体积为:50mL-20mL=30mL,沉淀质量达到最大,溶液为NaCl溶液;⑤50ml-C点,随盐酸的体积增加,沉淀的质量减少,发生反应是:Fe(OH)3+3HCl=FeCl3+3H2O;Al(OH)3+3HCl=AlCl3+3H2O;⑥C点,Fe(OH)3和Al(OH)3完全反应,溶液为FeCl3、AlCl3和NaCl混合液。(1) A处的沉淀为Fe(OH)3,因为加入20.0mLHCl恰好中和过量的NaOH,再加HCl沉淀增多,说明AlO2-转化为Al(OH)3,故A点沉淀为Fe(OH)3;20mL-50mL,即A点→B点,随盐酸的体积增加,生成沉淀的质量增加,该阶段发生反应是:NaAlO2+HCl+H2O=Al(OH)3↓+NaCl,故沉淀B为Al(OH)3,Fe(OH)3;(3)选50mL处,计算NaOH的质量,此时,溶液为NaCl溶液,溶液中Cl-来源于原混合物中的AlCl3、FeCl3和加入的50mLHCl,溶液中Na+来源于原混合物中的NaOH,即n(NaOH)= n(HCl)+ 3n(AlCl3)+ 3n(FeCl3)。
NaAlO2 + HCl + H2O=Al(OH)3↓+NaCl
0.03mol 0.03L×1mol/L=0.03mol
由Al原子守恒得原混合物中n(AlCl3)=n(NaAlO2)=0.03mol;
由Fe原子守恒得原混合物中n(FeCl3)=n[Fe(OH)3]= ![]() =0.01mol;
=0.01mol;
n(NaOH)= n(HCl)+ 3n(AlCl3)+ 3n(FeCl3)=0.05L×1mol/L+3×0.03mol+3×0.01mol=0.17mol;(4)由Na+离子和Cl-离子守恒得,原混合物中n(NaOH)=n(NaCl)=n(Cl-)=3n(FeCl3)+3n(AlCl3)+n(HCl)=0.01mol×3+0.03mol×3+0.05L×1mol/L=0.17mol,C点溶液为FeCl3、AlCl3和NaCl混合液,C点所加盐酸用于中和原混合物中的NaOH,此时所加盐酸物质的量:n(HCl)=n(NaOH)=0.17mol;C点所表示盐酸的体积为:V=![]() =0.17L=170mL。
=0.17L=170mL。


 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案科目:高中化学 来源: 题型:
【题目】下列哪一实例能够证明微量元素是生命活动所必需的
A. Mg是叶绿素的组成成分
B. 油菜缺少B时只开花不结果
C. 哺乳动物血液中Ca盐含量太低,会抽搐
D. 缺P会影响ATP的合成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某无色透明的酸性溶液中,能共存的离子组是( )
A. Na+ 、K+、SO42-、CO32 B. Cu2+、K+、SO42-、NO3
C. Na+、 K+、Cl、 NO3 D. Mg2+、K+、OH、Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁矿石是工业炼铁的主要原料之一,其主要成分为铁的氧化物(设杂质中不含铁元素和氧元素,且杂质不与H2SO4反应).某研究性学习小组对某铁矿石中铁的氧化物的化学式进行探究.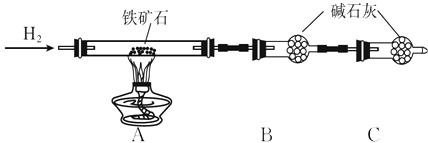
(1)Ⅰ.铁矿石中含氧量的测定
①按上图组装仪器,检查装置的气密性;
②将5.0 g铁矿石放入硬质玻璃管中,装置B、C中的药品如图所示(夹持仪器均省略);
③从左端导气管口处不断地缓缓通入H2 , 待C装置出口处H2验纯后,点燃A处酒精灯
④充分反应后,撤掉酒精灯,再持续通入氢气至完全冷却.
A.装置C的作用为 .
B.测的反应后装置B增重1.35 g,则铁矿石中氧的百分含量为 .
(2)Ⅱ.铁矿石中含铁量的测定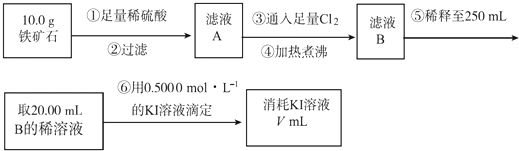
A.步骤④中煮沸的作用是 .
B.步骤⑤中用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、 .
C.下列有关步骤⑥的操作中说法正确的是 .
a.因为碘水为黄色,所以滴定过程中不需加指示剂
b.滴定过程中可利用淀粉溶液作为指示剂
c.滴定管用蒸馏水洗涤后可以直接装液
d.锥形瓶不需要用待测液润洗
e.滴定过程中,眼睛注视滴定管中液面变化
f.滴定结束后,30s内溶液不恢复原来的颜色再读数
D.若滴定过程中消耗0.5000molL﹣1KI溶液20.00mL,则铁矿石中铁的百分含量为 .
(3)Ⅲ.由Ⅰ、Ⅱ可以推算出该铁矿石中铁的氧化物的化学式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化硫酰(SO2Cl2)主要用作氯化剂.它是一种无色液体,熔点﹣54.1℃,沸点69.1℃.氯化硫酰可用干燥的二氧化硫和氯气在活性炭催化剂存在下反应制取:
SO2(g)+Cl2(g)SO2Cl2(l)△H=﹣97.3kJ/mol
(1)试写出常温常压下化学平衡常数K的表达式:K=;若在此条件下,将化学平衡常数K增大,化学反应速率v正也增大,可采取的措施是(选填编号).
a.降低温度 b.移走SO2Cl2 c.增加反应物浓度 d.以上都不对
(2)为了提高上述反应中Cl2的平衡转化率,下列措施合理的是(选填编号).
a.缩小容器体积 b.使用催化剂c.增加SO2浓度 d.升高温度
(3)在100℃时,往上述平衡体系中加入37Cl2 , 一段时间后,则平衡体系中含有37Cl的物质有(选填编号).
a.只有37Cl2 b.只有SO ![]() Cl2 c.37Cl2和SO
Cl2 c.37Cl2和SO ![]() Cl2 d.无法判断
Cl2 d.无法判断
(4)下列描述中能说明上述反应已达平衡的是(选填编号).
a.v(Cl2)=v(SO2)
b.容器中气体压强不随时间而变化
c.c(Cl2):c(SO2)=1:1
d.容器中气体颜色不随时间而变化.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度(t℃)时,水的KW=1×10﹣13 , 则该温度(填“大于”、“小于”或“等于”)25℃,其理由是 . 将此温度下pH=11的NaOH溶液a L与pH=1的H2SO4的溶液b L混合,若所得混合液为中性,则a:b= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有人设想将碳酸钙通过特殊的加工方法使之变为纳米碳酸钙(即碳酸钙粒子直径是纳米级),这将引起建筑材料的性能发生巨变。下列关于纳米碳酸钙的推测可能正确的是( )
A. 纳米碳酸钙是与胶体相似的分散系
B. 纳米碳酸钙会产生丁达尔效应
C. 纳米碳酸钙化学性质已与原来碳酸钙完全不同
D. 纳米碳酸钙的粒子能透过滤纸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学与生产、生活的说法中,不正确的是
A.陶瓷、水泥和玻璃都属于硅酸盐产品
B.用浸泡过高锰酸钾溶液的硅藻土吸收水果产生的乙烯以达到保鲜目的
C.铝合金的大量使用归功于人们能使用焦炭从氧化铝中获得铝
D.二氧化硫是主要的大气污染物,能形成酸雨,其pH小于5.6
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com