
【题目】下列物质分类正确的是
A.FeO、Fe2O3、Na2O2均为碱性氧化物
B.稀豆浆、硅酸、氯化铁溶液均为胶体
C.烧碱、冰醋酸、四氯化碳均为电解质
D.盐酸、水玻璃、氨水均为混合物
科目:高中化学 来源: 题型:
【题目】现有一些只含C、H、O三种元素的有机物,它们燃烧时消耗的O2和生成的CO2的体积比是3:4。
(1)这些有机物中,相对分子质量最小的化合物的分子式是_______________。
(2)某两种碳原子数相同的上述有机物,若它们的相对分子质量分别为a和b(a<b),则b-a必定是_______________(填入一个数字)的整数倍。
(3)在这些有机物中有一种化合物,它含有两个羧基。取0.2625g该化合物恰好能跟25.00mL0.1000moL·L-1NaOH溶液完全中和。由此可以得知该化合物的相对分子质量应是______,并可推导出它的分子式应是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在微生物作用下电解有机废水(含CH3COOH),可获得清洁能源H2,其原理如图所示,下列有关说法不正确的是

A. 电极B极为负极
B. 与电源A极相连的惰性电极上发生的反应为:CH3COOH-8e-+H2O=2CO2↑+8H+
C. 通电后,H+通过质子交换膜向右移动,最终右侧溶液PH减小
D. 通电后,若有0.1molH2生成,则转移0.2mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1—20号元素中(用元素符号或化学式填空)
(1)原子半径最小的是_______;第三周期中原子半径最大的是(稀有气体除外)________。
(2)与水反应最剧烈的金属单质是_______。
(3)气态氢化物最稳定的是_____(填化学式)。
(4)最活泼的金属与最活泼的非金属元素组成的化合物,电子式为 ______
(5)最高价氧化物的水化物中,酸性最强的是________,碱性最强的是______ (填化学式)。
(6)推测Si、N气态氢化物的稳定性:_____>_______(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素X、Q、Y、Z、M、R均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3:4,M原子的最外层电子数与次外层电子数之比为3:4;R-、Z+、X+离子半径逐渐减小;化合物XR常温下为气体,Q和Y在周期表中的位置相邻,请回答下列问题:
(1)写出单质R的一种工业用途_______________________。
(2)M和R的最高价氧化物的水化物中酸性最强的是___________(用化学式表示)。
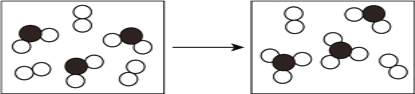
(3)下图表示由上述元素中的某两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,写出该转化过程的化学方程式为____________________。
(4)由X、Y、Z、M四种元素组成的一种离子化合物A,已知A,既能与盐酸反应,又能与氢氧化钠溶液反应,还能和氯水反应,写出A与氯水反应的离子方程式___________。
(5)科学家认为存在QX5这种物质,且预测其与水剧烈反应放出气体,所得水溶液呈弱碱性,已知QX5中含有离子键和极性键,写出化合物的电子式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,恒容密闭容器中,发生反应:X(g)+Y(g)![]() Z(g)
Z(g) ![]() ,各物质的浓度随时间变化如图所示。
,各物质的浓度随时间变化如图所示。

(1)从反应开始到4min时平衡,X的平均反应速率为________________。
(2)根据图像数据,4min时平衡常数K=________________。
(3)若使平衡时体系中c(X)=c(Z),则改变条件为 ________________。(只写一项)
(4)若某时刻,v正(Y)=2v逆(Z),则反应___________达平衡(填“已”或“未”)
(5)图中a.b对应的正反应速率大小关系为va_____vb(填“大于”、“等于”或“小于”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据美国《农业研究》杂志报导,美国的科学家发现半胱氨酸能增强艾滋病毒感染者的免疫力,对控制艾滋病的蔓延有奇效。已知半胱氨酸的结构式为:![]() ,则下列说法错误的是( )
,则下列说法错误的是( )
A. 半胱氨酸属α-氨基酸
B. 半胱氨酸是一种两性物质
C. 两个半胱氨酸发生缩合反应可能生成两种不同的二肽
D.  可与NaOH溶液反应放出一种碱性气体
可与NaOH溶液反应放出一种碱性气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以葡萄糖为原料制得的山梨醇(A)和异山梨醇(B)都是重要的生物质转化平台,化合物E是一种治疗心绞痛的药物,由葡萄糖为原料合成E的过程如下:

回答下列问题:
(1)葡萄糖的分子式为___________________。
(2)A中含有的官能团的名称为_________________。
(3)由B到C的反应类型为___________________。
(4)C的结构简式为___________________________。
(5)由D到E的反应方程式为__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石油化工是江苏省的支柱产业之一。醋酸乙烯酯是合成维尼纶的重要单体,某化工厂曾利用下列工艺生产醋酸乙烯酯:
2CH2=CH2+O2![]() 2CH3CHO………………………………………①
2CH3CHO………………………………………①
2CH3CHO+O2![]() 2CH3COOH……………………………………………②
2CH3COOH……………………………………………②
2CH2=CH2+2CH3COOH+O2→2CH3COOCH=CH2+2H2O…………………③
由于副反应的发生,反应①中乙烯的利用率为75%,反应②中乙醛的利用率为80%,反应③中乙烯和乙酸的利用率均为75%。
(1)为使乙酸乙烯酯获得最大产量,乙烯先后两次的投料比为多少_______?
(2)以2.8×104kg 乙烯为原料最多可制得醋酸乙烯酯多少千克_______?
(3)若各步副反应中反应物物质的量之比均与主反应相同。以乙烯和空气为原料生产醋酸乙烯酯,通入的空气(O2的体积分数为1/5)与乙烯的体积比至少为多少_______?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com