
【题目】下列说法不正确的是( )
A. 钠的金属性比锂强 B. 碘的非金属性比氯弱
C. ⅤA族中原子半径最小的是氮 D. 第三周期中,金属性最强的是铝
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示。若Y原子的L层电子数是K层电子数的3倍,下列说法不正确的是
![]()
A. Y的气态氢化物比X的稳定B. W的最高价氧化物对应水化物的酸性比Z的强
C. Y的非金属性比Z的强D. X与Y形成的化合物都易溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取乙烯,常因温度过高而使乙醇和浓H2SO4反应生成少量的二氧化硫。有人设计下列实验以确认上述混合气体中有乙烯和二氧化硫。其装置如下图所示。
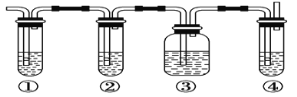
图中①、②、③、④装置可盛放的试剂依次是
A. 品红溶液 、NaOH溶液、浓H2SO4 、酸性KMnO4溶液
B. 品红溶液 、NaOH溶液、品红溶液 、酸性KMnO4溶液
C. 酸性KMnO4溶液 、NaOH溶液、品红溶液 、溴水
D. 浓H2SO4 、NaOH溶液、品红溶液 、溴水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在 Cu/ZnO催化剂存在下,CO2和H2可发生下列反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
(1)反应中被氧化的元素是:____,氧化剂是____。试在下列方程式中用单线桥标出电子转移的方向和数目:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)____
CH3OH(g)+H2O(g)____
(2)该反应的平衡常数表达式 K=____。若只增加CO2的浓度,该平衡向____移动,平衡常数 K___(选填“增大”、“小”或“不变”)。
(3)从下图可以看出,由于温度不同,A和B中___先达到平衡状态,说明反应温度 A___B(选填“>”、“<”或“=”),从甲醇体积分数的比较还可以说明该反应是______热反应(选填“放”或“吸”);反应进行到图中M处时,正反应速率______逆反应速率(选填“>”、 “<”或“=”)。

(4)一定条件下,将 n(CO2):n(H2)=1:1 的混合气充入恒温恒容密闭容器中,若容器中气体______(选填“密度”或“压强”)保持不变,说明该反应已达平衡状态。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是关于有机物A、B、C的信息:
A | B | C |
①它的产量可衡量一个国家石油化工发展水平; ②能使溴的四氯化碳溶液褪色; ③可用于果实催熟. | ①C、H两种元素组成 ②分子球棍模型为 | ①分子键线式为 ②相对分子质量为68 |
根据表中信息回答下列问题:
(1)A与溴的四氯化碳溶液反应的生成物的名称为_______________;
(2)A在一定条件下,与水反应制乙醇的化学方程式:____________________;反应类型是______。
(3)B具有的性质是_____________________(填序号)。
①无色无味液体 ②有毒 ③不溶于水 ④密度比水大 ⑤任何条件下均不与氢气反应
⑥一定条件下,能与CH2=CH2反应制苯乙烷 ⑦与溴水混合后液体分层且上层呈橙红色
(4)写出B的最简单同系物制TNT的化学方程式 _____________________;反应类型是________。
(5)C是天然橡胶的单体,写出天然高分子橡胶的结构简式________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中,所使用的装置(夹持装置略)、试剂和操作方法有错误的是

A. 观察Fe(OH)2的生成
B. 除去CO中的CO2
C. 配制一定物质的量浓度的NaNO3溶液
D. 25 mL滴定管读数为11.80 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家哈伯因为氨气的合成曾获1918年诺贝尔奖。
(1)写出实验室制取氨气的化学方程式_______________。检验氨气已装满的方法是_______________。
(2)氨气可用如图装置进行喷泉实验,把氨气换成______(填序号)也可形成喷泉实验。
A.二氧化碳 B.氧气 C.氯化氢气体 D.氢气

(3)完成氨催化氧化生成为NO的反应方程式_________,产物NO有毒,不能排入空气中,若将NO和氧气一起通入水中能生成硝酸的化学方程式:________
(4)2.56gCu与足量的浓硝酸反应生成的气体与一定量的O2混合,然后通入水中恰好完全反应无气体剩余,则该氧气的物质的量为____mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝元素在自然界中主要存在于铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)中。工业上用铝土矿制备铝的某种化合物的工艺流程如下。

(1)在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。
①检验滤液B中是否还含有铁元素的方法为:_______________(注明试剂、现象)。
②将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为__________(填代号)。
a.氢氧化钠溶液 b.硫酸溶液 c.氨水 d.二氧化碳
③由滤液B制备氯化铝晶体涉及的操作为:边滴加浓盐酸边___________________(填操作名称)、过滤、洗涤。
④高铁酸钠(Na2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与漂白液(主要成分NaClO)在强碱性条件下反应可制取Na 2FeO4,反应的离子方程式为___________________________。
(2) ①SiO2和NaOH焙烧制备硅酸钠,可采用的装置为_______________(填代号)。

②过量CO2通入到硅酸钠的溶液中,然后加热蒸干,再高温灼烧,最后所得固体成分___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关同分异构体数目的叙述中正确的是( )
A. 分子组成是C5H10O2属于羧酸的同分异构体有5种
B. C8H10中只有3种属于芳香烃的同分异构体
C. 甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有6种
D. 新戊烷的二氯代物只有1种同分异构体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com