
【题目】在 Cu/ZnO催化剂存在下,CO2和H2可发生下列反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
(1)反应中被氧化的元素是:____,氧化剂是____。试在下列方程式中用单线桥标出电子转移的方向和数目:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)____
CH3OH(g)+H2O(g)____
(2)该反应的平衡常数表达式 K=____。若只增加CO2的浓度,该平衡向____移动,平衡常数 K___(选填“增大”、“小”或“不变”)。
(3)从下图可以看出,由于温度不同,A和B中___先达到平衡状态,说明反应温度 A___B(选填“>”、“<”或“=”),从甲醇体积分数的比较还可以说明该反应是______热反应(选填“放”或“吸”);反应进行到图中M处时,正反应速率______逆反应速率(选填“>”、 “<”或“=”)。

(4)一定条件下,将 n(CO2):n(H2)=1:1 的混合气充入恒温恒容密闭容器中,若容器中气体______(选填“密度”或“压强”)保持不变,说明该反应已达平衡状态。
【答案】 H CO2 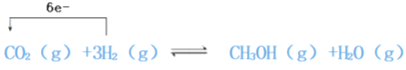
![]() 正反应方向 不变 B < 放 > 压强
正反应方向 不变 B < 放 > 压强
【解析】(1)反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)中氢气中氢元素由0价变为+1价,被氧化;故被氧化的元素为H元素;二氧化碳中碳由+4价变为-2价,转移电子数为6,氧化剂是CO2;用单线桥标出电子转移的方向和数目为:
CH3OH(g)+H2O(g)中氢气中氢元素由0价变为+1价,被氧化;故被氧化的元素为H元素;二氧化碳中碳由+4价变为-2价,转移电子数为6,氧化剂是CO2;用单线桥标出电子转移的方向和数目为: ;(2)反应CO2(g)+3H2(g)
;(2)反应CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)的平衡常数表达式 K=
CH3OH(g)+H2O(g)的平衡常数表达式 K=![]() ;若只增加 CO2的浓度,该平衡向正反应方向移动,平衡常数只与温度有关,反应温度不变,故平衡常数 K不变;(3)从右图可以看出,由于温度不同,根据先拐先平,A 和 B 中B先达到平衡状态,说明反应温度 A<B,温度高甲醇的体积分数小,说明升高温度平衡向逆反应方向移动,则该反应是放热反应;反应进行到图中 M 处时还没达到平衡状态,反应向正方向进行,故正反应速率>逆反应速率。(4)一定条件下,将 n(CO2):n(H2)=1:1 的混合气充入恒温恒容密闭容器中,恒容条件下反应物均为气体时密度始终保持不变,密度不变不能说明反应达平衡,故若容器中气体压强保持不变,说明该反应已达平衡状态。
;若只增加 CO2的浓度,该平衡向正反应方向移动,平衡常数只与温度有关,反应温度不变,故平衡常数 K不变;(3)从右图可以看出,由于温度不同,根据先拐先平,A 和 B 中B先达到平衡状态,说明反应温度 A<B,温度高甲醇的体积分数小,说明升高温度平衡向逆反应方向移动,则该反应是放热反应;反应进行到图中 M 处时还没达到平衡状态,反应向正方向进行,故正反应速率>逆反应速率。(4)一定条件下,将 n(CO2):n(H2)=1:1 的混合气充入恒温恒容密闭容器中,恒容条件下反应物均为气体时密度始终保持不变,密度不变不能说明反应达平衡,故若容器中气体压强保持不变,说明该反应已达平衡状态。


科目:高中化学 来源: 题型:
【题目】C8H18经多步裂化,最后完全转化为C4H8、C3H6、C2H4、C2H6、CH4五种气体的混合物.该混合物的平均相对分子质量可能是( )
A.28
B.30
C.38
D.40
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验过程中,溶液的pH大于7的是
A. 向NaCl溶液中滴加醋酸 B. 向KNO3溶液中滴加稀H2SO4
C. 向稀HCl溶液中滴加稀HNO3 D. 向NaOH溶液中滴加Na2CO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池可将化学能转化为电能.设计两种类型的原电池,探究其能量转化效率.限选材料:ZnSO4(aq),CuSO4(aq);铜片,锌片和导线.
(1)①完成原电池甲的装置示意图(如图),并作相应标注.要求:在同一烧杯中,电极与溶液含相同的金属元素. 
②以铜片为电极之一,CuSO4(aq)为电解质溶液,只在一个烧杯中组装原电池乙,工作一段时间后,可观察到负极 .
③甲乙两种原电池中可更有效地将化学能转化为电能的是 , 其原因是 .
④盐桥中向CuSO4溶液中迁移的离子是(填序号)
A.K+ B.NO3﹣ C.Ag+ D.SO42﹣
(2)电解原理在化学工业中有着广泛的应用.现将你设计的原电池通过导线与图2中电解池相连,其中,a为电解液,X和Y是两块电极板,则: ①若X和Y均为惰性电极,a为CuSO4溶液,则电解时的化学反应方程式为 . 通过一段时间后,向所得溶液中加入0.2molCuO粉末,恰好恢复电解前的浓度和pH,则电解过程中转移的电子的物质的量为 .
②若X、Y分别为铁和铜,a仍为CuSO4溶液,则Y极的电极反应式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化学键的说法正确的是( )
A.构成单质分子的微粒一定含有共价键
B.全部由非金属元素组成的化合物中可能含有离子键
C.非极性键只存在于非金属单质或共价化合物中
D.化学键包括离子键、共价键、氢键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水MgBr2可广泛用于有机反应催化剂、污水处理剂等。实验室可用镁屑与液溴为原料,采用下图装置制备无水MgBr2,请回答:
(1)识别下图中仪器。A的名称是_____,B是_____

(2)实验时,可向装置 C 中缓慢通入干燥的氮气,直至溴完全导入 三颈瓶中。干燥的氮气能将液溴吹出,因为液溴具有_____的性质;实验中不能用干燥空气代替干燥N2,原因是:____MgBr2和乙醚能发生如下反应:MgBr2+3C2H5OC2H5![]() MgBr2·3C2H5OC2H5+Q(Q>0);反应完毕后恢复至室温,过滤,滤液转移至另一干燥的烧瓶中,冷却至0℃,析出晶体,再过滤得三乙醚合溴化镁粗品。第一次过滤除去的 物质是____。过滤必须用到的玻璃仪器是:____。
MgBr2·3C2H5OC2H5+Q(Q>0);反应完毕后恢复至室温,过滤,滤液转移至另一干燥的烧瓶中,冷却至0℃,析出晶体,再过滤得三乙醚合溴化镁粗品。第一次过滤除去的 物质是____。过滤必须用到的玻璃仪器是:____。
(3)试用平衡移动的原理说明得到三乙醚合溴化镁后,加热有利于其分解,得无水MgBr2产品的原因:____。
(4)为测定产品的纯度,可用EDTA(简写为Y4-)标准溶液滴定,反应的离子方程式:Mg2++Y4-=MgY2-
①滴定前润洗滴定管的操作方法是____。
②测定前,先称取0.2500g无水MgBr2产品,溶解后,用0.0500mol/L的EDTA标准溶液滴定至终点,消耗EDTA标准溶液26.50mL,则测得无水MgBr2产品的纯度是____(以质量分数表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用镁一次氯酸钠燃料电池作电源模拟消除工业酸性废水中的Cr2O72-的过程(将“Cr2O72-”还原为“Cr3+”),装置如图所示。下列说法中错误的是
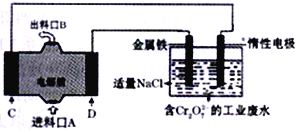
A. 金属铁电极的反应为:Fe-2e-=Fe2+
B. 装置中电子的流动路线是: C电极→惰性电极→金属铁电极→D电极
C. 装置工作过程中消耗14.4gMg,理论上可消除Cr2O72-0.1mol
D. 将Cr2O72-处理后的废水比原工业废水的pH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度700℃时,向容积为1L的密闭容器中充入一定量的CO和H2O发生反应CO(g)+H2O(g)CO2(g)+H2(g),反应过程中测定的部分数据见表(表中t1<t2).下列说法正确的是( )
反应时间/min | n(CO)/mol | n(H2O)/mol |
0 | 0.60 | 0.30 |
t1 | 0.40 | |
t2 | 0.10 |
A.反应在t1min内的平均速率为v(H2)=0.20/t1molL﹣1min﹣1
B.保持其他条件不变,向平衡体系中再通入0.10molH2O,与原平衡相比,达到新平衡时CO转化率增大,H2O的体积分数减小
C.温度升至800℃,上述反应平衡常数为0.64,则正反应为吸热反应
D.700℃时,若向密闭容器中充入CO(g)、H2O(g)、CO2(g)、H2(g)的物质的量分别为0.60mol、1.00mol、0.60mol、0.60mol,则此时该反应v(正)<v(逆)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C,H,N三种元素在人体的化学成分中,质量分数共占73%左右,而这三种元素在组成岩石圈的化学成分中,质量分数不到1%。这个事实说明
A. 生物界和非生物界具有统一性
B. 生物界和非生物界具有差异性
C. 这三种元素是组成人体的主要元素
D. 生物界和非生物界的组成元素完全不同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com