
����Ŀ����þһ��������ȼ�ϵ������Դģ��������ҵ���Է�ˮ�е�Cr2O72-�Ĺ���(����Cr2O72-����ԭΪ��Cr3+��)��װ����ͼ��ʾ������˵���д������
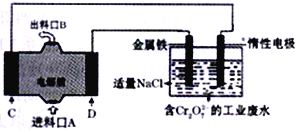
A. �������缫�ķ�ӦΪ:Fe-2e-=Fe2+
B. װ���е��ӵ�����·����: C�缫�����Ե缫���������缫��D�缫
C. װ�ù�������������14.4gMg�������Ͽ�����Cr2O72-0.1mol
D. ��Cr2O72-������ķ�ˮ��ԭ��ҵ��ˮ��pH����
���𰸡�B
��������Fe2+��Cr2O72-��ԭΪCr3+��������������Fe2+���������缫�ķ�ӦΪ:Fe-2e-=Fe2+����A��ȷ���������Һ��û�е�������������װ���е��ӵ�����·����: C�缫�����Ե缫���������缫��D�缫����B����װ�ù�������������14.4gMg��ת�Ƶ���1.2mol����������Fe2+0.6mol������Cr2O72+6Fe2++14H+�T2Cr3++6Fe3++7H2O��0.6mol Fe2+������Cr2O72-0.1mol����C��ȷ�����������ӵõ�����������������������Cr2O72+6Fe2++14H+�T2Cr3++6Fe3++7H2O�����Խ�Cr2O72-������ķ�ˮ��ԭ��ҵ��ˮ��pH��������D��ȷ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʯ��ʯ��ʳ�Ρ���̿��ˮΪԭ�ϣ�д���ϳɾ�����ϩ�Ļ�ѧ����ʽ������֪��CaO+3C ![]() CaC2+CO����
CaC2+CO����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ���ǣ�������
A.��ϡ��ˮ��μ���ϡ�����У�����Һ��pH=7ʱ��c��SO42������c��NH4+��
B.NaHCO3��Һ�У�c ��CO32����+c��H+��=c��H2CO3��+c��OH����
C.1 L 0��1 molL��1CuSO4��NH4��2SO46H2O��Һ�У�c��SO42������c��NH4+����c��Cu2+����c��H+����c��OH����
D.��0.1mol/L�İ�ˮ�м�����������粒��壬����Һ��c��OH����/c��NH3H2O������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���� Cu/ZnO���������£�CO2��H2�ɷ������з�Ӧ��CO2��g��+3H2��g��![]() CH3OH��g��+H2O��g��
CH3OH��g��+H2O��g��
��1����Ӧ�б�������Ԫ���ǣ�____����������____���������з���ʽ���õ����ű������ת�Ƶķ������Ŀ��CO2��g��+3H2��g��![]() CH3OH��g��+H2O��g��____
CH3OH��g��+H2O��g��____
��2���÷�Ӧ��ƽ�ⳣ������ʽ K=____����ֻ����CO2��Ũ�ȣ���ƽ����____�ƶ���ƽ�ⳣ�� K___��ѡ�������С�����䡱����
��3������ͼ���Կ����������¶Ȳ�ͬ��A��B��___�ȴﵽƽ��״̬��˵����Ӧ�¶� A___B��ѡ���������������=�������Ӽ״���������ıȽϻ�����˵���÷�Ӧ��______�ȷ�Ӧ��ѡ��š�������������Ӧ���е�ͼ��M��ʱ������Ӧ����______�淴Ӧ���ʣ�ѡ������� ��������=������

��4��һ�������£��� n(CO2):n(H2)=1:1 �Ļ����������º����ܱ������У�������������______��ѡ��ܶȡ���ѹǿ�������ֲ��䣬˵���÷�Ӧ�Ѵ�ƽ��״̬��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ˮ��25���95��ʱ������ƽ��������ͼ��ʾ�� 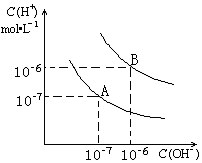
��1����25��ʱˮ�ĵ���ƽ������ӦΪ���A����B��������˵������
��2��25��ʱ����pH=9��NaOH��Һ��pH=4��H2SO4��Һ��ϣ������û����Һ�� pH=7����NaOH��Һ��H2SO4��Һ�������Ϊ
��3��95��ʱ����100���pH1=a��ijǿ����Һ��1���pH2=b��ijǿ����Һ��Ϻ���Һ�����ԣ�����ǰ����ǿ���pH1��ǿ���pH2֮��Ӧ����Ĺ�ϵ��
��4������B��Ӧ�¶��£�pH=2��ijHA��Һ��pH=10��NaOH��Һ�������Ϻ����Һ��pH=5���������ԭ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����:Ksp(PbI2)=4��10-6��Ksp(PbS)=8��10-28��ȡ������ɫPbI2�������Ƴ�100mL��Һ�����ƹ�������Һ������Ũ����ʱ��ı仯��ϵ��ͼ��ʾ������˵������ȷ����

A. A�㴦�ɱ�ʾPbI2�IJ�������Һ
B. Tʱ���п������PbI2��Һ�м�����KI����
C. ������PbI2������Һ�е�c(I-)=10-2mol/L
D. ��A�㴦��PbI2��Һ�м���100mL 2��10-3mol/L��Na2S��Һ,ƽ�����Һ�е�c(Pb2+)<4��10-3mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���Aֻ����C��H��O����Ԫ�أ��������л��ϳɵ��м��塣16.8g���л��ᆳȼ������44.0g CO2 ��14.4g H2O������ͼ��������Է�������Ϊ84���������������A�����к���O-H����-C��C-H�����Ź����������������壬�����֮��Ϊ6:1:1��
��1��A�ķ���ʽ��______________��
��2��A�Ľṹ��ʽ��___________________��
��3��A��һ�������£��ܷ����ķ�Ӧ����Ϊ____________________��
a.�ӳɷ�Ӧ b.������Ӧ c.�ۺϷ�Ӧ d.ȡ����Ӧ
��4���л���B��A��ͬ���칹�壬1molB����1molBr2��ȫ�ӳɡ���֪��B�ṹ�к���ȩ����B������̼ԭ��һ������ͬһ��ƽ�棬��д�����з���������B�Ľṹ��ʽ�������������칹��_________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�������ȷ�Ӧ����( )
A. C6H12O6(������aq)��6O2![]() 6CO2��6H2O
6CO2��6H2O
B. ����������Һ��������кͷ�Ӧ
C. ��Ӧ��������������������������
D. �ƻ���Ӧ��ȫ����ѧ���������������ƻ�������ȫ����ѧ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ɷ������·�Ӧ��P4+5O2�TP4O10 �� ��֪�������л�ѧ����Ҫ���յ������ֱ�Ϊ��P��P��a kJmol��1��P��O��b kJmol��1��P=O��c kJmol��1��O=O��d kJmol��1 �� ����ͼʾ�ķ��ӽṹ���й����ݹ���÷�Ӧ�ġ�H��������ȷ���ǣ�������
A.��6a+5d��4c��12b��kJmol��1
B.��4c+12b��6a��5d��kJmol��1
C.��4c+12b��4a��5d��kJmol��1
D.��4a+5d��4c��12b��kJmol��1
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com