
����Ŀ���л���Aֻ����C��H��O����Ԫ�أ��������л��ϳɵ��м��塣16.8g���л��ᆳȼ������44.0g CO2 ��14.4g H2O������ͼ��������Է�������Ϊ84���������������A�����к���O-H����-C��C-H�����Ź����������������壬�����֮��Ϊ6:1:1��
��1��A�ķ���ʽ��______________��
��2��A�Ľṹ��ʽ��___________________��
��3��A��һ�������£��ܷ����ķ�Ӧ����Ϊ____________________��
a.�ӳɷ�Ӧ b.������Ӧ c.�ۺϷ�Ӧ d.ȡ����Ӧ
��4���л���B��A��ͬ���칹�壬1molB����1molBr2��ȫ�ӳɡ���֪��B�ṹ�к���ȩ����B������̼ԭ��һ������ͬһ��ƽ�棬��д�����з���������B�Ľṹ��ʽ�������������칹��_________________________________________��
���𰸡� C5H8O 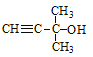 abcd (CH3)2C=CHCHO��CH3CH=C(CH3)CHO
abcd (CH3)2C=CHCHO��CH3CH=C(CH3)CHO
������������ͼ��������Է�������Ϊ84������16.8g���л��ᆳȼ������44.0g CO2��14.4g H2O���ɼ����л���C��H��O�ĸ������Դ�ȷ���л������ʽ���������������A�����к���O-H����-C��C-H�����˴Ź��������������壬�����Ϊ6��1��1��˵����3�ֲ�ͬ��Hԭ�ӣ��Դ�ȷ���ṹ��ʽ���ݴ˽��
��1���л���Aֻ����C��H��O����Ԫ�أ�����ͼ��������Է�������Ϊ84��16.8g�л���A�����ʵ���Ϊ0.2mol����ȼ������44.0g CO2�����ʵ���Ϊ1mol������14.4g H2O�����ʵ���Ϊ14.4g��18g/mol=0.8mol�����л���A��Cԭ����ĿΪ1mol��0.2mol=5��Hԭ����ĿΪ0.8mol��2/0.2mol=8������ԭ����ĿΪ(8412��58)/16=1����A�ķ���ʽΪC5H8O��
��2��A���ʵIJ����Ͷ�Ϊ(2��5+28)/2=2���������������A�����к���O-H����-C��C-H�����˴Ź��������������壬�����Ϊ6��1��1���ʷ����к���2��CH3��1��-OH������ͬһCԭ���ϣ����A�Ľṹ��ʽΪ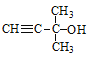 ��
��
��3��a.����̼̼�������ܷ����ӳɷ�Ӧ��a��ȷ��b.����̼̼�������ܷ���������Ӧ��b��ȷ��c.����̼̼�������ܷ����ۺϷ�Ӧ��c��ȷ��d.�����ǻ����ܷ���ȡ����Ӧ��d��ȷ����ѡabcd��
��4���л���B��A��ͬ���칹�壬1molB����1molBr2��ȫ�ӳɣ�����1��̼̼˫������֪B�ṹ�к���ȩ����B������̼ԭ��һ������ͬһ��ƽ�棬�����������B�Ľṹ��ʽ�������������칹��Ϊ(CH3)2C=CHCHO��CH3CH=C(CH3)CHO��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼���γɻ�������������Ԫ��,�䵥�ʼ������������������������Ҫ��Դ���ʡ���ش��������⡣
��1���л���M����̫������տ�ת����N,ת����������:
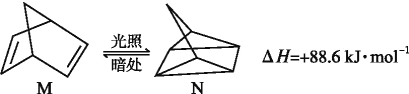
��M��N���, ���ȶ�����____��
��2������͵�������ı������������ʡ���ʯī�����ۺͶ������Ѱ�һ����������ڸ���������,�������ʿ������²���,4Al(s)+3TiO2(s)+3C(s)![]() 2Al2O3(s)+3TiC(s)����H=-1 176 kJ��mol-1,��Ӧ������,ÿת��1 mol���ӷų�������Ϊ________
2Al2O3(s)+3TiC(s)����H=-1 176 kJ��mol-1,��Ӧ������,ÿת��1 mol���ӷų�������Ϊ________
��3����֪��1 mol H��H����1 mol N��H����1 mol N��N���ֱ���Ҫ��������436 kJ��391 kJ��946 kJ,��N2��H2��Ӧ����NH3���Ȼ�ѧ����ʽΪ_________________
��4�����������Ȼ�ѧ����ʽ��
��C(s)��O2(g)===CO2(g)����H1����393.5 kJ��mol��1��
��H2(g)��1/2O2(g)===H2O(l)����H2����285.8 kJ��mol��1��
��CH3COOH(l)��2O2(g)===2CO2(g)��2H2O(l) ��H3����870.3 kJ��mol��1
���Լ����2C(s)��2H2(g)��O2(g)===CH3COOH(l)�ķ�Ӧ��Ϊ________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڻ�ѧ����˵����ȷ����(����)
A.���ɵ��ʷ��ӵ���һ�����й��ۼ�
B.ȫ���ɷǽ���Ԫ����ɵĻ������п��ܺ������Ӽ�
C.�Ǽ��Լ�ֻ�����ڷǽ������ʻۻ�������
D.��ѧ���������Ӽ������ۼ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����þһ��������ȼ�ϵ������Դģ��������ҵ���Է�ˮ�е�Cr2O72-�Ĺ���(����Cr2O72-����ԭΪ��Cr3+��)��װ����ͼ��ʾ������˵���д������
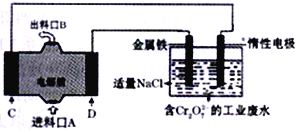
A. �������缫�ķ�ӦΪ:Fe-2e-=Fe2+
B. װ���е��ӵ�����·����: C�缫�����Ե缫���������缫��D�缫
C. װ�ù�������������14.4gMg�������Ͽ�����Cr2O72-0.1mol
D. ��Cr2O72-������ķ�ˮ��ԭ��ҵ��ˮ��pH����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ����20ml 0.1molL��1NaOH��Һ����μ���0.2molL��1������Һ���ζ�������ͼ��ʾ���й�����Ũ�ȵĹ�ϵ�У�����ȷ���ǣ������� 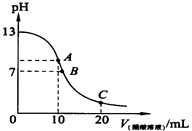
A.��A�㣺c��Na+����c��OH������c��CH3COO������c��H+��
B.��B�㣺c��Na+����c��CH3COO������c��OH������c��H+��
C.��C�㣺c��CH3COO������c��Na+����c��H+����c��OH����
D.��C�㣺c��CH3COO����+c��CH3COOH����2 c��Na+��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���¶�700��ʱ�����ݻ�Ϊ1L���ܱ������г���һ������CO��H2O������ӦCO��g��+H2O��g��CO2��g��+H2��g������Ӧ�����вⶨ�IJ������ݼ���������t1��t2��������˵����ȷ���ǣ�������
��Ӧʱ��/min | n��CO��/mol | n��H2O��/mol |
0 | 0.60 | 0.30 |
t1 | 0.40 | |
t2 | 0.10 |
A.��Ӧ��t1min�ڵ�ƽ������Ϊv��H2��=0.20/t1molL��1min��1
B.���������������䣬��ƽ����ϵ����ͨ��0.10molH2O����ԭƽ����ȣ��ﵽ��ƽ��ʱCOת��������H2O�����������С
C.�¶�����800�棬������Ӧƽ�ⳣ��Ϊ0.64��������ӦΪ���ȷ�Ӧ
D.700��ʱ�������ܱ������г���CO��g����H2O��g����CO2��g����H2��g�������ʵ����ֱ�Ϊ0.60mol��1.00mol��0.60mol��0.60mol�����ʱ�÷�Ӧv��������v���棩
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и����У�������֬�����ʵ��ǣ� ��
A. ά����D B. ���̴� C. ���Լ��� D. ֬��ø
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ƽ�����»�������8 �����������Ŷ���ʯīϩ������-20���ܷ���4 h �����ܷ���; �����Ͻ�ܲĺ�̼��ά�����˸�2.35m��������Ϊ10kg ����èľż��������չ������ʱ�����й���������˵���У�����ȷ����

A. ʯīϩ���ܵ��ȵĽ������� B. ���Ͻ����ܶȽϵ͵Ľ�������
C. ̼��ά���͵��µ����ǽ������� D. ���Ͳ�������ࡢ��;��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������һֱ�ڻ���̽��Ӱ��������������ؼ����ƴ�ʩ��
��1���������Ǵ����п�������������Ҫ�ɷ�֮һ�����ں�ˮ�����ܽ�Һ����ͨ����ѧ��Ӧ�����ġ�
�����ܽ����ڽ����ɢϵ�����չ�����������ܽ��İ���ʱ���ɹ۲쵽_______ЧӦ��
�������е�SO2ת��Ϊ�����εĹ����У��������������������õ���_____(����ĸ���)��
a.O2 b.H2S c.NH3 d.O3
�����о��߷����ض������£������е�NOx���Ϊ����SO2����Ҫ���ʣ�������Ϊ�������д����еĿ�������������س���ʱ��Ӧ��ȡ�������д�ʩ��ԭ����_________��
��2��ȼú�����к���NOx��SO2����ҵ�ϳ�����������(NaClO2)��ȼú����������������������
��֪:���������£�ClO2-��ת����ClO2��Cl-��ClO2�ǻ���ɫ��������ˮ�����壬����ǿ�����ԣ�������NOx��SO2��
I.��ʵ����ģ����������:����NaClO2����Һ��pHΪ5��������ͨ�뺬NO��ģ��������
�����������Ӧ����Һ�е�������ΪNO3-��Cl-����������Ӧ�����ӷ���ʽΪ_______��
���������Ч��(��NO��������)���¶ȱ仯����������ͼ��ʾ�������֪��Ϣ�������¶ȴ���50��ʱ�����¶���������Ч���½���ԭ����____________��

��.��ʵ����ģ��ͬʱ�������������:����NaClO2����Һ��pHΪ5��������ͨ�뺬SO2��NO(�����2:1)��ģ��������
���������������Ӧ����Һ�е�������ΪNO3-��SO42-��Cl-������c(SO42-)=amol/L��c(Cl-)=bmol/L����֪����Ч��Ϊ100%����������Ч��Ϊ_________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com