
| A.通入BaCl2溶液中,有白色沉淀生成 | B.通入FeCl3溶液中,有SO42-生成 |
| C.通入氯水中,有淡黄色沉淀生成 | D.通入KI溶液中,有I2生成 |
 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源:不详 题型:单选题
| A.NaHCO3和Al(OH)3 | B.BaCl2和NaCl |
| C.KClO3和K2SO4 | D.Na2SO3和BaCO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.将SO2通入Ba(OH)2溶液中观察有白色沉淀生成 |
| B.将SO2通入Ba(NO3)2溶液中观察有白色沉淀生成 |
| C.将SO2分别通入BaCl2溶液、BaCl2与HCl的混合溶液、Ba(OH)2溶液中,观察到只有Ba(OH)2中有白色沉淀生成 |
| D.将SO2通入BaCl2与NH3的混合溶液中有白色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
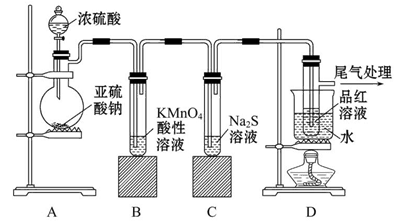
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
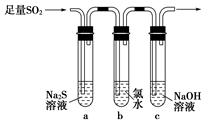
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.将蔗糖加入浓硫酸后变黑,说明浓硫酸具有脱水性 |
| B.浓硫酸可用作气体干燥剂,说明浓硫酸具有吸水性 |
| C.铜与浓硫酸共热有刺激性气味气体放出,说明浓硫酸具有强氧化性 |
| D.常温下浓硫酸可以用铝罐储存,说明铝与冷的浓硫酸不反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

| A.该Na2S2O3溶液中水电离的c(OH﹣)=10﹣8mol/L |
| B.H2S2O3是一种弱酸 |
| C.Na2S2O3是一种弱电解质 |
| D.Na2S2O3水解方程式为S2O32﹣+2H2O=H2S2O3+2OH﹣ |
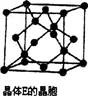
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
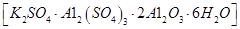 制备无水氯化铝的流程如下:
制备无水氯化铝的流程如下: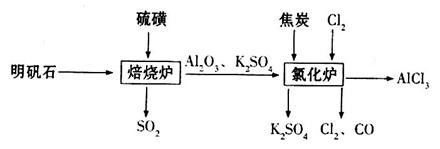
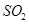 的方法是________________________________。
的方法是________________________________。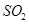 ,下列装置合理的是________(填代号)。
,下列装置合理的是________(填代号)。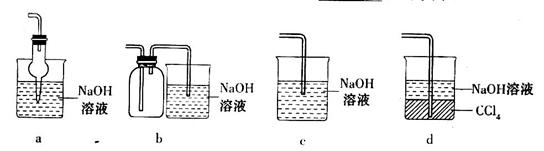
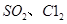 等大气污染物,若将二者按照一定比例通入水中可减少或消除污染。试设计简单实验检验二者是否恰好完全反应。(简要描述实验步骤、现象和结论)
等大气污染物,若将二者按照一定比例通入水中可减少或消除污染。试设计简单实验检验二者是否恰好完全反应。(简要描述实验步骤、现象和结论)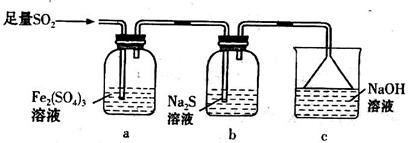
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com