
分析 (1)盐酸与氢氧化钠反应实质氢离子与氢氧根离子反应生成水,酚酞与碱显红色,与酸显无色;
(2)写出反应的化学方程式,标明物质的聚集状态,依据每生成23g NO2需要吸收16.95kJ热量,计算消耗1mol氮气吸收热量,据此书写热化学方程式;
(3)反应放出的热量与消耗反应物的物质质量成正比;
(4)①+②-2×③得到目标方程式,依据盖斯定律计算反应热,书写热化学方程式.
解答 解:(1)盐酸与氢氧化钠反应实质氢离子与氢氧根离子反应生成水,离子方程式:H++OH-=H2O,酚酞与碱显红色,与酸显无色,将稀盐酸逐滴滴入到含有酚酞的NaOH溶液中现象为:;
故答案为:红色溶液逐渐褪为无色; H++OH-=H2O;
(2)氮气与氧气反应生成二氧化氮,每生成23g NO2需要吸收16.95kJ热量,则消耗1mol氮气吸收热量为:67.8KJ,反应的热化学方程式:
N2(g)+2O2(g)=2NO2(g)△H=+67.8 kJ/mol;
故答案为:N2(g)+2O2(g)=2NO2(g)△H=+67.8 kJ/mol;
(3)已知C的燃烧热△H=-393.5kJ/mol,则24g C在O2中完全燃烧生成CO2(g)放出的热量为$\frac{24}{12}$×393.5KJ=787KJ;
故答案为:787;
(4)①CH4(g)+O2(g)?CO(g)+H2(g)+H2O(g)△H=-321.5kJ/mol
②CH4(g)+H2O(g)?CO(g)+3H2(g)△H=+250.3kJ/mol
③CO(g)+2H2(g)?CH3OH(g)△H=-90kJ/mol
依据盖斯定律,①+②-2×③得到:2CH4(g)+O2(g)=2CH3OH(g)△H=-251.2KJ/mol,
故答案为:2CH4(g)+O2(g)=2CH3OH(g)△H=-251.2KJ/mol.
点评 本题考查了离子方程式、化学方程式、热化学方程式的书写,明确化学方程式与热化学方程式区别是解题关键,注意盖斯定律计算反应热方法,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 150 mL 1mol/L氯化钠溶液 | B. | 5 mL 2mol/L 氯化铵溶液 | ||
| C. | 150 mL 1mol/L氯化钾溶液 | D. | 75 mL 1.5mol/L 氯化镁溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
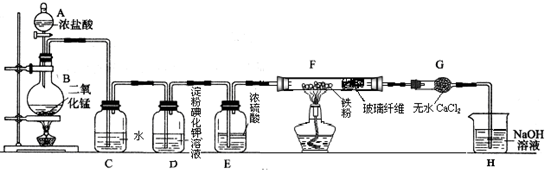
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{c(O{H}^{-})}{c({H}^{+})}$ | B. | $\frac{c(C{H}_{3}COOH)}{c(O{H}^{-})}$ | C. | c(H+)•c(OH-) | D. | OH-的物质的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,48 g O3中的氧原子数为3NA | |
| B. | 24 g金属镁变为镁离子时失去的电子数为NA | |
| C. | 4℃时9 mL水和标准状况下11.2 L氮气中的原子数均为NA | |
| D. | 2 mol•L-l的CuCl2溶液中含有的氯离子数为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体的分散质粒子直径在1nm~100nm之间 | |
| B. | 胶体粒子带电荷并且在一定条件下能稳定存在 | |
| C. | 胶体粒子不能穿过半透膜,能通过滤纸空隙 | |
| D. | 光束通过胶体时有丁达尔效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 火炬燃料丙烷充分燃烧后只生成二氧化碳和水 | |
| B. | 撑杆跳高运动员使用的碳纤维撑杆属于有机高分子材料 | |
| C. | 泳池中加入的适量漂白粉可起到杀菌消毒作用 | |
| D. | 举重和体操运动员手上涂抹的碳酸镁白色粉末可吸水防滑 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
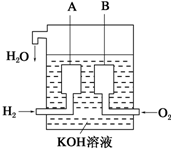 (1)对于反应:K2Cr2O7+HCl→KCl+CrCl3+Cl2↑+H2O,回答下列问题:
(1)对于反应:K2Cr2O7+HCl→KCl+CrCl3+Cl2↑+H2O,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com