
【题目】某探究小组设计如图所示装置(夹持、加热仪器略),模拟工业生产进行制备三氯乙醛(CCl3CHO)的实验。查阅资料,有关信息如下:

①制备反应原理:C2H5OH+4Cl2→CCl3CHO+5HCl
可能发生的副反应:C2H5OH+HCl→C2H5Cl+H2O
CCl3CHO+HClO→CCl3COOH(三氯乙酸)+HCl
②相关物质的相对分子质量及部分物理性质:
C2H5OH | CCl3CHO | CCl3COOH | C2H5Cl | |
相对分子质量 | 46 | 147.5 | 163.5 | 64.5 |
熔点/℃ | -114.1 | -57.5 | 58 | -138.7 |
沸点/℃ | 78.3 | 97.8 | 198 | 12.3 |
溶解性 | 与水互溶 | 可溶于水、乙醇 | 可溶于水、乙醇、三氯乙醛 | 微溶于水,可溶于乙醇 |
(1)仪器A中发生反应的化学方程式为____________。
(2)装置B中的试剂是____________,若撤去装置B,可能导致装置D中副产物____________(填化学式)的量增加;装置D可采用____________加热的方法以控制反应温度在70℃左右。
(3)装置中球形冷凝管的作用为____________,写出E中所有可能发生的无机反应的离子方程式____________。
(4)反应结束后,有人提出先将D中的混合物冷却到室温,再用过滤的方法分离出CCl3COOH。你认为此方案是否可行____________。
(5)测定产品纯度:称取产品0.40g配成待测溶液,加入0.1000molL-1碘标准溶液20.00mL,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,立即用0.02000molL-1Na2S2O3溶液滴定至终点。进行三次平行实验,测得消耗Na2S2O溶液20.00mL。则产品的纯度为____________(计算结果保留三位有效数字)。
滴定的反应原理:CCl3CHO+OH-═CHCl3+HCOO-
HCOO-+I2═H++2I-+CO2↑
I2+2S2O32-═2I-+S4O62-
(6)为证明三氯乙酸的酸性比乙酸强,某学习小组的同学设计了以下三种方案,你认为能够达到实验目的是____________
a.分别测定0.1molL-1两种酸溶液的pH,三氯乙酸的pH较小
b.用仪器测量浓度均为0.1molL-1的三氯乙酸和乙酸溶液的导电性,测得乙酸溶液的导电性弱
c.测定等物质的量浓度的两种酸的钠盐溶液的pH,乙酸钠溶液的pH较大
【答案】(1)MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
(2)饱和食盐水;C2H5Cl;水浴;
(3)冷凝回流;Cl2+2OH-=Cl-+ClO-+H2O、H++OH-=H2O;
(4)不可行;
(5)66.4%;
(6)abc
【解析】
试题分析:A装置利用二氧化锰与浓盐酸制备氯气,B装置用饱和食盐水除去HCl,C装置盛放浓硫酸干燥氯气,D中反应制备CCl4CHO,E装置盛放氢氧化钠溶液,吸收尾气中氯气、HCl防止污染空气。
(1)二氧化锰与浓盐酸在加热条件下反应生成氯化锰、氯气与水,反应方程式为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
(2)B装置用饱和食盐水除去HCl,减少副反应发生,撤去B装置,氯气中混有HCl,增大副反应C2H5OH+HCl→C2H5Cl+H2O的发生,导致装置D中副产物C2H5Cl增多,控制反应温度在70℃左右,应采取水浴加热,受热均匀,偏于控制温度,故答案为:饱和食盐水;C2H5Cl;水浴;
(3)有机物易挥发性,冷凝回流挥发的有机物;EE装置盛放氢氧化钠溶液,吸收尾气中氯气、HCl防止污染空气,反应离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O、H++OH-=H2O,故答案为:冷凝回流;Cl2+2OH-=Cl-+ClO-+H2O、H++OH-=H2O;
(4)CCl3COOH溶于乙醇与CCl3CHO,应采取蒸馏方法进行分离,故答案为:不可行,CCl3COOH溶于乙醇与CCl3CHO;
(5)根据消耗的Na2S2O3计算,剩余I2的物质的量0.02000molL-1×0.02L=2×10-4mol,与HCOO-反应的I2的物质的量为0.1000molL-1×0.02L-2×10-4mol=1.8×10-3mol,由CCl3CHO~HCOO-~I2可知,CCl3CHO的物质的量为1.8×10-3mol,则产品的纯度为![]() ×100%=66.4%,故答案为:66.4%;
×100%=66.4%,故答案为:66.4%;
(6)酸性越强,电离程度越大,溶液pH越小;电离程度越大,酸性越强,溶液中离子浓度越大,导电能力越强;酸性越弱,其钠盐的水解程度越大,溶液pH越大。a.分别测定0.1molL-1两种酸溶液的pH,三氯乙酸的pH较小,说明三氯乙酸电离程度比乙酸的大,则三氯乙酸的酸性比乙酸的强,故a正确;b.用仪器测量浓度均为0.1molL-1的三氯乙酸和乙酸溶液的导电性,测得乙酸溶液的导电性弱,三氯乙酸溶液中离子浓度更大,说明三氯乙酸电离程度比乙酸的大,则三氯乙酸的酸性比乙酸的强,故b正确;c.测定等物质的量浓度的两种酸的钠盐溶液的pH,乙酸钠溶液的pH较大,说明乙酸钠的水解程度更大,则乙酸的酸性比三氯乙酸的弱,故c正确,故选:abc。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某温度下,向某密闭容器中加入1molN2和4molH2,使之反应合成NH3,平衡后测得NH3的体积分数为m。若T不变,只改变起始加入的物质的量,使之反应平衡后NH3的体积分数仍为m,若N2、H2、NH3的加入量用X、Y、Z表示应满足:
(1)恒定T、V:
[1]若X=0,Y=1,则Z= 。
[2]若X=0.75,Y= ,Z=0.5。
[3]X、Y、Z应满足的一般条件是(分别用只含X、Z和只含Y、Z写两个方程式表示) 。
(2)恒定T、P:
[1]若X=1、Y= ,则Z=2。
[2]若X=2,则Y=10,Z= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L密闭容器中,800℃时反应2NO(g)+O2(g)![]() 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)上述反应________(填“是”或“不是”)可逆反应。
(2)如图所示,表示NO2变化曲线的是 ________。用O2表示从0~2 s内该反应的平均速率v=________。

(3)能说明该反应已达到平衡状态的是_______(填序号)。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)苯、四氯化碳、乙醇都是常见的有机溶剂。能与水互溶的是 ;难溶于水,且密度比水小的是 。
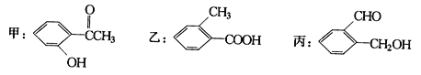
(2)现有化合物:
①请写出丙中含氧官能团的名称: 。
②请判别上述哪些化合物互为同分异构体: (填代号)。
(3)同温同压下,相同体积某烷烃的蒸气质量是氢气质量的36倍,该烃的分子式为____________,写出该烃的所有同分异构体的结构简式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2X+Y![]() 2Z,反应中ω(Z的物质的量分数)随温度T的变化如下图所示。下列判断正确的是( )
2Z,反应中ω(Z的物质的量分数)随温度T的变化如下图所示。下列判断正确的是( )

A.T 1时,v正>v逆
B.正反应的△H<0
C.a、b两点的反应速率 v( a)=v( b)
D.T<T1时,ω增大的原因是平衡向正方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有金属单质A、B、C、I和气体甲、乙、丙及物质D、E、F、G、H。其中B是地壳中含量最多的金属。它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
请根据以上信息回答下列问题:
(1)写出下列物质的化学式 甲: 乙: C: H: 。
(2)写出反应⑦的离子方程式: ________。
(3)要除去物质F中的物质G,可行的方法是( )
A.滴入KSCN溶液 B.通入足量的氯气 C.滴入NAOH溶液 D.加入过量铁粉
(4)若将D溶液滴入F溶液中,将其长时间露置于空气中观察到的现象为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用浓硫酸和乙醇制取乙烯时,常会看到烧瓶中液体变黑,制得的乙烯中混有CO2、SO2等杂质。某课外小组设计了如下装置,证明乙烯中混有CO2、SO2并验证乙烯的性质。
回答下列问题:

(1)装置A是乙烯的发生装置。图中一处明显的错误是__________,烧瓶中碎瓷片的作用是__________。
(2)若要检验A中所得气体含有SO2,可将混合合气体直接通入__________(填代号,下同)装置;若要检验,A中所得气体含有CH2=CH2,可将混合气体先通入B装置,然后通入__________装置。
(3)写出实验室制取乙烯的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳、氮广泛的分布在自然界中,碳、氮的化合物性能优良,在工业生产和科技领域有重要用途。
(1)氮化硅(Si3N4)是一种新型陶瓷材料,它可由SiO2与过量焦炭在1300~1700oC的氮气流中反应制得:3SiO2(s)+6C(s)+2N2(g) ![]() Si3N4(s)+6CO(g)。⊿H =-1591.2 kJ/mol,则该反应每转移1mole—,可放出的热量为 。
Si3N4(s)+6CO(g)。⊿H =-1591.2 kJ/mol,则该反应每转移1mole—,可放出的热量为 。
(2)某研究小组现将三组CO(g)与H2O(g)的混合气体分别通入体积为2L的恒容密闭容器中,一定条件下发生反应:CO(g)+H2O(g)![]() CO2(g)+H2(g),得到如下数据:
CO2(g)+H2(g),得到如下数据:
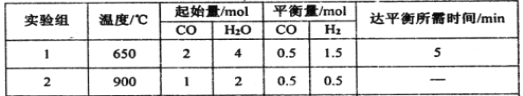
① 实验1中,前5min的反应速率v(CO2)= 。
②下列能判断实验2已经达到平衡状态的是 。
a.容器内CO、H2O、CO2、H2的浓度不再变化 b.容器内压强不再变化
c.混合气体的密度保持不变 d.v正(CO) =v逆(CO2)
e.容器中气体的平均相对分子质量不随时间而变化
③若实验2的容器是绝热的密闭容器,实验测得H2O(g)的转化率H2O%随时间变化的示意图如下图所示, b点v正 v逆(填“<”、“=”或“>”),t3~t4时刻,H2O(g)的转化率H2O%降低的原因是 。

(3)利用CO与H2可直接合成甲醇,下图是由“甲醇-空气”形成的绿色燃料电池的工作原理示意图,写出以石墨为电极的电池工作时负极的电极反应式 ,利用该电池电解1L 0.5mol/L的CuSO4溶液,当消耗560mLO2(标准状况下)时,电解后溶液的pH= (溶液电解前后体积的变化忽略不计)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】3,5-二甲氧基苯酚是重要的有机合成中间体,可用于天然物质白柠檬素的合成。一种以间苯三酚为原料的合成反应如下:

甲醇、乙醚和3,5-二甲氧基苯酚的部分物理性质见下表:
物质 | 沸点/℃ | 熔点/℃ | 密度(20℃) / g·cm-3 | 溶解性 |
甲醇 | 64. 7 |
| 0. 7915 | 易溶于水 |
乙醚 | 34. 5 |
| 0. 7138 | 微溶于水 |
3,5-二甲氧基苯酚 |
| 33-36 |
| 易溶于甲醇、乙醚,微溶于水 |
反应结束后,先分离出甲醇,再加入乙醚进行萃取。
(1)①分离出甲醇的操作是的 。
②萃取用到的分液漏斗使用前需 并洗净,分液时有机层在分液漏斗的 填(“上”或“下”)层。
(2)分离得到的有机层依次用饱和NaHCO3溶液、饱和食盐水、少量蒸馏水进行洗涤。用饱和NaHCO3 溶液洗涤的目的是 ;用饱和食盐水洗涤的目的是 。
(3)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是 (填字母)。
a.蒸馏除去乙醚 b.重结晶 c.过滤除去干燥剂 d.加入无水CaCl2干燥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com