
四种元素X、Y、Z、W位于元素周期表的前四周期,已知它们的核电荷数依次增加,且核电荷数之和为51;Y原子的L层p轨道中有2个电子;Z与Y原子的价层电子数相同;W原子的L层电子数与最外层电子数之比为4:1,其d轨道中的电子数与最外层电子数之比为5:1。
(1)Y、Z可分别与X形成只含一个中心原子的共价化合物a、b,它们的分子式分别是__________________、_____________________;杂化轨道分别是_________________、_________________;a分子的立体结构是_________________;
(2)Y的最高价氧化物和Z的最高价氧化物的晶体类型分别是______________晶体、_______________晶体;
(3)X的氧化物与Y 的氧化物中,分子极性较小的是(填分子式)_________________;
的氧化物中,分子极性较小的是(填分子式)_________________;
(4)Y与Z比较,电负性较大的是(填元素符号)_________________;
(5)W的元素符号是____________,其+2价离子的核外电子排布式是_________________。
【答案】
(1)CH4 SiH4 SP3 SP3 正四面体
(2)分子 原子
(3)CO2
(4)C
(5)Zn 1S22S22P63S23P63d10
【解析】由“ Y原子的L层p轨道中有2个电子”知其第二层有4个电子,是碳元素。由“Z与Y原子的价层电子数相同”可判断Z可能是Si或Ge。由“W原子的L层电子数与最外层电子数之比为4∶1”,判断W最外层有2个电子,由“其d轨道中的电子数与最外层电子数之比为5∶1”,判断出其d轨道有10个电子,则W是锌,30号元素,再根据“它们的核电荷数依次增加,且核电荷数之和为51”推断出X是氢元素,Z是硅元素。H2O分子是V形,是极性分子;CO2分子是直线形,是非极性分子。
Y原子的L层p轨道中有2个电子”知其第二层有4个电子,是碳元素。由“Z与Y原子的价层电子数相同”可判断Z可能是Si或Ge。由“W原子的L层电子数与最外层电子数之比为4∶1”,判断W最外层有2个电子,由“其d轨道中的电子数与最外层电子数之比为5∶1”,判断出其d轨道有10个电子,则W是锌,30号元素,再根据“它们的核电荷数依次增加,且核电荷数之和为51”推断出X是氢元素,Z是硅元素。H2O分子是V形,是极性分子;CO2分子是直线形,是非极性分子。


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
碳族元素包括:C、Si、 Ge、 Sn、Pb。
(1)碳纳米管有单层或多层石墨层卷曲而成,其结构类似于石墨晶体,每个碳原子通过 杂化与周围碳原子成键,多层碳纳米管的层与层之间靠 结合在一起。
(2)CH4中共用电子对偏向C,SiH4中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为 。
(3)用价层电子对互斥理论推断SnBr2分子中Sn—Br的键角 120°(填“>”“<”或“=”)。
(4)铅、钡、氧形成的某化合物的晶胞结构是:Pb4+处于立方晶胞顶点,Ba2+处于晶胞中心,O2-处于晶胞棱边中心,该化合物化学式为 ,每个Ba2+与 个O2-配位。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是
A.金属与盐溶液的反应都是置换反应
B.阴离子都只有还原性
C.与强酸、强碱都反应的物质只有两性氧化物或两性氢氧化物
D.分子晶体中都存在范德瓦耳斯力,可能不存在共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
某元素的一种同位素X的原子质量数为A,含N个中子,它与1H原子组成HmX分子。在a g HmX中所含质子的物质的量是
A. 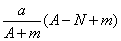 mol B.
mol B. 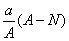 mol
mol
C. 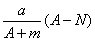 mol D.
mol D. 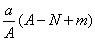 mol
mol
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素W、X、Y、Z 的原子序数依次增大,W与Y、X与Z 位于同一主族。W 与X 可形成共价化合物WX2,Y原子的内层电子总数是其最外层电子数的2.5 倍。下列叙述中不正确的是
A.WZ2分子中所有原子最外层都为8 电子结构
B.WX2、ZX2的化学键类型和晶体类型都相同
C.WX2是以极性键结合成的非极性分子
D.原子半径大小顺序为X <W<Y<Z
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是
A. 分子晶体中的每个分子内一定含有共价键
B. 原子晶体中的相邻原子间只存在非极性共价键
C. 离子晶体中可能含有共价键
D.金属晶体的熔点和沸点都很高
查看答案和解析>>
科目:高中化学 来源: 题型:
请完成下列各题:
(1)前四周期元素中,基态原子中未成对电子数与其所在周期数相同的元素有________种。
(2)第ⅢA、ⅤA族元素组成的 化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与单晶硅相似。Ga原子的电子排布式为______________。在GaN晶体中,每个Ga原子与__________个N原子相连,与同一个Ga原子相连的N原子构成的空间构型为________。在四大晶体类型中,GaN属于_______晶体。
化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与单晶硅相似。Ga原子的电子排布式为______________。在GaN晶体中,每个Ga原子与__________个N原子相连,与同一个Ga原子相连的N原子构成的空间构型为________。在四大晶体类型中,GaN属于_______晶体。
(3)在极性分子NCl3中,N原子的化合价为-3,Cl原子的化合价为+1,请推测NCl3水解的主要产物是_________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作、现象和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将干燥纯净的氯气通入装有湿润的红色纸条的试剂瓶中 | 红色褪去 | 氯气有漂白性 |
| B | 往乙醇中加入适量浓硫酸制备乙烯,并将产生的气体直接通入酸性KMnO4溶液中 | 酸性KMnO4溶液紫红色褪去 | 证明乙烯能被酸性高锰酸钾氧化 |
| C | 取少量BaSO4固体于试管中,加入足量的盐酸 | 沉淀不溶解 | BaSO4不溶于盐酸,且可以用盐酸和BaCl2溶液检验SO42- |
| D | 在分液漏斗中加入碘水后再加入CCl4,充分振荡 | 分层,且上层溶液呈紫色 | CCl4可作为碘的萃取剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com