
【题目】下列说法正确的是( )
A.石油裂化主要得到乙烯
B.热化学方程式CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H= -802.3kJ/mol中△H, 可以表示甲烷的燃烧热
C.蛋白质、纤维素、淀粉都是高分子化合物
D.煤的气化是物理变化,是高效、清洁地利用煤的重要途径
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:
【题目】CuSO4 是一种重要的化工原料,其有关制备途径及性质如图所示。
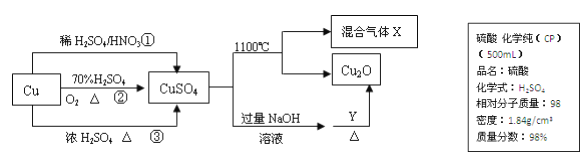
(1)现要用如上图所示的浓硫酸来配制步骤①中所需要的 1mol/L 的稀硫酸 480mL,需用这种浓硫酸的体积为________mL。(保留到小数点后 1 位)
(2)配制该稀硫酸溶液所用到的玻璃仪器除了玻璃棒、量筒、烧杯之外还有_____、_______。
(3)下列哪些操作会使所配的稀硫酸浓度减小________。
A.洗涤烧杯和玻璃棒的溶液未转入容量瓶
B.定容时,眼睛仰视溶液凹液面最低点
C. 容量瓶中原残留少量蒸馏水
D.定容摇匀后容量瓶液面低于刻度线,又加水定容到刻度线
E.量取浓硫酸时量筒内有少量蒸馏水
(4)制取硫酸铜的途径①、②、 ③中,途径______能更好地体现绿色化学思想。
(5)请写出途径③的化学反应方程式________________。
(6)配制 1000mL 0.1mol/L 的硫酸铜溶液,需用托盘天平称取_______g 胆矾。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中进行反应:2SO2(g)+O2(g) ![]() 2SO3(g).已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.4mol/L、0.2mol/L、0.4mol/L.当反应达到平衡时,可能存在的数据是( )
2SO3(g).已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.4mol/L、0.2mol/L、0.4mol/L.当反应达到平衡时,可能存在的数据是( )
A.SO2为0.8mol/L,O2为0.4 mol/L
B.SO2为0.5 mol/L
C.SO3为0.8 mol/L
D.SO2、SO3均为0.3 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pH都等于9的NaOH和CH3COONa两种溶液中,设由水电离产生的OH-浓度分别为amol·L-1与bmol·L-1,则a和b的关系为
A. a>b B. a=10-4b C. b=10-4a D. a=b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学学习小组设计了两组实验来探究元素周期律. 一组同学为验证卤素单质氧化性的相对强弱,用如图所示装置进行实验(夹持仪器已略去,气密性已检验).
实验过程及现象:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸.
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹.
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a.
Ⅳ.打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下D振荡.静
置后CCl4层溶液变为紫红色.
请回答下列有关问题:
(1)验证氯气的氧化性强于碘的实验现象是 .
(2)B和C仪器口盛放浸有NaOH溶液的棉花的作用 .
(3)过程Ⅲ实验的目的是 .
(4)由此实验得出的结论:同主族元素从上到下,原子半径逐渐增大,得电子能力逐渐(填“减弱”或“增强”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知正四面体型分子E和单质分子G反应,生成四面体型分子L和分子M(组成E分子的元素的原子序数小于10,组成G分子的元素为第三周期的元素),如图,则下列判断中不正确的是( ) 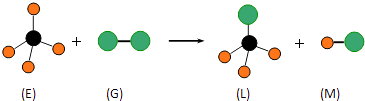
A.常温常压下,E、L均为气态有机物
B.E是一种含有10个电子的分子
C.上述反应的类型是置换反应
D.上述4种物质中有3种为共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子能在溶液中大量共存的是( )
A. Ag+、K+、NO3-、C1- B. Mg2+、Na+、Cl-、SO42-
C. NH4+、Cu2+、OH一、Cl— D. H+、Na+、HCO3-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用石墨电极完成下列电解实验
实验一 | 实验二 | |
装置 |
|
|
现象 | a、d处试纸变蓝;b处变红,局部褪色;c处无明显变化 | 两个石墨电极附近有气泡产生;n处有气泡产生…… |
下列对实验现象的解释或推测不合理的是( )
A. a、d处:2H2O+2e-=H2↑+2OH- B. b处:2Cl--2e-=Cl2↑
C. c处发生了反应:Fe-2e-=Fe2+ D. 根据实验一的原理,实验二中m处能析出铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关热化学方程式的叙述正确的是( )
A. 已知2H2(g)+O2(g)=2H2O(g);△H=﹣483.6kJ/mol,则氢气的燃烧热为241.8kJ
B. 已知4P(红磷,s)=P4(白磷,s);△H>0,则白磷比红磷稳定
C. 含20.0g NaOH的稀溶液与稀硫酸完全中和,放出28.7kJ的热量,则表示该反应中和热的热化学方程式为:NaOH(aq)+ ![]() H2SO4(aq)=
H2SO4(aq)= ![]() Na2SO4(aq)+H2O(l);△H=﹣57.4kJ/mol
Na2SO4(aq)+H2O(l);△H=﹣57.4kJ/mol
D. 己知C(s)+O2(g)=CO2(g);△H1 C(s)+ ![]() O2(g)=CO(g);△H2 则△H1>△H2
O2(g)=CO(g);△H2 则△H1>△H2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com