
| A. | 11.11 | B. | 22.22 | C. | 30.00 | D. | 32.00 |
分析 设气体总质量为100g,根据质量分数计算各自质量,再根据n=$\frac{m}{M}$计算各自物质的量,根据M=$\frac{m}{n}$计算混合气体的平均摩尔质量,由ρ=$\frac{M}{{V}_{m}}$可知,气体的摩尔质量之比等于密度之比,以此解答该题.
解答 解:设气体总质量为100g,则m(O2 )=32g,m(N2)=28g,m(CO2)=22g,m(CH4)=16g,m(H2)=2g,
故n(O2)=$\frac{32g}{32g/mol}$=1mol,n(N2)=$\frac{28g}{28g/mol}$=1mol,n(CO2)=$\frac{22g}{44g/mol}$=0.5mol,n(CH4)=$\frac{16g}{16g/mol}$=1mol,n(H2)=$\frac{2g}{2g/mol}$=1mol,
则平均摩尔质量=$\frac{100g}{(1+1+0.5+1+1)mol}$=22.22g/mol,
由ρ=$\frac{M}{{V}_{m}}$可知,气体的摩尔质量之比等于密度之比,则此混合气体对氢气的相对密度为$\frac{22.22}{2}$=11.11,
故选A.
点评 本题考查物质的量的相关计算,侧重于学生的分析能力和计算能力的考查,注意把握相关计算公式的运用,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 氮化碳的化学式为C4N3 | |
| B. | 氮化碳的晶体类型为离子晶体 | |
| C. | 构成氮化碳晶体的微粒是碳原子和氮原子,且构成空间网状结构 | |
| D. | 氮化碳晶体中存在的微粒间的作用力有共价键和分子间作用力 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 牛油、纤维素和蛋白质都是天然高分子化合物 | |
| B. | 淀粉水解的最终产物是葡萄糖 | |
| C. | 葡萄糖能发生氧化反应和水解反应 | |
| D. | 浓硫酸溅在皮肤上,使皮肤呈黄色是由于浓硫酸和蛋白质发生了颜色反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素周期表有8个主族 | B. | 0族原子的最外层电子数均为8 | ||
| C. | ⅠA族的元素全是金属元素 | D. | 短周期是指第1、2、3周期 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
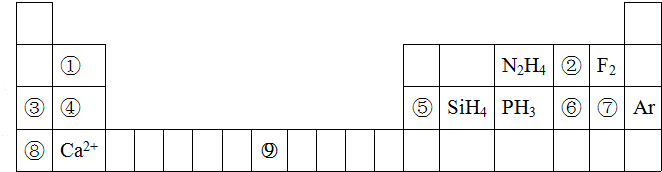
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氨水 | B. | 氢氧化钠 | C. | 酸性高锰酸钾 | D. | 盐酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com