
 、CO32-、OH
、CO32-、OH 和SO
和SO 。请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑盐类的水解).
。请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑盐类的水解). L-1 H2SO4 b.0.01mol
L-1 H2SO4 b.0.01mol L-1 KMnO4 c.1mol
L-1 KMnO4 c.1mol L-1 BaCl2
L-1 BaCl2| 实验步骤 |  预期现象和结论 预期现象和结论 |
步骤1:取少量吸收液于试管中,滴加3 mol L-1 H2SO4至溶液呈酸性,然后将所得溶液分置于A、B试管中。 L-1 H2SO4至溶液呈酸性,然后将所得溶液分置于A、B试管中。 | |
| 步骤2:向A试管中滴加1~2滴 (填序号)。 | 若溶液 ,则假设1成立。 否则,则假设2或3成立。 |
| 步骤3:向B试管中滴加1~2滴 (填序号)。 | 若溶液 ,则假设3成立。 否则,结合步骤2,则假设2成立。 |
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
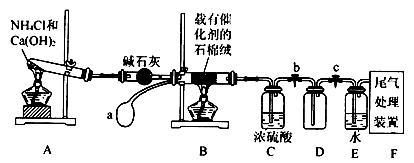
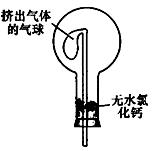
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
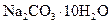 晶体配制
晶体配制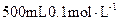 的
的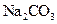 溶液,请回答下列问题。
溶液,请回答下列问题。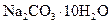 晶体_______g。
晶体_______g。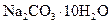 晶体是__________g。
晶体是__________g。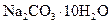 晶体已失去部分结晶水。____________
晶体已失去部分结晶水。____________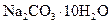 晶体中混有少量
晶体中混有少量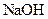 固体,且用所配制的
固体,且用所配制的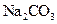 溶液与盐酸反应来测定某盐酸的物质的量浓度,所测盐酸的浓度会________。(填“偏高”、“偏低”、“不变”。)
溶液与盐酸反应来测定某盐酸的物质的量浓度,所测盐酸的浓度会________。(填“偏高”、“偏低”、“不变”。)查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
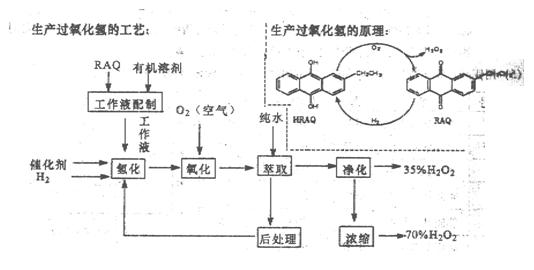
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
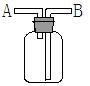

A.A口进气,B口排气,用于收集H2 | B.广口瓶中充满水,从A口进气用于收集O2 | C.广口瓶中盛有浓硫酸,从B口进气用于干燥SO2气体 | D.广口瓶中盛有NaOH水溶液,从B口进气用于除去Cl2中的HCl气体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.容量瓶中原有少量蒸馏水 |
| B.溶液从烧杯转移到容量瓶中后没有洗涤烧杯 |
| C.定容时观察液面俯视 |
| D.定容时倒转容量瓶几次,发现凹液面最低点低于标线,再补几滴水到标线 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com