
【题目】短周期元素W、X、Y和Z的原子序数依次增大,元素W是制备一种高效电池的重要材料, X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最丰富的金属元素,Z原子的最外层电子数是其电子层数的2倍。下列说法错误的是 ( )
A. 元素Z可与元素X形成共价化合物XZ2
B. 元素X与氢形成的原子比为1:1的化合物有很多种
C. 元素W、X的氯化物中,各原子均满足8电子的稳定结构
D. 元素Y的单质与氢氧化钠溶液或盐酸反应均有氢气生成
【答案】C
【解析】元素W是制备一种高效电池的重要材料,W为Li元素;X原子的最外层电子数是内层电子数的2倍,X为C元素;Y为Al元素;Z原子的最外层电子数是其电子层数的2倍,且Z原子序数大于X,可知Z为S元素。
A、碳与硫元素形成CS2化合物,只含共价键,属于共价化合物,A正确。B、碳与氢形成的化合物属于有机化合物中的烃类,形成1:1的化合物有很多种 如C2H2、C6H6等,B正确。C、锂与氯形成的化合物LiCl的电子式为![]() ,氯原子周围有8个电子,而锂原子周围只有2个电子;碳与氯形成的的化合物为CCl4,电子式为
,氯原子周围有8个电子,而锂原子周围只有2个电子;碳与氯形成的的化合物为CCl4,电子式为 ,每个原子周围都达到8电子稳定结构,C错误。D、铝既能与酸反应也能与碱反应,均产生氢气,2Al+6HCl=2AlCl3+3H2↑,2Al+2NaOH+2H2O=2NaAlO2+3H2↑,D 正确。正确答案为C
,每个原子周围都达到8电子稳定结构,C错误。D、铝既能与酸反应也能与碱反应,均产生氢气,2Al+6HCl=2AlCl3+3H2↑,2Al+2NaOH+2H2O=2NaAlO2+3H2↑,D 正确。正确答案为C


 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:
【题目】按下面的实验过程完成下题:

(1)写出上述过程颜色变化(a)________;(b)______;(d)________。
(2)写出上述反应的化学方程式:(1)____________;(3)_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属硫化物和硫酸盐在工农业生产中有广泛应用。
(1)二硫化钼(MoS2)是重要的固体润滑剂。
向体积为2L的恒容密闭容器中加入0.1molMoS2、0.2molNa2CO3,并充入0.4molH2,
发生反应:MoS2(s)+2Na2CO3(s)+4H2(g)![]() Mo(s) +2CO(g) + 4H2O(g) + 2Na2S(s) △H =akJ mol-1,测得在不同温度下达到平衡时各气体的物质的量分数如图所示。
Mo(s) +2CO(g) + 4H2O(g) + 2Na2S(s) △H =akJ mol-1,测得在不同温度下达到平衡时各气体的物质的量分数如图所示。

①a________0(填“<”“>”“=”,下同)。
②容器内的总压:P点________Q点。
③P点对应温度下,H2的平衡转化率为________,平衡常数K=________。
(2)辉铜矿(主要成分是Cu2S)在冶炼过程中会产生大量的SO2。已知冶炼过程中部分反应为:
①2Cu2S(s)+3O2(g)=2Cu2O(s)+2SO2(g) △H=-768.2kJ/mol
②2Cu2O+Cu2S(s)=6Cu(s)+SO2(g) △H=+116kJ/mol,则Cu2S与O2反应生成Cu与SO2的热化学方程式为___________________________。
(3)回收处理SO2的方法之一是用氨水将其转化为NH4HSO3。已知常温下 Kb(NH3H2O) =1.5×l0-5 Ka1(H2SO3) =1.6×l0-2 Ka2(H2SO3)=1×10-7,若吸收过程中氨水与SO2恰好完全反应,则所得溶液在常温下的pH________7(填“>”“ <”或“=”,下同),溶液中c(SO32-)________c(H2SO3)。

(4)在500℃下硫酸铵分解会得到4种产物,其含氮物质的物质的量随时间的变化如上图所示。则该条件下硫酸铵分解的化学方程式为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于盐类水解反应说法正确的是
A.任何盐都可发生水解反应
B.盐只能发生水解反应而不能发生其他反应
C.盐水解反应肯定能破坏水的电离平衡且促进水的电离
D.盐的水溶液为中性时,则盐一定不发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. O3是由3个氧原子构成的化合物
B. 稀H2SO4能导电,所以稀H2SO4是电解质
C. 根据交叉分类法MgSO4既是镁盐又是硫酸盐
D. 根据是否有丁达尔效应将分散系分为溶液、胶体和浊液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种物质之间有下图所示的转化关系.已知:A是空气中的主要成分,B、C、D均为化合物,且C为红棕色气体.
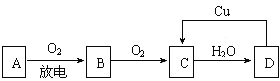
请回答下列问题:
(1)写出A和C的名称或化学式:A_________________,C________________;
(2)在上图D→C的过程中,D表现出强__________________(填“氧化性”或“还原性”);
(3)在D的稀溶液中滴入NaOH溶液,其反应的离子方程式是_________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列操作或试剂的选择合理的是
A.铁丝能代替铂丝来做焰色反应实验
B.容量瓶用蒸馏水洗涤后须烘干才能使用
C.用分液漏斗分离苯和CCl4混合物
D.用Ba(OH)2溶液鉴别SO2和CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了除去硫酸铜溶液中含有的Fe2+杂质,先加入合适的氧化剂使Fe2+氧化为Fe3+,最适合的氧化剂是
A.H2O2水溶液 B.KMnO4溶液
C.Cl2水溶液 D.HNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的CO2气体通入2L未知浓度的NaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的气体与HCl的物质的量的关系如图所示(忽略气体的溶解和HCl的挥发),下列说法不正确的是

A.O点溶液中所含溶质的化学式为NaOH、Na2CO3
B.a点溶液中c (HCO3-) > c (CO32-)
C.标准状况下,通入CO2的体积为44.8L
D.原NaOH溶液的物质的量浓度为5mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com