
 (1)分子式为C8H10,含有苯环的同分异构体有4种;其中苯环上的一个氢原子被氯原子取代后产生同分异构体数目最少的是
(1)分子式为C8H10,含有苯环的同分异构体有4种;其中苯环上的一个氢原子被氯原子取代后产生同分异构体数目最少的是 ; (填结构简式)
; (填结构简式)分析 (1)分子式为C8H10,该烃含苯环的结构,为苯的同系物,为乙苯或二甲苯,二甲苯有邻、间、对三种;苯环上的一个氢原子被氯原子取代后产生同分异构体数目最少,为对二甲苯;
(2)根据烷烃的通式CnH(2n+2)和B的分子中含有200个氢原子计算;
(3)根据同温同压下,体积比等于物质的量之比,再根据氢原子守恒计算出n;
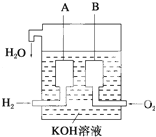
(4)①负极失去电子发生氧化反应,正极得到电子发生还原反应,据此进行判断;
②根据X、Y电极形成该电池的总反应的离子方程式;
③根据燃料电池中负极失去电子,化合价升高,正极得到电子,化合价降低以及正极的电极反应式,注意电解质溶液为氢氧化钾.
解答 解:烃的分子式为C8H10,该烃含苯环的结构,为苯的同系物,为乙苯或二甲苯,二甲苯有邻、间、对三种,故4种同分异构体;
苯环上的一个氢原子被氯原子取代后产生同分异构体数目最少,则两个甲基处于苯环的对位,应该为对二甲苯,其结构简式为: ,
,
故答案为:4; ;
;
(2)烷烃B的分子中含有200个氢原子,即2n+2=200,解得:n=99,所以B的分子式为:C99H200,
故答案为:C99H200;
(3)1L烷烃D的蒸气完全燃烧时,生成同温、同压下15L水蒸气,根据氢原子守恒,所以烷烃D分子中含30个氢原子,即2n+2=30,n=14,所以D的分子式为:C14H30,
故答案为:C14H30;
(4)①X极锌失去电子生成锌离子,化合价升高发生氧化反应,则X为负极,
故答案为:负;
②将X极和Y极的电极反应式相加可得该反应的总反应为:Zn+2MnO2+2NH4+=Zn2++Mn2O3+2NH3+H2O,
故答案为:Zn+2MnO2+2NH4+=Zn2++Mn2O3+2NH3+H2O;
③因燃料电池的总反应为:2H2+O2=2H2O,负极失去电子发生氧化反应,则负极通入的是H2,电解质为氢氧化钾溶液,则负极氢气生成电子与氢氧根离子结合生成水,负极的电极反应式为:H2-2e-+2OH-=2H2O,
故答案为:H2-2e-+2OH-=2H2O.
点评 本题考查了原电池工作原理、有机层分子式、结构简式的确定,题目难度中等,明确原电池工作原理及常见有机物结构与性质为解答关键,试题培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | BaCl2溶液 | B. | Ba(NO3)2溶液 | ||
| C. | BaCl2溶液和稀H2SO4 | D. | BaCl2溶液和稀盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
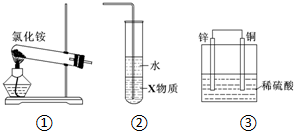
| A. | 实验室用装置①制取氨气 | |
| B. | 装置②中X若为四氯化碳,可用于吸收氨气,并防止倒吸 | |
| C. | 装置③是电解池,Cu上产生气泡 | |
| D. | 装置③是原电池,锌电极为阴极,发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去乙烷中少量的乙烯:通过溴的四氯化碳溶液洗气 | |
| B. | 除去乙酸乙酯中少量的乙酸:先加入氢氧化钠溶液后再分液 | |
| C. | 除去乙醇中少量的乙酸:加足量生石灰,蒸馏 | |
| D. | 除去溴苯中混有的少量苯:加入液溴和铁粉后过滤 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com