
下列离子在溶液中能大量共存的一组是( )
A.Fe2+、H+、ClO-、SO32- B.K+、Al3+、Cl-、CO32-
C.Na+、Ca2+、HCO3-、OH- D.Fe2+、NH4+、NO3-、SO42-
 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值。下列叙述正确的是
A.0.1mol Fe在过量的C12中充分燃烧,转移的电子数为0.3NA
B.常温下,22.4L甲烷中含有的共价键数目为4NA
C.2mol SO2和1mol O2在密闭容器中催化加热,充分反应后,容器内分子总数为2NA
D.由CO2和O2组成的混合气体中共有NA个分子,其中的氧原子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
某原子核内的质子数为m,中子数为n,则下述论断正确的是( )
A.原子核内中子的总质量小于质子的总质量;
B.该原子的质量数等于m-n;
C.该元素的相对原子质量近似等于m+n;
D.该原子的相对原子质量近似等于m+n。
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A元素的离子不含电子;B元素的最高价氧化物对应水化物与其氢化物能反应生成盐F;D与A同主族,且与E同周期;E元素原子的最外层电子数是其次外层电子数的3/4,A、B、D、E这四种元素,每一种与C元素都能形成元素的原子个数比不相同的若干种化合物。请回答下列问题:
⑴ C元素在元素周期表中的位置是____________。
⑵ C和E两种元素相比较,非金属性较强的是(填元素名称)____________,可以验证该结论的是(填写编号)______________。
A.比较这两种元素的常见单质的沸点
B.比较这两种元素的单质与氢气化合的难易
C.比较这两种元素的气态氢化物的稳定性
⑶ A、C、E间可形成甲、乙两种微粒,它们均为-1价双原子阴离子,且甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为
_______________________________。
⑷ F含有的化学键类型是______________,请用相关的离子方程式表示其与KOH稀溶液之间的反应____________________________________。
⑸ D和C形成的一种化合物能与A和C形成的一种化合物反应产生C单质,该过程的化学方程式为__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
丁子香酚结构简式如图:
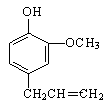
丁子香酚的一种同分异构体:对—甲基苯甲酸乙酯(F)是有机化工原料,用于合成药物的中间体。某校兴趣小组提出可以利用中学所学的简单有机物进行合成,A的产量标志着一个国家石油化工发展水平。其方案如下:
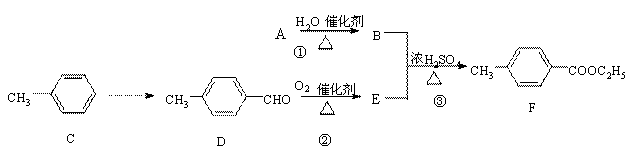
(1)写出丁子香酚的分子式 含有官能团的名称 。
(2)指出化学反应类型:① ;② 。
(3)下列物质不能与丁子香酚发生反应的是 (填序号)。
a.NaOH溶液 b.NaHCO3溶液 c.Br2的四氯化碳溶液 d.乙醇
(4)写出反应③的化学反应方程式: 。
(5)写出符合①含有苯环;②能够发生银镜反应的D的同分异构体: 。(只答对一种即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:C(s)+H2O(g)===CO(g)+H2(g) ΔH=a kJ·mol-1
2C(s)+O2(g)===2CO(g) ΔH=-220 kJ·mol-1
H—H、OO和OH键的键能分别为436 kJ·mol-1、496 kJ·mol-1和462 kJ·mol-1,则a为( )
A.-332 B.-118
C.+350 D.+130
查看答案和解析>>
科目:高中化学 来源: 题型:
用FeCl3酸性溶液脱除H2S后的废液,通过控制电压电解得以再生。某同学使用石墨电极,在不同电压(x)下电解pH=1的0.1 mol/L FeCl2溶液,研究废液再生机理。记录如下(a、b、c代表电压值):
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| Ⅰ | x≥a | 电极附近出现黄色,有气泡产生 | 有Fe3+、有Cl2 |
| Ⅱ | a>x≥b | 电极附近出现黄色,无气泡产生 | 有Fe3+、无Cl2 |
| Ⅲ | b>x>0 | 无明显变化 | 无Fe3+、无Cl2 |
(1)用KSCN溶液检验出Fe3+的现象是________。
(2)Ⅰ中,Fe3+产生的原因还可能是Cl-在阳极放电,生成的Cl2将Fe2+氧化。写出有关反应的离子方程式:________________________________________________。
(3)由Ⅱ推测,Fe3+产生的原因还可能是Fe2+在阳极放电。原因是Fe2+具有________性。
(4)Ⅱ中虽未检验出Cl2,但Cl-在阳极是否放电仍需进一步验证。电解pH=1的NaCl溶液做对照实验,记录如下:
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| Ⅳ | a>x≥c | 无明显变化 | 有Cl2 |
| Ⅴ | c>x≥b | 无明显变化 | 无Cl2 |
①NaCl溶液的浓度是________mol/L。
②Ⅳ中检验Cl2的实验方法:_____________________________________________________________________。
③与Ⅱ对比,得出的结论(写出两点):______________________________________________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com