
 2CrO42—+2H+平衡左移,导致Ag2CrO4沉淀过迟,影响实验结果
2CrO42—+2H+平衡左移,导致Ag2CrO4沉淀过迟,影响实验结果 实验数据 实验数据实验序号 | FeSO4溶液体积读数/mL | |
| 滴定前 | 滴定后 | |
| 第一次 | 0.10 | 16.20 |
| 第二次 | 0.30 | 15.31 |
| 第三次 | 0.20 | 15.19 |
 2CrO42—+2H+平衡左移,导致Ag2CrO4沉淀过迟,影响实验结果
2CrO42—+2H+平衡左移,导致Ag2CrO4沉淀过迟,影响实验结果

科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.CH3OH(l) + 3/2O2(g) ="=" CO2(g) + 2H2O(l); △H =" +726.5KJ/mol" |
| B.CH3OH(l) + 3/2O2(g) ="=" CO2(g) + 2H2O(l); △H =" -726.5KJ/mol" |
| C.CH3OH(l) + 3/2O2(g) ="=" CO2(g) + 2H2O(g); △H =" -675.3KJ/mol" |
| D.2CH3OH(l) + 3O2(g) ="=" 2CO2(g) + 4H2O(l); △H = -1453KJ/mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.a=b |
| B.混合溶液的PH=7 |
| C.混合溶液中,c(H+)+ c(B+)= c(OH-)+ c(A-) |
D.混合溶液中,c(H+)= |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
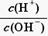 =1010,请回答下列问题:
=1010,请回答下列问题:A.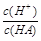 | B.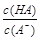 | C.c(H+)·c(OH-) | D.c(OH-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.10a+b-12 % | B.10a+b-14 % | C.1012-a-b % | D.1014-a-b % |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.11 : 1 | B.12 : 11 | C.9 : 2 | D.9: 1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.95℃纯水的pH<7,说明加热可导致水呈酸性 |
| B.pH=3的醋酸溶液,稀释至10倍后pH=4 |
| C.0.2 mol?L-1的盐酸,与等体积水混合后pH=1 |
| D.pH=3的醋酸溶液,与pH=11的氢氧化钠溶液等体积混合后pH=7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com