
| 一定条件 |
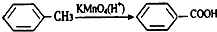
 (苯胺,弱碱性,易氧化)
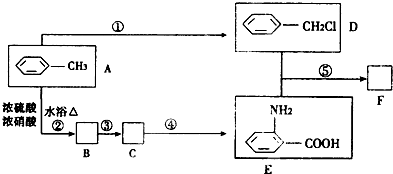
(苯胺,弱碱性,易氧化)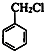 ,由A系列反应得到E,反应中引入-COOH、-NH2,且处于邻位,甲基氧化得到-COOH,由题目信息可知,-NO2还原得到-NH2,由于苯胺易被氧化,所以用KMnO4(H+)先氧化-CH3成-COOH,再将-NO2还原得到-NH2,故A转化得到B是甲苯的硝化反应,可知B为
,由A系列反应得到E,反应中引入-COOH、-NH2,且处于邻位,甲基氧化得到-COOH,由题目信息可知,-NO2还原得到-NH2,由于苯胺易被氧化,所以用KMnO4(H+)先氧化-CH3成-COOH,再将-NO2还原得到-NH2,故A转化得到B是甲苯的硝化反应,可知B为 ,C为
,C为 ,D和E发生取代反应,由信息Ⅰ可知生成F为
,D和E发生取代反应,由信息Ⅰ可知生成F为 ,据此解答.
,据此解答. ,由A系列反应得到E,反应中引入-COOH、-NH2,且处于邻位,甲基氧化得到-COOH,由题目信息可知,-NO2还原得到-NH2,由于苯胺易被氧化,所以用KMnO4(H+)先氧化-CH3成-COOH,再将-NO2还原得到-NH2,故A转化得到B是甲苯的硝化反应,可知B为
,由A系列反应得到E,反应中引入-COOH、-NH2,且处于邻位,甲基氧化得到-COOH,由题目信息可知,-NO2还原得到-NH2,由于苯胺易被氧化,所以用KMnO4(H+)先氧化-CH3成-COOH,再将-NO2还原得到-NH2,故A转化得到B是甲苯的硝化反应,可知B为 ,C为
,C为 ,D和E发生取代反应,由信息Ⅰ可知生成F为
,D和E发生取代反应,由信息Ⅰ可知生成F为 ,
, ,故答案为:
,故答案为: ;
; ,
, ;
;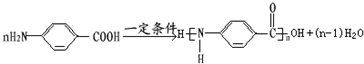 ,
, ;
;

 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:
| A、化学反应过程中,分子的种类和数目一定发生改变 |
| B、如果某化学反应的△H和△S均小于0,则反应一定能自发进行 |
| C、化学反应过程中,一定有化学键的断裂和形成 |
| D、放热反应的反应速率,一定比吸热反应的反应速率快 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 粒子代码 | a | b | c | d | e | f | g |
| 原子核数 | 单核 | 单核 | 双核 | 多核 | 单核 | 多核 | 多核 |
| 电荷数(单位电荷) | 0 | 1+ | 1- | 0 | 2+ | 1+ | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H+、Na+、NO3-、Cu2+ |
| B、Ba2+、Mg2+、Cl-、SO42- |
| C、Mg2+、K+、OH-、NO3- |
| D、NO3-、SO42-、K+、Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
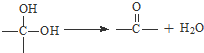
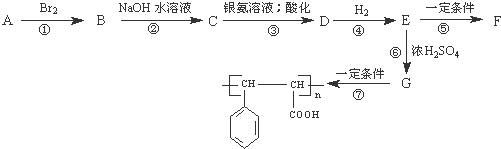
查看答案和解析>>
科目:高中化学 来源: 题型:
| 滴定 次数 | 样品的质量/g | 稀盐酸的体积/mL | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 0.320 0 | 1.02 | 21.03 |
| 2 | 0.320 0 | 2.00 | 21.99 |
| 3 | 0.320 0 | 0.20 | 20.20 |
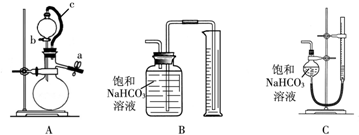
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、v(A)=0.3 mol?L-1?min-1 |
| B、v(B)=0.6 mol?L-1?s-1 |
| C、v(C)=0.5 mol?L-1?min-1 |
| D、v(A)=0.1 mol?L-1?s-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com