
【题目】对于某一可逆反应,改变下列条件,一定能使化学平衡发生移动的是( )
A. 增加某反应物的质量B. 使用催化剂
C. 降低反应体系的压强D. 升高温度
科目:高中化学 来源: 题型:
【题目】某核素![]() 的氯化物XCl2 9.5 g配成溶液后,需要1 mol/L的硝酸银溶液200 mL才能把氯离子完全沉淀下来。
的氯化物XCl2 9.5 g配成溶液后,需要1 mol/L的硝酸银溶液200 mL才能把氯离子完全沉淀下来。
(1)写出![]() 的具体符号____________。
的具体符号____________。
(2)若X的核内中子数为12,求4.75 g XCl2中所含质子的物质的量是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据元素周期表和元素周期律,判断下列叙述不正确的是

A. 气态氢化物的稳定性:H2O>NH3>SiH4
B. 氢元素与其他元素可形成共价化合物或离子化合物
C. 上图所示实验可证明元素的非金属性:Cl>C>Si
D. 用中文“![]() ”(ào)命名的第118号元素在周期表中位于第七周期0族
”(ào)命名的第118号元素在周期表中位于第七周期0族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家最近研制出可望成为高效火箭推进剂的N(NO2)3(如下图所示)。已知该分子中N-N-N键角都是108.1°,下列有关N(NO2) 3的说法正确的是
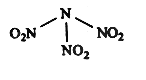
A.分子中N、O间形成的共价键是非极性键 B.分子中四个氮原子共平面
C.该物质既有氧化性又有还原性 D.15.2g该物质含有6.02×1022个原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期元素A、B、C、D的性质或结构信息如下:
信息:①原子半径:A>B>C>D ②四种元素之间形成的某三种分子的比例模型及部分性质如下:
甲:![]() 是地球上最常见的物质之一,是所有生命体生存的重要资源,约占人体体重的三分之二.
是地球上最常见的物质之一,是所有生命体生存的重要资源,约占人体体重的三分之二.
乙:![]() 无色,无气味并且易燃.是常见的一种基础能源,17年5月18日,我国首次开采成功它的水合物并连续产量,可解千年能源之忧。
无色,无气味并且易燃.是常见的一种基础能源,17年5月18日,我国首次开采成功它的水合物并连续产量,可解千年能源之忧。
丙:![]() 有强氧化性的弱酸,可以用于消毒杀菌.
有强氧化性的弱酸,可以用于消毒杀菌.
请根据上述信息回答下列问题.
(1)B元素在元素周期表中的位置为_____,请写出BC2分子的电子式:______.
(2)A、E、F在同一周期,E元素的单质还原性最强,F元素的某些盐类常用作净水剂.E单质与甲反应有化合物X生成.请写出以下两个反应的离子方程式:
①A元素的单质与物质甲发生反应:________________________________.
②F、C两种元素组成的化合物Y可作为耐高温结构的材料,X与Y两种化合物在溶液中发生反应的离子方程式:_________________________________________________.
(3)物质丁的元素组成和甲相同,丁分子具有18电子结构.向盛有一定浓度丁溶液的试管中,逐滴加入硫酸酸化的硫酸亚铁溶液.滴加过程中的现象为:①试管中溶液变成深棕黄色,②开始有少量气泡出现(经验证是氧气),片刻后反应变得剧烈,继续滴加溶液,静置一段时间,试管底部出现红褐色沉淀.请回答“片刻后反应变得剧烈”的原因
a_____________________b_________________.
(4)物质戊的元素组成和乙相同,戊分子具有18电子结构.与乙互为同系物,则戊的氯取代有机物的共________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在体积一定的密闭容器中加入1mol N2和3mol H2发生反应:N2+3H2![]() 2NH3(正反应是放热反应).下列有关说法正确的是
2NH3(正反应是放热反应).下列有关说法正确的是
A. 升高温度能加快反应速率
B. 1mol N2和3mol H2的总能量低于2mol NH3的总能量
C. 达到化学反应限度时,生成2molNH3
D. 平衡时各组分含量之比一定等于3:1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】晶体具有规则的几何外形,晶体中最基本的重复单元称之为晶胞。NaCl晶体的晶胞如图所示。随着科学技术的发展,测定阿伏伽德罗常数的手段越来越多,测定精确度也越来越高。现有一简单可行的测定方法,具体步骤如下:①将固体食盐研细,干燥后,准确称取mgNaCl固体并转移到定容仪器A中。②用滴定管向仪器A中加苯,并不断振荡,继续加苯至A仪器的刻度线,计算出NaCl固体的体积为VmL。回答下列问题:
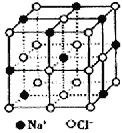
(1)步骤①中A仪器最好用_________(填仪器名称)
(2)能否用胶头滴管代替步骤②中的滴定管________,其原因是____________。
(3)经X射线衍射测得NaCl晶胞中最邻近的Na+和Cl-平均距离为acm,则利用上述方法测得的阿伏伽德罗常数的表达式为NA=________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列设计的实验方案能达到相应实验目的是( )
选项 | 实验目的 | 实验方案 |
A | 蛋白质发生了变性 | 向蛋白质溶液中加入CuCl2或(NH4)2SO4饱和溶液 |
B | 证明反应速率会随反应物浓度的增大而加快 | 用3mL稀硫酸与足量纯锌反应,产生气泡速率较慢,然后加入1mL 1mol·Lˉ1CuSO4溶液,迅速产生较多气泡 |
C | 比较Ksp(BaCO3)、Ksp(BaSO4) | 常温下,向饱和Na2CO3溶液中加少量BaSO4粉末,过滤,向洗净的沉淀中加稀盐酸,有气泡产生 |
D | 通过观察液面差判断该装置的气密性 |
|
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,圆底烧瓶中充满干燥的氯气,将胶头滴管中的浓氨水挤入圆底烧瓶中,发生反应:2NH3+3Cl2=N2+6HCl,同时生成白烟并发红光。回答下列问题。
(1)实验室制氨气的化学反应方程式是:____________________________。
(2)在2NH3+3Cl2=N2+6HCl反应中,氨气表现了___________的化学性质, 请列举出NH3的另一个化学性质:__________________________。
(3)实验中生成的白烟是_____________________。
(4)反应完成后,将导管插入烧杯的水面下,并打开止水夹,观察到有水吸入烧瓶中形成喷泉,当喷泉停止后,烧瓶___________(填“能”或“不能”)被水充满。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com