
(12分)下图是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质被略去。反应①常被应用于野外焊接钢轨,②是工业上重要的反应之一。
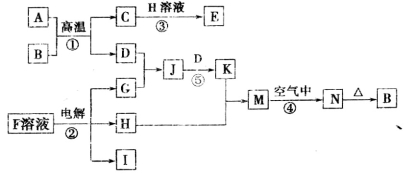
请回答下列问题:
(1)H中含有的化学键类型是________________________。
(2)上述框图所示的反应中,既属于化合反应,又属于氧化还原反应的反应共有______个;反应③的离子方程式____________________________。
(3)25℃时,以Pt为电极电解含有少量酚酞的F的饱和溶液,若在溶液变红的一极收集到0.2 g气体,则此时溶液的pH是_______(假设溶液的体积为2 L且不考虑电解后溶液体积的变化)。
(4)J溶液显_______(填“酸”、“碱”或“中”)性,原因是_________________________。(用离子方程式表示)
(12分)(1)共价键、离子键(2分)
(2)3(2分);Al2O3+2OH-+3H2O=2[Al(OH)4]- (2分)
(3)13(2分)
(4)酸(2分); Fe3++3H2O Fe(OH)3+ 3 H+(2分)
Fe(OH)3+ 3 H+(2分)
【解析】
试题分析:铝热反应常被用来焊接钢轨,所以①为铝热反应;M在空气中变为N,N受热分解,判断N是氢氧化铁,M是氢氧化亚铁,B为氧化铁,则A是Al;工业上常电解食盐水产生氯气、氢气、氢氧化钠,因为M是氢氧化亚铁,所以D为Fe,C是氧化铝;G为氯气,氯气与铁反应生成氯化铁,则J是氯化铁,K为氯化亚铁,氯化亚铁与氢氧化钠反应生成氢氧化亚铁,所以H为氢氧化钠,I是氢气,F是氯化钠,氧化铝与氢氧化钠溶液反应生成四羟基合铝酸钠 ,E是四羟基合铝酸钠。
(1)H是氢氧化钠,含有离子键和共价键;
(2)在上述反应中,铁与氯气的反应、氯化铁与铁的反应、氢氧化亚铁与氧气、水的反应都是化合反应且是氧化还原反应,共3个;反应③是氧化铝与氢氧化钠溶液反应生成四羟基合铝酸钠,离子方程式是Al2O3+2OH-+3H2O=2[Al(OH)4]-;
(3)电解饱和食盐水的化学方程式为2NaCl+2H2O 2NaOH+H2↑+Cl2↑,阴极是氢离子放电产生氢气,同时溶液变红色,所以氢气的质量是0.2g,物质的量是0.1mol,则氢氧化钠的物质的量是0.2mol,所以氢氧根离子的浓度是0.2mol/2L=0.1mol/L,则氢离子浓度是10-13mol/L,溶液的pH=13;
2NaOH+H2↑+Cl2↑,阴极是氢离子放电产生氢气,同时溶液变红色,所以氢气的质量是0.2g,物质的量是0.1mol,则氢氧化钠的物质的量是0.2mol,所以氢氧根离子的浓度是0.2mol/2L=0.1mol/L,则氢离子浓度是10-13mol/L,溶液的pH=13;
(4)J为氯化铁,铁离子的水解使溶液呈酸性,离子方程式为Fe3++3H2O Fe(OH)3+ 3 H+。
Fe(OH)3+ 3 H+。
考点:考查无机推断,物质性质的应用,离子方程式、化学方程式的书写,化学键的判断,溶液pH的计算


科目:高中化学 来源:2014-2015学年上海市虹口区高三上学期期末考试化学试卷(解析版) 题型:选择题
下列实验过程中,始终无明显现象的是
A.NO2通入FeSO4溶液中 B.CO2通入CaCl2溶液中
C.NH3通入AlCl3溶液中 D.SO2通入Ba(NO3)2溶液中
查看答案和解析>>
科目:高中化学 来源:2014-2015学年陕西省五校高三第一次模拟联考理综化学试卷(解析版) 题型:选择题
某pH=1的X溶液中可能含有Fe2+、A13+、NH4+、CO32―、SO32―、SO42―、C1―中的若干种,现取X溶液进行连续实验,实验过程及产物如下:

下列说法正确的是
A.气体A是NO2
B.X中肯定存在Fe2+、A13+、NH4+、SO42―
C.溶液E和气体F不能发生化学反应
D.X中不能确定的离子是 A13+和C1―
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西省等四校高三第二次联考化学试卷(解析版) 题型:选择题
近年来化学科学家采用“组合转化”技术,将二氧化碳在一定条件下转化为重要的化工原料乙烯:2CO2(g)+6H2(g)  C2H4(g)+4H2O(g);△H=+1411.0 kJ/mol,关于该反应,下列图示与对应的叙述相符的是
C2H4(g)+4H2O(g);△H=+1411.0 kJ/mol,关于该反应,下列图示与对应的叙述相符的是

A.图1表示该反应分别在有、无催化剂的情况下反应过程中的能量变化
B.图2表示一定条件下反应达到平衡后改变压强反应物的转化率的变化
C.图3表示一定条件下反应达到平衡后改变温度反应平衡常数的变化
D.图4 表示一定条件下反应达到平衡后改变温度、压强产物百分含量的变化
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西省等四校高三第二次联考化学试卷(解析版) 题型:选择题
已知A、B为单质,C为化合物。且有如下转化关系

①若C溶于水后得到强碱溶液,则A可能是Na
②若C溶液与Na2CO3溶液反应,放出CO2气体,则A可能是H2
③若C溶液中滴加NaOH溶液,先生成沉淀后又溶解,则B可能为Al
④若C溶液中滴加NaOH溶液有蓝色沉淀生成,则B可能为Cu
能实现上述转化关系的是
A.①② B.②④ C.①③ D.③④
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东师大附中高三第四次模拟考试理综化学试卷(解析版) 题型:选择题
下列说法中,不正确的是
A.短周期元素中,最外层电子数是其电子层数两倍的元素共有3种
B.第三周期元素的离子半径大小比较:S2->Cl->Na+>Mg2+>Al3+
C.日本核电站释放出的131I、132I和133I属于同素异形体
D.相同条件下,测定同浓度的Na2CO3溶液和Na2SO4溶液的pH,可比较C和S的非金属性强弱
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省曲阜市高三上学期期中考试化学试卷(解析版) 题型:填空题
(131分)某利,盐溶解后得到的溶液中,可能含有Fe2+、Fe3+、SO42-、NH4+、Ba2+、CO32-离子中的某几种。
(1)甲同学做如下实验:①取少量溶液于试管中逐滴加人浓氢氧化钠溶液,发现先生成白色沉淀,迅速变为灰绿色,最后变为红揭色,并有刺激性气体生成;②另取少量溶液于试管中,加人少量盐酸酸化的氯化钡溶液,有白色沉淀生成。该溶液中一定含有的离子是_____;写出①中白色沉淀转化为红褐色沉淀的化学方程式__________________。
(2)乙同学做如下实验:取少量溶液于试管中,滴加几滴硫氰酸钾溶液,无明显现象;再滴加H2O2发现溶液变红色。继续滴加H2O2,红色逐渐褪去且有气泡产生。为弄清其中缘由,他查阅资料知:
①该反应中,被氧化的元素为__________,每生成1molCO2转移的电子数为___________;
②根据乙同学的实验现象,请判断还原性强弱为:Fe2+__________SCN-(填<、=或>);
③根据资料,乙同学提出的猜想是:H2O2将SCN-氧化使红色逐渐褪去。请你设计一个实验,验证乙同学的猜想是否正确_____________________________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省曲阜市高三上学期期中考试化学试卷(解析版) 题型:选择题
下列推断正确的是
A.SiO2能与NaOH溶液、HF溶液反应,所以SiO2是两性氧化物
B.Na2O、Na2O2组成元素相同,阳离子与阴离子个数比也相同
C.CO、NO、NO2都是大气污染气体,在空气中都能稳定存在
D.新制氯水显酸性,向其中滴加少最紫色石蕊试液,充分振荡后溶液呈红色
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省高三12月学情调研化学试卷(解析版) 题型:选择题
下列物质的转化在给定条件下能实现的是
①
②
③
④
⑤
A.①⑤ B.②⑤ C.③④ D.②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com